Материал: Шмид Р. Наглядная биотехнология и генетическая инженерия
D,L-Метионин |
|
С5Н11NO2S |
|
MR |
149,21 |
Код CAS |
63-68-3 |
L-Лизин |
|
С6Н14N2O2 |
|
MR |
146,19 |
Код CAS |
56-87-1 |
L-Треонин |
|
С4Н9NO3 |
|
MR |
119,12 |
Код CAS |
72-19-5 |
Аминокислоты в кормах |
|
|
|
|
|
|
||
Пшеница |
без добавок |
|
|
|
|
|
||
|
|
|
|
|
|
|||
|
L-лизин 0,25% |
|
|
|
|
|
||
L-лизин 0,4% + L-треонин 0,4% |
|
|
|
|
|
|||
Кукуруза |
без добавок |
|
|
|
|
|
||
|
|
|
|
|
|
|||
|
L-лизин 0,05% |
|
|
|
|
|
||
L-лизин 0,4% + L-триптофан 0,35% |
|
|
|
|
|
|||
Рис |
без добавок |
|
|
|
|
|
||
|
|
|
|
|
|
|||
|
L-лизин 0,1% |
|
|
|
|
|
||
L-лизин 0,2% + L-треонин 0,1% |
|
|
|
|
|
|||
Для сравнения: |
казеин без добавок |
|
|
|
|
|
||
|
|
0 |
0,5 |
1,0 |
1,5 |
2,0 |
2,5 |
|
|
|
|
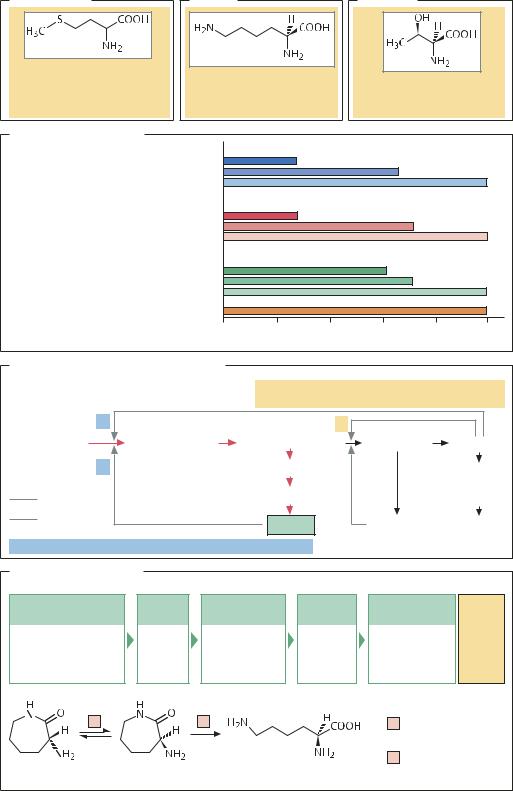
Относительная пищевая ценность при откорме свиней |
|||||
Биосинтез и штаммы-суперпродуценты |
|
|
|
|
|
|||
Синтез L-лизина в клетках |
|
Мутанты с заблокированными побочными процессами |
||||||
Corynebacterium glutamicum |
|
|||||||
|
в среде с L-гомосерином |
|
|
|
||||
|
|
|
|
|
|
|||
2 |
|
|
|
1 |
|
|
|
|
Аспарагиновая |
|
|
Полуальдегид |
|
|
|
||
Аспартилфосфат |
|
аспарагиновой кислоты |
L-Гомосерин |
L-Треонин |
||||
кислота |
|
|||||||
|
|
|
|
|
|
|
||
2 |
|
|
Дегидродипиколиновая |
|
|
|
||
|
|
кислота |
|
|
2-Оксо- |
|||
|
|
|
|
|
||||
|
|
|
Диаминопимелиновая |
|
|
масляная |
||
|
|
|
|
|
кислота |
|||
Ингибирование |
|
|
кислота |
|
|
|||
|
|
|
|
|
||||
Репрессия |
|
|
L-Лизин |
L-Метионин |
L-Изолейцин |
|||
|
|
|
||||||
В мутантных штаммах нет ингибирования L-лизином и L-треонином |
|
|
|
|||||
Производство L-лизина |
|
|
|
|
|
|
||
|
Основной метод получения: ферментация |
|
|
|
||||
Штаммы- |
Предфер- |
Основная |
Удаление |
Очистка |
Выход |
|||
суперпродуценты |
ментация |
ферментация |
клеток |
|
|
L-лизина |
||
Мутанты по регулятор- |
30 м3, |
500 м3, декстроза, |
Сепаратор |
Ионообменная |
120 г/л |
|||
ным ферментам или |
декстроза, |
соевая мука, |
или ультра- |
хроматография, |
через |
|||
80 ч |
||||||||
ауксотрофные мутанты |
соевая |
оптимизирован- |
фильтрация |
перекристалли- |
||||
фермен- |
||||||||
Corynebacterium |
мука |
ные условия |
|
зация или сушка |
||||
|
тации |
|||||||
glutamicum |
|
массопереноса |
|
распылением |
||||
|
|
|
||||||
Другая технология: каскадная реакция в биореакторе |
|
|
|
|||||
1 |
2 |
|
|
|
1 |
ACL-рацемаза: |
||
|
|
|
|
|
Achromobacter obae |
|||
|
|
|
|
|
2 |
ACL-гидролаза: |
||
D-α-амино- |
L-α-амино- |
|
L-лизин |
|
Cryptococcus laurentii |
|||
|
|
|
|
|
||||
ε-капролактам (ACL) |
ε-капролактам |
|
|
|
|
|
35 |
|
|
|
|
|
|
|
|
||
Спирты, кислоты и аминокислоты
36
Аспартам™, L-фенилаланин и L-аспарагиновая кислота
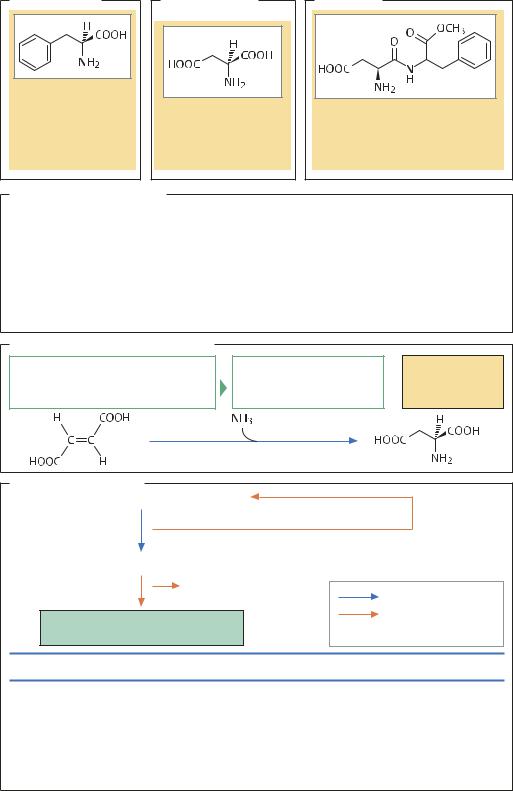
ВВЕДЕНИЕ. Аспартам (метиловый эфир L-α-аспартил- L-фенилаланина) – это низкокалорийный искусственный подсластитель, который по сладости в 200 раз превосходит сахар, полученный из сахарной свеклы. Объем производства аспартама составляет 30 000 т/г (2004). Исходными веществами для синтеза аспартама являются L-аспарагиновая кислота и L-фенилала- нин. При химическом синтезе аспартама требуются дополнительные затраты на введение защитных групп в молекулы исходных веществ, поэтому в настоящее время применяют ферментативные методы получения этого продукта.
L-АСПАРАГИНОВАЯ КИСЛОТА. Одним из методов получения L-аспарагиновой кислоты является экстракция из белкового гидролизата, однако экономически более выгодным оказался синтез клетками Escherichia coli из фумаровой кислоты в присутствии аммиака. Реакцию осуществляет фермент аспартаза, находящаяся в клетках микроорганизма. Как правило, для выращивания клеток используют реактор, в котором бактерии иммобилизованы на κ- каррагинане или полиакриламиде. Выход продукта в такой системе достигает 140 г/(л ч), а срок службы биокатализатора на основе иммобилизованных клеток составляет два года. Использование сублимированных клеток промышленных штаммов позволяет получать до 166 г L-аспарагиновой кислоты с литра клеточной культуры. В лабораторных условиях удалось получить штамм E. coli с плазмидой, несущей ген аспартазы (aspA). В таком штамме выход L-аспарагиновой кислоты увеличивается в 30 раз.
L-ФЕНИЛАЛАНИН. Традиционно производство L-фе- нилаланина осуществлялось в ферментативных реакторах на доступном сырье. В последнее время в связи с развитием молекулярно-биологических методов, позволяющих получать генетически модифицированные штаммы-суперпродуценты, все шире используют ферментацию. Распространение ферментативных методов объясняется доступностью и невысокой стоимостью синтетического сырья, а также выгодным соотношением между производственными площадями, временными затратами и выходом продукта. Для производства L-фенилаланина наиболее выгодным оказалось использование биореактора, в котором в присутствии аммиака происходит аминирование коричной кислоты под действием фермента фенилаланинаммиаклиазы из Rhodotorula glutinis. В таком реакторе выход продукта достигает 50 г/л, а эффективность переработки сырья составляет 83%. Перспективным также считается метод расщепления D,L-5-бензилгидантоина ферментами L-гидантоина- зой и L-N-карбамоилазой, выделенными из Flavobacterium ammoniagenes. Для ферментации в биореакторах в современном производстве, как правило,
используют штаммы-суперпродуценты E. coli или коринебактерий. В этих организмах биосинтез L-фени- лаланина из эритрозо-4-фосфата и фосфоенолпирувата протекает в несколько стадий. В качестве промежуточных соединений образуются шикимовая, префеновая и фенилпировиноградная кислоты, в диком штамме они предшественники L-триптофана и L-тирозина. Однако в промышленности используют мутантные ауксотрофные штаммы, в которых активность ключевых ферментов строго регулируется. Практически все гены, продукты которых участвуют в биосинтезе L-фенилаланина, к настоящему времени клонированы. Это позволяет получать новые штам- мы-суперпродуценты, применяя генно-инженерные методы. Так, выход L-фенилаланина в одном из рекомбинантных штаммов Brevibacterium fermentum
составляет 45 г на литр клеточной культуры. После завершения ферментации по воздушно-проточному способу клетки отделяют, а затем концентрируют культуральную жидкость ульрафильтрацией. Для окончательной очистки L-фенилаланина применяют ионообменную хроматографию или кристаллизацию. АСПАРТАМТМ. Для синтеза аспартама из L-аспараги- новой кислоты и L-фенилаланина необходимо сначала ввести в исходные молекулы пять защитных групп, а в конце синтеза их удалить. Такой метод значительно сложнее синтеза с использованием протеиназы. В обычных условиях протеолитические ферменты катализируют гидролиз пептидных связей, однако возможно сдвинуть равновесие в сторону образования пептидной связи. Так, в концентрированных растворах, содержащих L-аспарагиновую кислоту (в которой аминогруппа защищена бензилоксикарбонилом) и метиловый эфир L-фенилаланина, протеиназа катализирует образование малорастворимого пептида, который выпадает в осадок. Особенно важно, что в этой реакции принимает участие только α-карбоксильная группа L-аспарагиновой кислоты, так как изомер аспартама – метиловый эфир L-β-аспартил-L-фенилаланина – обладает сильно выраженным горьким вкусом. В промышленном производстве, как правило, используют иммобилизованную протеиназу термолизин, выделенную из Bacillus thermoproteolyticus. Этот фермент устойчив к высоким температурам и может осуществлять реакцию при 70 °С, что значительно повышает эффективность процесса (выход продукта достигает 30 г/л). Образовавшийся аспартам в значительной степени отделен от побочных продуктов, так что для окончательной очистки от примеси исходных веществ достаточно ионообменной хроматографии.
Copyright ОАО «ЦКБ «БИБКОМ» & ООО «Aгентство Kнига-Cервис»
L-Фенилаланин |
L-Аспарагиновая |
||
|
|
кислота |
|
С9Н11NO2 |
|
С4Н7NO4 |
|
MR |
165,19 |
MR |
133,10 |
Тпл |
310–312 °C |
Код CAS |
56-84-8 |
Код CAS |
63-91-2 |
|
|
Получение L-фенилаланина |
|
|
|
α-Аспартам |
|
С14Н18N2O5 |
|
MR |
294,31 |
Максимальная |
40 мг/кг |
суточная доза |
|
Код CAS |
22389-47-0 |
Наиболее распространенный метод – ферментация |
|
|
Штаммы-суперпродуценты: |
Источник С: глюкоза |
Более 40 г/л |
коринебактерии |
Очистка: использование мембран, |
через 60 ч роста |
или E. coli |
ионообменная хроматография, |
|
|
перекристаллизация |
|
|
|
|
|
Другой метод – ферментативный реактор |
|
Добавление аммиака |
Иммобилизованный фермент |
Около 50 г/л при 83% |
к транс-коричной кислоте |
L-фенилаланин-аммиаклиаза |
конверсии сырья |
|
из Rhodotorula glutinis |
|
Получение L-аспарагиновой кислоты
Многоступенчатая реакция в биореакторе |
|
Очистка |
Выход 90–95%, |
|
Иммобилизованные клетки E. coli; |
Добавление H2SO4 при 15 °С |
|||
срок службы клеток |
||||
1,2 М фумаровая кислота, аммиак, |
(рН 2,8) приводит к выпадению |
E. coli 2 года |
||
рН 8,5, 37°С |
|
аспарагиновой кислоты в осадок |
|
|
|
|
Аспартаза (иммобилизованные клетки E. coli) |
|
|
|
|
Получение α-аспартама |
|
|
|
|
|
L-Z-аспарагиновая кислота + D,L-фенилаланин-ОМе |
|
|
|
||
иммобилизованый |
|
|
|
рацемизация |
|
|
|
|
|
|
|
термолизин |
|
D-фенилаланин-ОМе |
|
|
|
(60 °С, 2 ч) |
|
|
|
||
L-Z-α-аспартил-L-фенилаланин-ОМе |
|
|
|
||
гидрирование |
ZH |
ферментативный катализ |
|
||
|
|
|
|
||
L-α-аспартил-L-фенилаланин-ОМе |
химические реакции |
|
|||
|
|
|
|||
|
α-Аспартам |
Z = бензилоксикарбонил |
|
||
Подсластитель |
Химическое строение |
|
Относительная |
|
|
|
|
|
|
сладость |
|
Сахароза |
Дисахарид |
|
|
1 |
|
Цикламат |
Синтетическая циклогексилсульфаминовая кислота, натриевая соль |
40 |
|
||
α-Аспартам |
Дипептид, метиловый эфир |
|
200 |
|
|
Стевиозид |
Гликозилированный дитерпен |
|
300 |
|
|
Сахарин |
Синтетический имид 2-сульфобензойной кислоты, натриевая соль |
450 |
|
||
Тауматин |
Негликозилированный белок – одна полипептидная цепь |
|
2500 |
|
|
|
из 208 аминокислотных остатков |
|
|
||
Монеллин |
Негликозилированный белок – две полипептидные цепи |
|
2500 |
|
|
|
из 44 и 50 аминокислотных остатков |
|
37 |
||
|
|
|
|
|
|
Спирты, кислоты и аминокислоты
Получение L-аминокислот
путем ферментативной трансформации
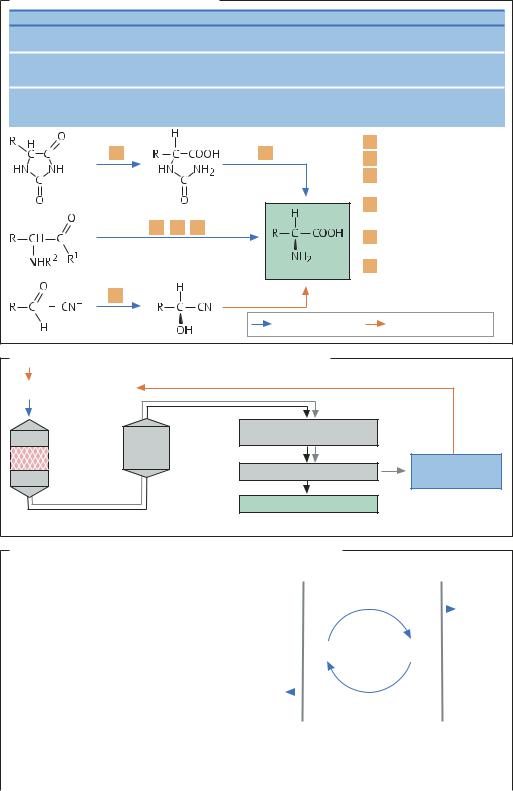
ВВЕДЕНИЕ. Как мы уже видели на примере L-лизина, L-аспарагиновой кислоты и L-фенилаланина, тот или иной энантиомер аминокислоты можно получить путем ферментативных превращений предшественников. В отличие от ферментации использование энантиоспецифичных ферментов позволяет синтезировать небелковые аминокислоты. Для этой цели наиболее широко используют гидролазы, селективно расщепляющие определенные энантиомеры в рацемате. В качестве примера можно привести эстеразы, аминоацилазы, амидазы и гидантоиназы. Недостаток метода заключается в необходимости удаления «неправильного» энантиомера из реакционной смеси, его рацемизации и повторного введения в реакцию. В другом методе используются реакции присоединения, катализируемые лиазами (например, оксинитрилазами), или окислительно-восстановитель- ные реакции, катализируемые оксидоредуктазами; в этих реакциях образуются только «правильные» энантиомеры.
ЭНАНТИОСЕЛЕКТИВНЫЙ ГИДРОЛИЗ. Наиболее хорошо изучены и активно применяются в современных промышленных процессах аминоацилазы и гидантоиназы. Для осуществления гидролиза рацемата N-ациламинокислот используют иммобилизованную ацилазу, выделенную из Aspergillus oryzae или Baсillus thermoglucosidius. В реакции участвуют только L-энантиомеры, а N-ацил-D-аминокислоты, оставшиеся в реакционной смеси после кристаллизации L-аминокислот, подвергают термической рацемизации и снова вводят в реакцию. Таким способом ежегодно производят сотни тонн L-метионина, L-тирози- на, L-пролина и L-валина для медицинских нужд. Аналогичным образом можно получать и D-амино- кислоты, однако более выгодно использовать доступные предшественники аминокислот – гидантоины. После расщепления гидантоинов специфическими гидантоиназами образуются N-карбамоил- аминокислоты, которые в свою очередь могут быть превращены в D- или L-аминокислоты при помощи карбамоилаз. «Ложный» гидантоин прекращает ферментативную рацемизацию и в ходе оптимизированного путем генетических технологий ферментативного каскада приводит к количественному выходу абиогенных L- и D-аминокислот. Свойство «неправильного» гидантоина рацемизоваться при рН 8,5 легло в основу нового метода, перспективного для промышленного получения D-фенилглицина и 4-гидроксифенилглицина – важных предшественников полусинтетических пенициллинов ампициллина и амоксициллина.
ЭНАНТИОСЕЛЕКТИВНЫЕ РЕАКЦИИ ПРИСОЕДИНЕНИЯ.
оксинитрилазы – ферменты из растительных тканей.
Внастоящее время R- и S-оксинитрилазы получены в виде рекомбинантных белков в клетках E. coli; при этом ген R-оксинитрилазы клонирован из маниока, а ген S-оксинитрилазы – из миндаля. Определена пространственная структура обоих ферментов и с помощью методов белковой инженерии предприняты попытки усовершенствовать ферменты для промышленного применения.
ЭНАНТИОСЕЛЕКТИВНЫЕ ОКИСЛИТЕЛЬНО-ВОССТАНО- ВИТЕЛЬНЫЕ РЕАКЦИИ. На примере стереоселективного синтеза L-лейцина из α-оксоизокапроновой кислоты видно, что для восстановительного аминирования с помощью L-лейциндегидрогеназы из Bacil-
lus sp. кроме NH3 необходим NADH. Ввиду высокой стоимости кофермента необходимо создать систему его регенерации. Очень элегантно эта проблема решена в случае формиатдегидрогеназы из Candida boi-
dinii: CO2 – один из побочных продуктов реакции – сдвигает равновесие в сторону образования L-лейци- на. Использование NADH, связанного с полиэтиленгликолем (ПЭГ), позволяет получать до 600 000 молярных эквивалентов продукта из одного моля NADH.
Впромышленности восстановление NADH в окисли- тельно-восстановительных реакциях происходит на неизменяющемся коэнзиме в порционном режиме. Еще более интенсивно подобный процесс происходит
сучастием измененных (путем Protein Design или направленной эволюции) ферментов в генетически модифицированных микроорганизмах.
Для осуществления реакций, специфичных для 38 R- и S-энантиомеров, используют соответствующие
Copyright ОАО «ЦКБ «БИБКОМ» & ООО «Aгентство Kнига-Cервис»
Наиболее хорошо изученные реакции |
|
|
|
||||
Тип реакции |
Класс фермента |
Комментарий |
|
|
|||
Гидролиз рацемических |
Гидролазы |
|
Простая, широко применяемая, но дорогостоящая реакция, так как |
||||
смесей предшествеников |
|
|
|
«неправильный» энантиомер необходимо вновь рацемизировать |
|||
Присоединение |
Лиазы |
|
|
Простая реакция с количественным выходом; |
|||
HCN или NH3 |
|
|
|
недостаток – малый выбор ферментов |
|
||
по карбонильной группе |
|
|
|
|
|
|
|
Восстановительное |
Дегидрогеназы |
Образуется только один энантиомер, однако это процесс |
|||||
аминирование |
|
|
|
дорогой из-за затрат на системы регенерации кофакторов |
|||
α-оксокарбоновых кислот |
|
|
|
|
|
|
|
1 |
|
|
|
|
2 |
1 |
Гидантоиназы |
|
|
|
|
2 |
Карбамоилазы |
||
|
|
|
|
|
|
||
|
|
|
|
|
|
3 |
Эстеразы |
|
|
|
|
|
|
|
(R1 = OR, R2 = H) |
|
|
|
|
|
|
4 |
Аминоацилазы |
|
|
|
|
|
|
|
(R1 = OH, R2 = Acyl) |
|
3 |
4 |
5 |
|
|
5 |
Амидазы |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
(R1 = NH2, R2 = H) |
|
|
|
|
|
L-Аминокислота |
6 |
Оксинитрилазы |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Например, |
|
6 |
|
|
|
|
|
L- или S-специфические |
|
|
|
|
|
|
|
ферменты |
|
|
|
|
|
|
Ферментативный |
|
Реакции химического |
|
|
|
|
|
катализ |
|
синтеза |
Энантиоселективное расщепление D,L-N-ациламинокислот |
|
|
|||||
N-Ацетил-D,L-аминокислоты |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рацеми- |
Иммоби- |
|
|
|
|
Кристаллизатор |
|
зация |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
лизован- |
|
|
|
|
|
|
|
ная амино- |
|
|
|
|
|
|
N-Ацетил- |
ацилаза |
|
|
|
|
Сепаратор |
|
|
Испаритель |
|
|
D-аминокислота |
||||
|
|
|
|
||||
|
|
|
|
|
|||
|
(растворитель, |
L-Аминокислота |
|
Не кристаллизуется |
|||
|
уксусная кислота) |
|
|
||||
|
|
|
|
|
Кристаллизуется |
|
|
Восстановительное аминирование α-оксокарбоновых кислот |
|
|
|||||
Лейциндегидрогеназа, обладающая широкой |
|
|
Мембранный ферментный реактор |
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
субстратной специфичностью, осуществляет реакцию |
|
|
|
|
|
|
|
|
|
|
|
|
||||
аминирования не только лейцина, |
|
|
|
|
|
L-Лейциндегидрогеназа |
|
|
|
|
|
|
|
|||
но и других α-оксокарбоновых кислот. |
|
|
α-Оксо- |
|
|
|
|
|
|
|
L-Лейцин |
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
||||||
При этом образуются небелковые аминокислоты, |
изокап- |
|
|
|
|
|
|
|
|
|
||||||
например L-лейцин. |
|
|
|
ронат |
до 106 циклов |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
Лейциндегидрогеназа |
Относительная |
K , mM |
|
|
|
ПЭГ-NADH |
ПЭГ-NADH+ |
|
|
|
|
|
|
|
|
|
из Bacillus sphaericus |
активность |
M |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
α-оксоизокапронат |
100 |
0,31 |
|
СО2 |
|
|
|
|
|
|
|
Муравьиная |
|||
|
α-оксоизовалериат |
126 |
1,4 |
|
|
Формиатдегидрогеназа |
|
|
|
кислота |
||||||
|
α-оксовалериат |
76 |
1,7 |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
α-оксобутират |
57 |
7,7 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Мембрана для |
||||||||||||
|
α-оксокапронат |
46 |
7,0 |
|
|
|
|
|
||||||||
|
|
|
|
|
|
ультрафильтрации |
||||||||||
ПЭГ-NADH – синтетическое производное NADH с MR = 3000. Многие дегидрогеназы способны использовать |
||||||||||||||||
его в качестве кофактора. Для удерживания ПЭГ-NADH в реакционной смеси используют ультрафильтрацию. |
||||||||||||||||
Реакция протекает со свободным NADH и расходованием продукта. |
|
|
|
|
|
|
|
|
39 |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||