Материал: Шмид Р. Наглядная биотехнология и генетическая инженерия
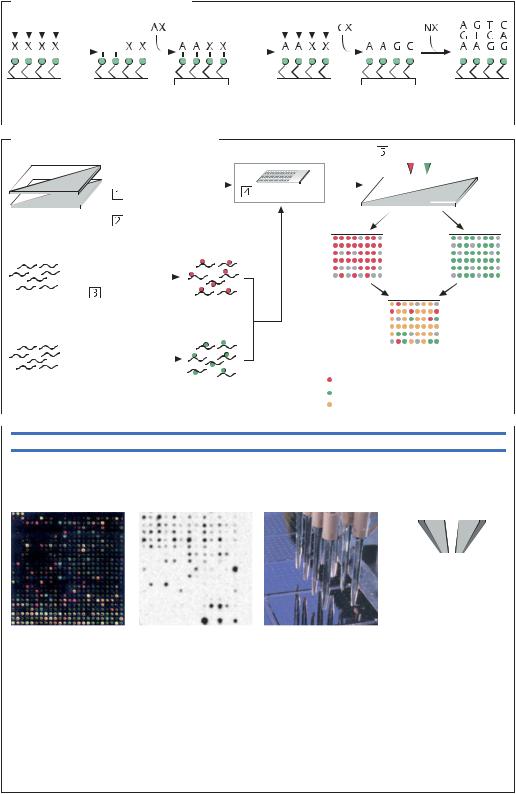
Введение радиоактивной метки |
|
Проточная цитометрия с использованием |
||||
Введение 32P-dATP |
|
|
флуоресцентной метки (FACS*) |
|||
|
|
|
Электрод |
|
||
|
|
|
|
|
|
|
|
Фрагмент Клёнова |
|
|
Пьезо- |
||
|
|
|
преобразователь |
|||
|
+ 32P-dATP |
|
|
|
||
Липкий |
|
|
|
|
|
|
|
Меченые |
|
Кювета |
|
|
|
конец (EcoRI) |
|
|
|
|
||
концы |
|
|
|
Лазерный |
||
|
|
|
|
|
||
|
|
|
|
|
|
луч |
Гибридизация с радиоактивно меченными зондами |
|
|
|
|||
|
|
|
|
Заземление |
Меченые клетки |
|
|
|
|
|
|
||
|
|
|
|
|
Немеченые клетки |
|
Носитель |
Разделение |
|
|
Заряженные |
* FACS – метод |
|
|
|
пластины |
||||
с иммобили- |
хромосомы |
Зонд, |
|
сортировки клеток |
||
|
|
с флуоресцентной |
||||
зованными |
|
авторадио- |
|
меткой |
||
клетками |
|
графия |
|
|
|
|
Положение пятен |
|
|
Вакуум |
|
|
|
на авторадио- |
|
|
|
|
|
|
грамме указывает |
|
|
|
|
|
|
на локализацию |
|
|
|
|
|
|
исследуемого |
|
|
|
|
|
|
гена на хромосоме |
|
|
X/Y-столик |
|
|
|
|
|
|
|
|
|
|
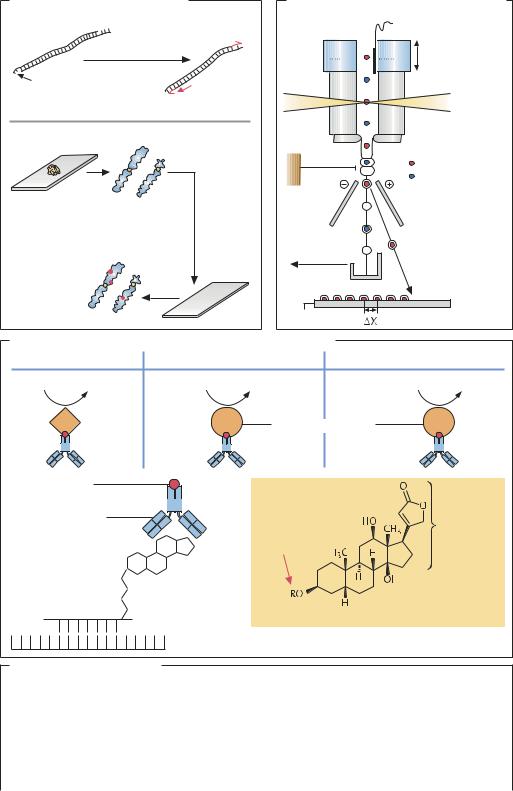
Оптические методы наблюдения результатов гибридизации |
|
|
||||
Флуоресценция |
Хемилюминесценция |
Визуальное наблюдение |
||||
hν1 |
hν2 |
Диоксетан |
hν |
|
Индолилфосфат |
Индиго |
|
|
|
|
Щелочная фосфатаза |
|
|
Метка |
|
|
|
|
|
|
Антитело |
|
|
Сайт связывания |
|
Участок |
|
|
|
|
связывания |
|||
|
|
|
|
с ДНК через |
|
|
|
|
|
|
|
с антителом |
|
|
|
|
|
спейсер |
|
|
|
|
|
|
|
|
|
Дигоксигенин |
|
|
|
|
|
|
(гаптен) |
|
|
|
|
|
|
|
|
Спейсер |
|
|
|
|
|
|
Зонд |
|
|
Дигоксигенин |
|
|
|
|
|
|
|
|
|
|
Мишень (последовательность) |
|
|
||
Часто используемые метки |
|
|
|
|
|
|
|
Ген |
Субстрат |
Детектирование |
|
|
|
lacZ ': фрагмент гена |
5-Бром-4-хлор-3-индолил- |
Белый или голубой цвет |
|
|
|
β-галактозидазы |
β-D-Галактопиранозид (X-Gal) |
|
|
|
|
lux: люцифераза светляков |
Люциферин |
Люминесценция |
|
|
|
или фотобактерий |
|
|
|
|
|
GFP: зеленый флуоресцентный |
– |
Флуоресценция |
|
|
|
белок из медузы |
|
|
|
267 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

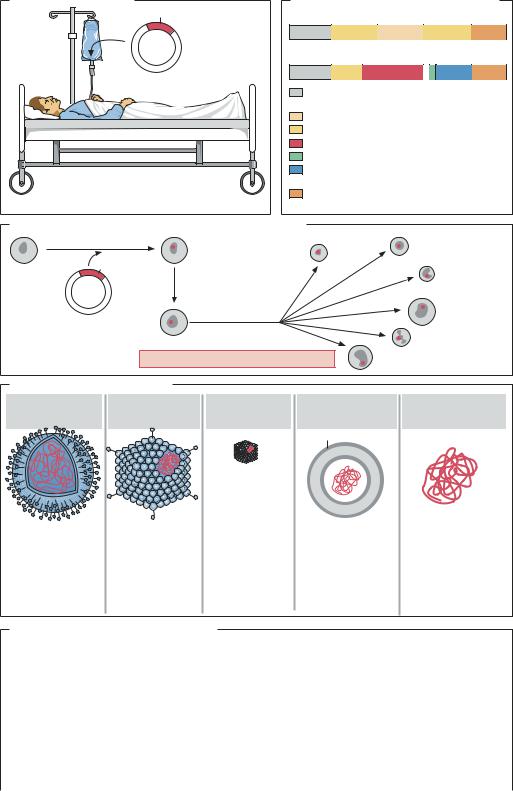
Генная терапия in vivo |
|
Вектор на основе генома ретровируса |
|||
|
кДНК человека |
Геном ретровируса |
|
|
|
|
|
|
|
|
|
|
Вектор |
|
|
|
|
|
с полноценным |
Вектор на основе генома ретровируса |
|||
|
геном |
||||
|
|
|
5'-Концевая последовательность |
||
|
|
|
инициации транскрипции |
||
|
|
|
Обратная транскриптаза, интеграза |
||
|
|
|
Белок капсида вируса |
||
|
|
|
Конструкция, несущая кДНК человека |
||
|
|
|
Промотор |
|
|
|
|
|
Селективный маркер, например, |
||
|
|
|
устойчивости к неомицину (NeOR) |
||
|
|
|
3'-Концевая последовательность |
||
|
|
|
с сигналом полиаденилирования |
||
Генная терапия ex vivo (на примере стволовых клеток) |
|
|
|||
Трансфекция |
|
Т-клетки |
|
В-клетки |
|
|
|
|
|
||
|
|
|
|
|
|
кДНК человека |
Имплантация |
|
|
Базофилы |
|
Взятые |
|
|
|
||
у пациента |
|
клеток пациенту |
|
|
|
стволовые |
|
|
|
|
|
клетки |
|
|
|
|
|
Вектор, |
|
Дифференцировка |
|
|
Моноциты |
|
|
|
|
||
несущий |
|
|
|
|
|
|
клеток |
|
|
Нейтрофилы |
|
полноценный |
|
|
|||
ген |
Все зрелые клетки несут нормальный ген |
Эозинофилы |
|||
|
|||||
Векторы для генной терапии |
|
|
|
|
|
Ретровирусы |
Аденовирусы |
Адено- |
Липосомы |
|
Чистая ДНК |
|
|
ассоциирован- |
|
|
|
|
|
ные вирусы |
Липидная мембрана |
|
|
|
|
|
|
||
Преимущества |
Преимущества |
Преимущества |
Преимущества |
|
Преимущества |
Стабильное |
Можно встраивать |
Стабильное |
Нет риска возникно- |
Нет риска возникно- |
|
встраивание в геном |
крупные |
встраивание |
вения заболевания |
вения заболевания |
|
Недостатки |
фрагменты ДНК |
в геном |
в результате терапии |
в результате терапии |
|
Инфицируют |
Недостатки |
Недостатки |
Недостатки |
|
Недостатки |
случайным образом |
Нестабильное |
Можно встраивать |
Невысокая |
|
Невысокая эффектив- |
только делящиеся |
встраивание |
только небольшие |
эффективность |
|
ность доставки ДНК, |
клетки |
в геном |
фрагменты ДНК |
доставки ДНК |
|
нестабильная система |
Применение генной терапии (2004 г.) |
|
|
|
||
|
Заболевание |
Примеры/перенесенные гены |
|
|
|
Злокачественные опухоли |
Гены комплекса гистосовместимости, гены-супрессоры опухолей, |
|
|
|
(более 2000 пациентов, 675 протоколов) |
суицидные гены, IL-2, IL-7 и IL-12, противоопухолевые антитела |
|
|
|
Моногенные заболевания |
Ген SCID-ADA, муковисцидоз, фактор IX, |
|
|
|
(более 300 пациентов, 93 протокола) |
хронический гранулематоз |
|
|
|
Инфекционные заболевания, в основном СПИД |
Трансгенные Т-лимфоциты, ДНК-вакцины |
|
|
|
(около 400 пациентов, 68 протоколов) |
|
|
|
|
Другие заболевания |
VEGF121 (атеросклероз), ревматоидный артрит |
|
|
|
(более 70 пациентов, 184 протокола) |
|
|
|
|
|
|
|
269 |
|
|
|
|
|
|
|
|
|
|