Материал: Шмид Р. Наглядная биотехнология и генетическая инженерия
инженерии |
Функциональный анализ генома человека |
|
|
|
||
ВВЕДЕНИЕ. Целью функционального анализа генома |
человека) и таким образом изучать механизм их дей- |
|||||
|
||||||
|
человека в первую очередь является установление |
ствия. |
В |
этой |
свя- |
|
генетической |
генетических механизмов моногенных или полиген- |
зи особое место занимает анализ генома мыши. |
||||
ных наследственных заболеваний. Для этого необхо- |
Нуклеотидная |
последовательность генома |
мыши |
|||
|
||||||
|
димо идентифицировать гены, отвечающие за фор- |
(3,3 млрд п.н.) полностью расшифрована; показано, |
||||
|
мирование фенотипического признака, а затем |
что геном мыши обладает большим генетическим и |
||||
|
установить, какие изменения в нуклеотидной после- |
физиологическим сходством с геномом человека. |
||||
|
довательности приводят к измененному фенотипу, |
Линии «нокаутных» мышей, у которых направленно |
||||
|
соответствующему симптомам заболевания. Неко- |
выключены определенные гены или регуляторные |
||||
Методы |
торые наследственные заболевания обусловлены |
элементы, служат моделью некоторых заболеваний |
||||
заменой лишь одного нуклеотида (полиморфизм |
человека (например, линия мышей с болезнью Альц- |
|||||
|
||||||
|
одного нуклеотида, или сокращенно снипса, SNP), |
геймера, мыши линии SCID с тяжелым комбиниро- |
||||
|
например муковисцидоз. Данные функционального |
ванным иммунодефицитом). Изучение таких моде- |
||||
|
анализа генома человека необходимы для: 1) генети- |
лей занимает центральное место в фундаментальных |
||||
|
ческого исследования тех участков генома, которые |
и медицинских исследованиях. Результаты этих ис- |
||||
|
могут быть причислены к «областям риска»; 2) раз- |
следований открывают новые перспективы для диаг- |
||||
|
работки новых терапевтических препаратов с новыми |
ностики генетических заболеваний, например с по- |
||||
|
«мишенями»; 3) индивидуального подхода к лечению |
мощью ДНК-чипов: по результатам секвенирования |
||||
|
заболевания с учетом генетических причин патоло- |
определенных областей генома можно предсказать, |
||||
|
гии; 4) генной терапии; 5) изучения молекулярной |
болен ли пациент в настоящее время и насколько ве- |
||||
|
физиологии и патофизиологии человека (см. также |
лик риск развития патологии в будущем. Конечно, |
||||
|
раздел «Протеомика», стр. 272 |
при обсуждении возможностей применения таких |
||||
|
ДИАГНОСТИКА ГЕНЕТИЧЕСКИХ ЗАБОЛЕВАНИЙ. В сос- |
подходов обязательно затрагивается этический ас- |
||||
|
таве двойного хромосомного набора каждый индиви- |
пект проблемы. |
|
|
|
|
|
дуум обладает примерно 6 млн снипсов (SNP) |
МИШЕНИ ДЛЯ ДЕЙСТВИЯ ЛЕКАРСТВЕННЫХ ПРЕПАРА- |
||||
|
(в среднем 1 на 1000 п.н. ДНК). В рамках междуна- |
ТОВ. Если установлено, что причиной наследственно- |
||||
|
родного проекта HapMap к середине 2005 г. в на- |
го заболевания является изменение определенного |
||||
|
учных базах данных должно оказаться около 1 млн |
белка или его сигнальной последовательности, этот |
||||
|
снипсов (SNP) индивидов европейского, китайского, |
белок или белковый комплекс, полученный в реком- |
||||
|
японского и нигерийского происхождения. Если снипс |
бинантной форме, становится мишенью при скринин- |
||||
|
(SNP) находится внутри сайта узнавания некоторой |
ге новых лекарственных препаратов. Однако регуля- |
||||
|
рестриктазы, фермент перестает узнавать этот сайт, |
ция обмена веществ и фармакодинамика в организме |
||||
|
однако по-прежнему расщепляет интактную ДНК в |
(его усвояемость, распределение, метаболизм в орга- |
||||
|
другой хромосоме. Таким образом, данные рестрикт- |
низме и др.) – все это очень усложняет проблему, а |
||||
|
ного анализа отличаются у двух аллелей одного гена, |
изучение действия препарата на рекомбинантные |
||||
|
т. е. наблюдается полиморфизм длины рестрикцион- |
белки – всего лишь начальная стадия пути к лекарст- |
||||
|
ных фрагментов (ПДРФ). Большинство снипсов |
венному препарату. |
|
|
||
|
(SNP) не приводят к фенотипическим проявлениям. |
ФАРМАКОГЕНОМИКА. Целью фармакогеномики яв- |
||||
|
Установление их связи с моногенными (некоторые за- |
ляется установление индивидуальных различий при |
||||
|
болевания крови, брахидактилия) или полигенными |
полигенных заболеваниях (т. е. поиск мишени для |
||||
|
(цвет волос, интеллект, предрасположенность к онко- |
терапии в каждом конкретном случае), изучение осо- |
||||
|
логическим заболеваниям) фенотипическими призна- |
бенностей метаболизма лекарств у пациента и разра- |
||||
|
ками – очень сложная задача. Для ее решения требу- |
ботка индивидуальной стратегии лечения. Предпола- |
||||
|
ется применение самых разнообразных методов, |
гается, что полученные таким способом данные в |
||||
|
прежде всего – анализа сцепленных признаков. Важ- |
будущем смогут помочь при выборе наиболее эффе- |
||||
|
ная информация может быть получена при сравнении |
ктивного лекарства, а также снизить риск возникно- |
||||
|
генома человека с геномами других организмов. Да- |
вения нежелательных побочных явлений. |
|
|||
|
же такие филогенетически отдаленные организмы, |
ГЕННАЯ ТЕРАПИЯ. Детальный анализ структуры и |
||||
|
как плодовая мушка, нематода или дрожжи (Drosophi- |
функций генома человека позволяет использовать |
||||
|
la, Caenorhabditis, Saccharomyces), обладают множе- |
методы генетической инженерии в генной терапии, |
||||
|
ством генов, функционально и структурно сходных с |
например заменять дефектный ген на его полноцен- |
||||
|
генами человека. В исследовательских целях гены |
ную копию. |
|
|
|
|
260 |
этих организмов можно подвергнуть определенным |
|
|
|
|
|
изменениям (что непозволительно делать с генами |
|
|
|
|
||
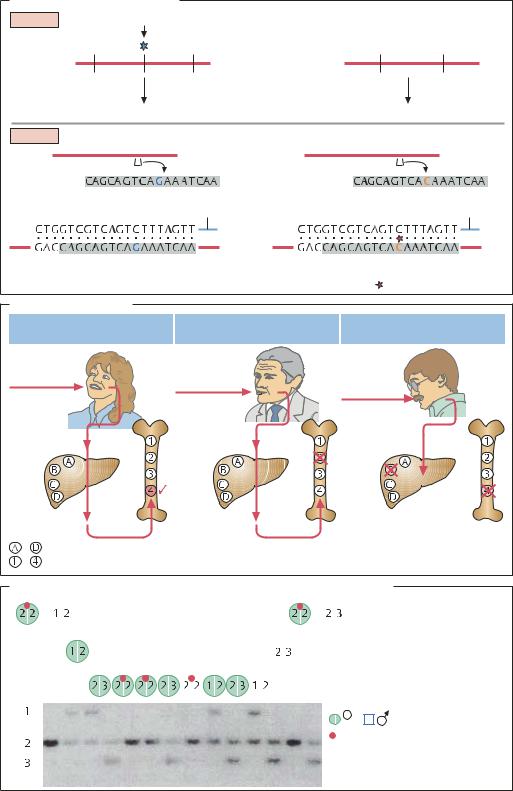
Полиморфизм и снипсы (SNP) |
|
|
|
|
|
Случай 1 Полиморфизм в сайте узнавания рестриктазы |
|
|
|||
ДНК (аллель 1) |
|
ДНК (аллель 2) |
|
|
|
|
Рестрикция |
|
|
Рестрикция |
|
|
4 рестрикционных фрагмента |
|
3 рестрикционных фрагмента |
||
Случай 2 Полиморфизм одного нуклеотида – SNP |
|
|
|
||
Аллель 1 |
|
Аллель 2 |
|
|
|
|
Меченый олигонуклеотидный зонд |
|
|
Метка |
|
|
Полная комплементарность, |
Неполная комплементарность, |
|||
|
стабильный дуплекс ДНК |
|
дуплекс содержит неспаренные |
||
|
|
|
основания ( |
mismatch) |
|
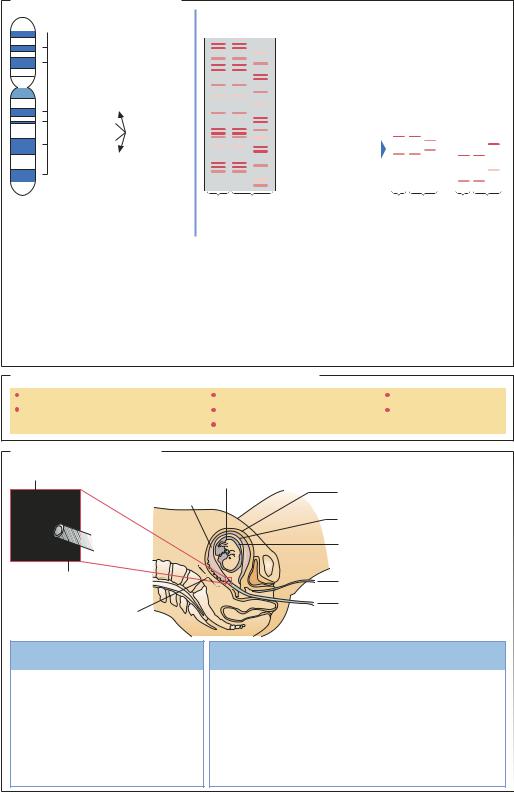
Фармакогеномика |
|
|
|
|
|
Пациент А: лекарство оказывает |
Пациент В: лекарство |
Пациент С: лекарство |
|||
положительное действие |
не оказывает никакого действия |
не оказывает никакого действия |
|||
Лекарство |
Лекарство |
|
Лекарство |
||
|
|
|
|||
|
|
|
|
||
– Этапы обмена веществ, при которых происходит активация лекарства |
|
||||
– |
Этапы обмена веществ, нарушенные при заболевании |
|
|
||
Наследование ПДРФ (полиморфизм длины рестриктных фрагментов) |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Дедушки |
ДНК, взятая у членов |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
и бабушки |
семьи с наследуемой |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
лимфобластомой |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(из коллекции Центра |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Родители |
изучения полимор- |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
физма человека, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Париж). Был создан |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Дети |
ПДРФ-зонд для локуса |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
на хромосоме 5. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Наследование признака |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
продемонстрировано |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
результатами гель- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Гомозиготы |
электрофореза. |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
261

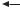 Теломеры,
Теломеры, 
 минисателлиты
минисателлиты
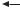 Центромера
Центромера сосредото-
сосредото-  чены в тем-
чены в тем-  ных полосах (G-бэндинг)
ных полосах (G-бэндинг)
 Гипервариабельные
Гипервариабельные  ДНК-минисателлиты
ДНК-минисателлиты