Материал: Шмид Р. Наглядная биотехнология и генетическая инженерия
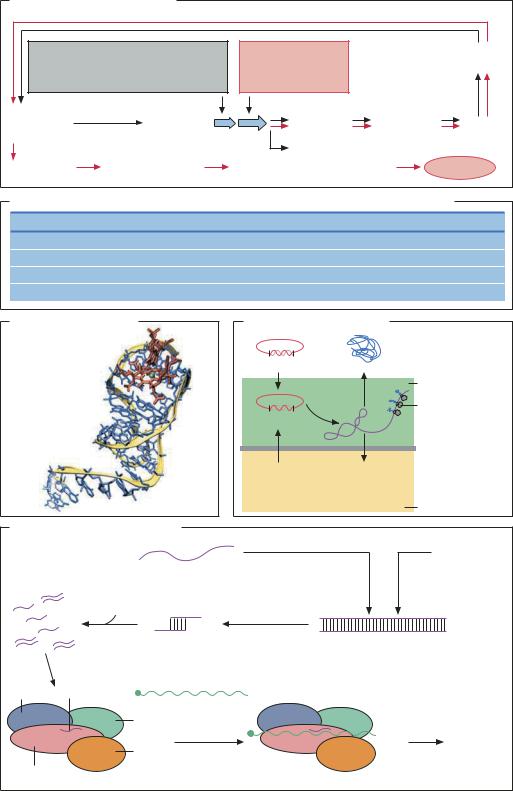
SELEX (получение аптамеров) |
|
|
|
|||
|
|
Транскрипция с помощью РНК-полимеразы фага T7 |
|
|||
Негативная селекция: |
|
Позитивная селекция |
оценка |
ПЦР- |
||
предварительный отбор с целью |
в колонках |
продукт – |
||||
успешности |
ДНК |
|||||
исключения тех РНК, которые |
с иммобилизованным |
|||||
связывания |
|
|||||
неспецифически связываются с матриксом |
лигандом |
Ампили- |
||||
|
||||||
|
|
|
|
|
фикация |
|
Произвольная Транскрипция |
Произвольная |
элюирование |
обратная |
(ПЦР) |
||
кДНК |
||||||
гетерогенная |
|
гетерогенная |
с аффинным |
транскрипция |
||
ДНК |
|
ДНК |
лигандом |
|
||
|
|
|
||||
|
|
|
удаление несвязанной РНК |
|
||
Клонирование |
Определение |
Синтез последовательности in vitro |
Аптамер |
|||
последовательности |
||||||
|
|
|
|
|||
Аптамеры на основе РНК с высоким сродством к внеклеточным белкам (примеры) |
||||||
Целевой белок |
|
Kd (нмоль) |
|
Нуклеиновая кислота |
||
Ацетилхолиновый рецептор |
|
2,0 |
|
РНК |
|
|
Основной фактор роста фибробластов (PGDF) |
|
0,35 |
|
РНК |
|
|
γ-Интерферон |
|
6,8 |
|
2’-Модифицированная РНК |
||
Фактор роста кератиноцитов (KGF) |
|
0,0003 |
|
2’-Модифицированная РНК |
||
Аптамерный комплекс |
|
Биосинтез белков in vitro |
|
|||
Красным |
|
|
|
|
|
|
показан |
|
|
|
|
|
|
витамин B12 |
|
ДНК-матрица |
Белок |
|
||
(1DDY_5) |
|
|
|
|||
|
|
|
|
|
Транс- |
Объем реакционной |
|
|
|
Транс- |
ляция |
системы |
|
|
|
|
крипция |
|
Молекулы тРНК, |
|
|
|
|
T7-полимераза |
|
|
рибосомы |
|
|
|
|
|
|
|
|
|
|
|
|
|
Мембрана |
|
|
|
Нуклеотид- |
Метаболиты, |
|
|
|
|
|
трифосфаты, |
побочные |
|
|
|
|
|
аминокислоты, |
продукты, |
|
|
|
|
|
фосфоенол- |
непереносимый |
|
|
|
|
|
пируват |
субстрат |
Объем реагентов |
|
|
|
|
|
|
|
|
RNAi – интерферирующая РНК |
|
|
|
|
|
|
|
неспецифичная |
|
|
|
|
двухцепочечная |
|
|
|
РНК-зависимая |
|
||
|
одноцепочечная РНК |
|
РНК вирусного |
|||
|
РНК-полимераза |
|
или иного |
|||
|
|
неспецифически |
|
|
происхождения |
|
|
Амплификация |
|
|
|
||
|
расщепляющая |
|
|
|
||
|
Р |
РНКаза (“DICER”) |
|
|
двух- |
|
|
Р |
|
|
|
|
цепочечная |
|
|
|
|
|
РНК |
|
|
Интерферирующий |
|
|
|
|
|
|
|
|
|
|
|
|
|
РНК-дуплекс |
|
|
|
|
|
|
(21–23 нуклеотида) |
|
|
|
|
|
Хеликаза |
«Руководящая» |
|
|
|
|
|
РНК |
|
АААА |
|
|
|
|
|
зрелая мРНК |
|
|
|
|
|
|
Эндо- |
|
|
|
|
|
|
нуклеаза |
|
|
|
АААА |
Деградация |
|
|
|
|
|
||
|
Экзо- |
|
|
|
|
мРНК |
Активность |
нуклеаза |
|
|
|
|
|
|
|
|
|
|
|
|
по поиску гомологии |
|
|
|
|
251 |
|
|
|
|
|
|
|
|

Copyright ОАО «ЦКБ «БИБКОМ» & ООО «Aгентство Kнига-Cервис»
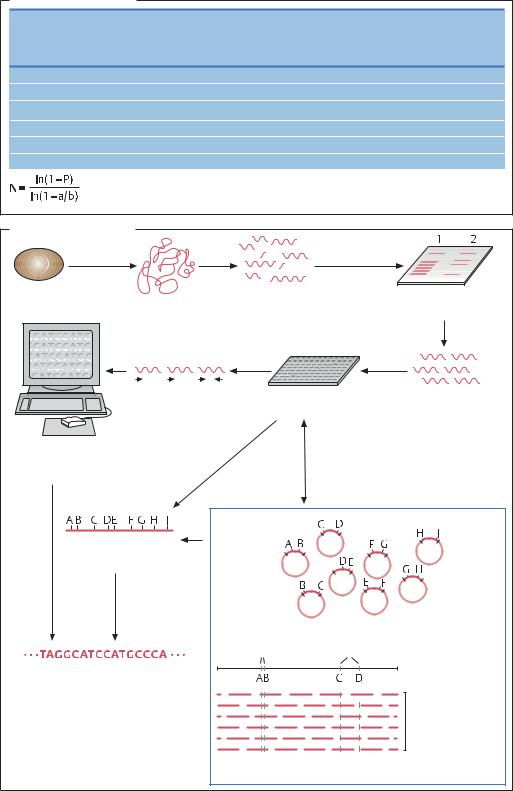
Геномные библиотеки |
|
|
|
|
|
|
|
|
|
|
Число исследованных клонов (Р = 95%) |
|
|
||||
|
Гаплоидный |
λ-Вектор |
|
Космиды |
BAC |
|
YAC |
|
|
геном b |
(EMBL4) |
|
a = 35 т.п.н. |
a = 250 т.п.н. |
a = 1000 т.п.н. |
||
|
|
a = 17 т.п.н. |
|
|
|
|
|
|
E. coli |
4 800 000 |
850 |
|
|
410 |
56 |
|
13 |
S. cerevisiae |
14 000 000 |
2 500 |
|
|
1 200 |
167 |
|
41 |
Drosophila melanogaster |
170 000 000 |
30 000 |
|
|
14 500 |
2 036 |
|
508 |
Томат |
700 000 000 |
123 500 |
|
|
59 000 |
8 387 |
|
2 096 |
Человек |
3 000 000 000 |
529 000 |
|
|
257 000 |
35 948 |
|
8 986 |
Лягушка |
23 000 000 000 |
4 053 000 |
|
1 969 000 |
275 602 |
|
68 901 |
|
|
N = число исследованных клонов |
|
|
a = средняя длина ДНК-фрагментов, |
||||
|
Р = вероятность |
|
|
|
встроенных в вектор, п.н. |
|||
|
|
|
|
|
b = полный размер генома, п.н. |
|||
Картирование генома |
|
Обработка |
|
|
|
|
|
|
|
|
|
|
Электрофорез |
|
|
||
Выделение ДНК |
ультра- |
|
|
|
|
|||
звуком |
|
|
в агарозном геле |
|
|
|||
Клетки |
|
Фрагменты ДНК |
1: Фрагментированная ДНК |
|||||
|
|
|||||||
|
|
|
|
|
|
2: ДНК-маркер |
||
|
Секвенирование |
Создание |
|
Выделение из геля |
||||
|
концевых участков ДНК |
библиотеки |
|
фрагментов ДНК |
||||
|
|
|
клонов |
|
размером |
|||
|
|
|
|
|
|
|
1,6–2,0 т.п.н. |
|
Создание контигов |
|
|
|
|
Использование |
|
|
|
(наборов клонированных |
|
|
|
|
|
|
||
фрагментов, непрерывно |
|
|
|
|
библиотеки клонов |
|
|
|
перекрывающих часть генома) |
|
|
|
для картирования |
|
|
||
|
|
|
|
|
генома |
|
|
|
Создание STS-карты |
|
|
|
|
|
|
|
|
|
|
Близко- |
|
Удаленные |
|
|
||
|
|
расположенные |
друг от друга |
|
|
|||
|
|
маркеры |
|
маркеры |
Полная ДНК |
|||
|
|
|
|
|
|
|
||
Полная последовательность ДНК |
|
|
|
|
|
или ее крупный |
||
|
|
|
|
|
|
|
фрагмент |
|
|
|
|
|
|
|
|
Коллекция |
|
|
|
|
|
|
|
|
мелких |
|
|
|
|
|
|
|
|
фрагментов |
|
|
|
6 общих |
|
2 общих |
|
|
||
|
|
фрагментов |
|
фрагмента |
|
|
||
|
|
|
|
|
|
|
|
253 |