Материал: Шмид Р. Наглядная биотехнология и генетическая инженерия
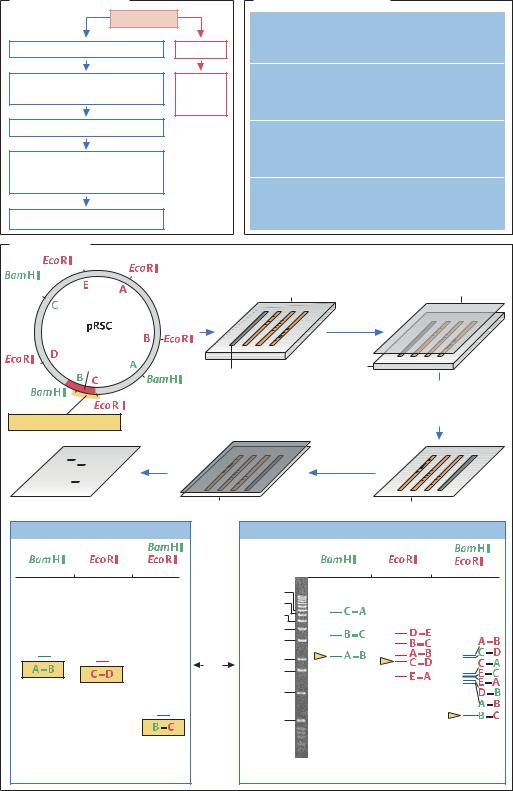
Клонирование генов |
|
|
|
|
Методы идентификации |
|
|
|||
|
a |
Проба ДНК |
б |
|
Саузерн-блот |
Поиск ДНК |
|
Гибридизация |
||
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
с меченым ДНК- |
Получение библиотеки генов |
|
ПЦР |
|
|
|
|
|
или РНК-зондом |
||
|
|
|
|
|
|
|
||||
Гибридизация для поиска |
|
Секвени- |
|
Нозерн-блот |
Поиск мРНК |
|
Гибридизация |
|||
|
нужного клона |
|
|
рование |
|
|
|
|
|
с меченым ДНК- |
|
|
|
|
гена |
|
|
|
|
|
или РНК-зондом |
|
|
|
|
|
|
|
|
|
|
|
|
Очистка ДНК |
|
|
|
|
Вестерн-блот |
Поиск белка |
|
Иммуноанализ |
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
с мечеными |
|
Получение |
|
|
|
|
|
|
|
|
антителами |
|
|
|
|
|
|
|
|
|
|
|
коротких фрагментов гена |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
Использование |
Поиск |
|
Экспрессия |
|
|
|
|
|
|
|
репортерных |
регуляторных |
|
репортерных |
|
Секвенирование гена |
|
|
|
групп |
элементов |
|
белков |
|||
Саузерн-блот |
|
|
|
|
|
|
|
|
|
|
|
11 540 п.н. |
997 п.н. |
Расщепление рестриктазами |
|
|
|||||
|
|
|
|
Нейлоновая |
||||||
10 068 п.н. |
|
|
|
BamHI и EcoRI, электрофорез |
|
|||||
|
|
|
в агарозном геле |
|
|
мембрана |
||||
|
|
|
|
|
|
|
|
Перенос |
|
|
|
12 002 п.н. |
|
|
|
|
|
|
|
|
|
|
|
|
3 188 п.н. |
|
|
|
|
|
|
|
7 959 п.н. |
Ген |
|
|
|
|
|
Агарозный гель |
|
|
|
|
|
|
Маркерная ДНК |
|
|
|
||||
|
|
4 467 п.н. |
|
|
|
|
Гибридизация |
|||
|
|
|
|
|
со специфическим зондом |
|||||
6 621 п.н. |
6 022 п.н. |
|
|
|
|
|||||
|
|
|
|
|
(содержащим |
|||||
Специфический зонд |
|
|
|
|
|
|
радиоактивную метку) |
|||
|
|
|
|
Радиоавтография |
|
|
|
|||
|
|
|
|
|
|
|
|
|
||
|
|
|
Рентгеновская |
|
|
|
|
|
|
|
|
|
|
пленка |
|
|
|
|
|
|
|
Проявленная пленка |
|
|
Нейлоновая мембрана |
Нейлоновая мембрана |
||||||
|
Рентгеновская пленка |
|
|
|
|
|
Агарозный гель |
|
||
|
|
|
|
|
|
|
Маркерная |
|
|
|
|
|
|
|
|
|
|
ДНК |
|
|
|
|
|
|
|
|
|
|
7 |
|
|
|
|
|
|
|
|
|
|
6 |
|
|
|
|
|
|
|
|
|
|
5 |
|
|
|
|
|
|
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
Срав- |
н. |
2 |
|
|
|
|
|
|
|
|
не- |
|
т. п. |
|
|
|
|
|
|
|
|
|
1,6 |
|
|
|
||
|
|
|
|
ние |
|
|
|
|
||
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
500 |
|
|
|
|
Следы |
|
|
|
|
|
|
|
Следы |
|
1 |
2 |
|
3 |
|
|
|
Маркер |
1 |
2 |
3 |
245
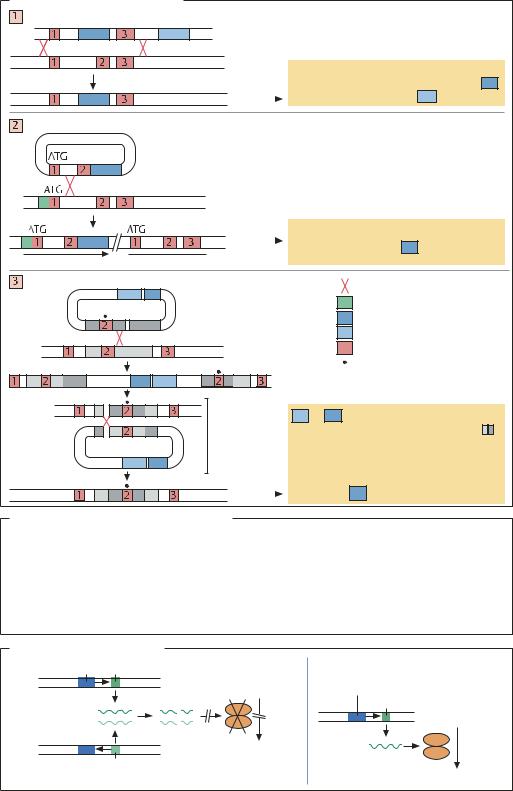
Выключение генов (knock-out) |
|
|
|
|
|||
Позитивно-негативная селекция |
|
|
|
|
|||
m1 |
|
|
m2 |
Вектор |
|
|
|
|
|
|
|
ДНК–мишень |
|
|
|
|
|
|
|
|
Экзон 2 выключен. |
|
|
|
Обмен |
|
|
|
Трансформанты содержат ген для маркера m1 , |
||
m1 |
|
|
|
Результат |
но не несут ген для маркера m2 |
|
|
Инактивация в результате встраивания (инсерция) |
|
|
|
||||
|
|
Вектор |
|
|
|
|
|
|
m1 |
|
|
|
|
|
|
|
|
|
|
ДНК–мишень |
|
|
|
m1 |
|
|
|
Результат |
Экзон 3 выключен. |
|
|
|
|
|
Происходит экспрессия m1 |
|
|||
|
|
|
|
|
|
||
Активный ген |
Неактивный (молчащий) ген |
|
|
|
|||
Встраивание и выщепление |
|
|
|
Рекомбинация |
|
||
|
m2 |
m1 |
|
|
|
||
|
|
|
Промотор |
|
|||
|
|
|
Вектор |
|
|
||
|
|
|
m1 |
Позитивный селективный маркер |
|||
|
|
|
|
|
|||
|
|
|
|
|
m2 |
Негативный селективный маркер |
|
|
|
|
|
ДНК–мишень |
Экзоны |
|
|
|
|
|
|
Точка маркирования |
|
||
|
|
|
|
|
Промежуточная |
|
|
|
m1 |
m2 |
|
|
|
||
|
|
конструкция |
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
Внутри- |
m2 и m1 расположены вне области |
|
|
|
|
|
|
рекомбинации (отмеченной серым цветом |
). |
||
|
|
|
|
хромосомная |
|||
|
|
|
|
В результате инсерции область рекомбинации |
|||
|
|
|
|
рекомбинация |
|||
|
|
|
|
оказывается удвоенной, и в ходе внутри- |
|
||
|
m2 |
m1 |
|
|
|||
|
|
хромосомной рекомбинации происходит |
|
||||
|
|
|
|
|
|
||
|
|
|
|
|
потеря функционального экзона 2. |
|
|
|
|
|
|
Результат |
Экспрессии |
m1 не происходит. |
|
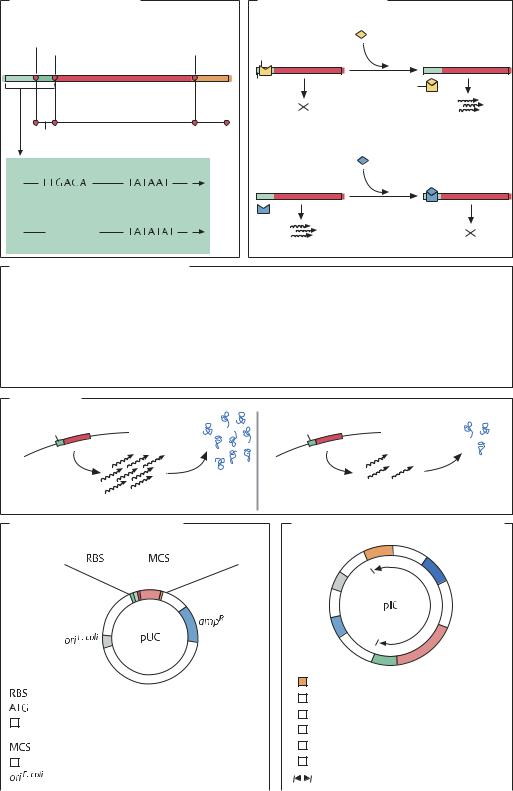
Эукариотические селективные маркеры |
|
|
|
||||
Маркер |
Тип клеток |
Индикатор |
Рецессивный: аденозиндезаминаза |
Мутантные линии клеток СНО |
9-β-Ксилофураноксил |
Доминантный: дигидрофолатредуктаза |
Любые |
Метотрексат |
Слитый белок: |
|
|
неомицинфосфотрансфераза и тимидинкиназа |
Любые |
Неомицина сульфат |
Металлотионеин I |
Любые |
Cd2+, Zn2+ |
Метод антисмысловой РНК |
|
|
|
|
|
Промотор |
Ген–мишень |
|
Дикий тип (для сравнения) |
|
|
Фермент– |
|
|
|
||
|
|
Промотор |
|
|
|
|
Деградация |
мишень |
|
|
|
мРНК мишени |
Субстрат |
ДНК |
Ген–мишень |
|
|
|
Фермент– |
|
|||
Антисмысловая РНК |
|
|
|
|
|
|
Продукт |
|
мишень |
Субстрат |
|
|
|
|
|
||
|
|
|
мРНК |
|
|
|
|
|
|
|
|
|
|
|
мишени |
|
Продукт |
Синтетическая последовательность |
|
|
|
||
|
|
|
|
||
«антисмыслового» гена |
|
|
|
249 |
|
|
|
|
|
|
|