Материал: Шмид Р. Наглядная биотехнология и генетическая инженерия
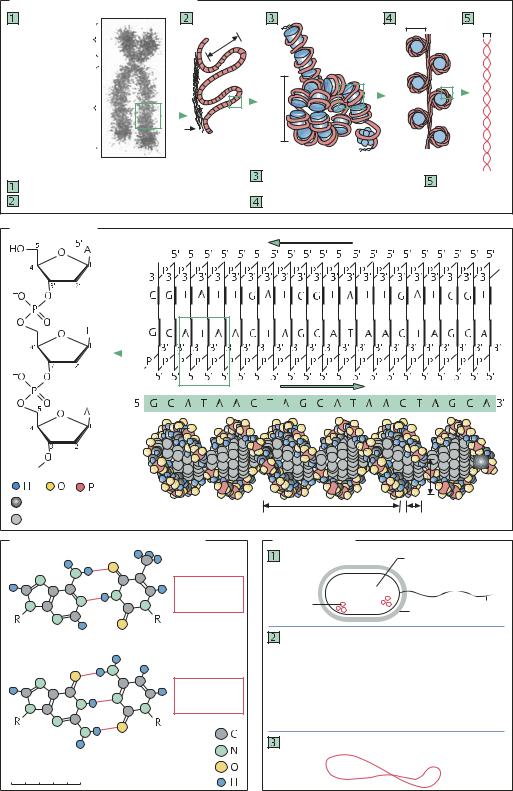
От хромосомы к двойной спирали |
|
|
|
250 нм |
10 нм |
2 нм |
|
Короткое плечо (p) |
|
|
|
Центромера |
|
|
|
Длинное плечо (q) |
нм |
|
|
30 |
|
||
|
|
||
Гистон |
|
|
|
|
Хроматиновая фибрилла, |
Двойная |
|
Целая метафазная хромосома |
содержащая 1200 п.н. |
||
спираль ДНК – |
|||
|
|
||
Петли хроматина – около 100 000 п.н. на петлю |
«Бусины» нуклеосом – по 80 п.н. |
10 п.н. в 3,4 нм |
|
Структура ДНК |
|
|
С в сахарофосфатном остове |
|
1 нм |
|
|
С или N в азотистых основаниях |
3,4 нм |
0,34 нм |
|
|
|
|
|||
Комплементарные пары оснований |
ДНК бактерий |
|
|
|
в ДНК |
|
Бактериальная клетка |
Нуклеоид, содержащий |
|
|
|
|||
|
|
|
суперскрученную |
|
|
Пара АТ – два |
Плазмид- |
молекулу ДНК |
|
|
водородных |
|
|
|
|
мостика |
ная ДНК |
Клеточная |
Жгутик |
|
|
|
стенка |
|
Аденин (А) |
Тимин (Т) |
Раскручивание витков спирали в результате |
||
|
|
разрывов, образованных ферментом ДНКазой I |
||
|
Пара GС – три |
|
|
|
|
водородных |
|
|
|
|
мостика |
|
|
|
|
|
Открытая кольцевая форма молекулы ДНК |
|
|
Гуанин (G) |
Цитозин (С) |
|
|
|
0 |
0,5 нм |
|
|
225 |
|
|
|
|
|

Функции ДНК |
|
|
|
|
ДНК |
Транскрипция |
Трансляция** |
Белок |
Рибосомы на мРНК |
Обратная |
мРНК |
|
||
|
|
|
|
|
|
транскрипция* |
|
|
|
Репли- |
|
|
|
|
кация |
|
|
|
|
|
|
|
ДНК |
РНК-полимераза |
ДНК |
Наследование |
|
0,5 мкм |
|
|
|
|||
* только у ретровирусов |
|
Транскрипция бактериальной ДНК |
||
** на рибосомах |
|
|
|
|
Генетический код |
|
|
|
|
Аминокислота |
Кодон |
Аминокислота |
Кодон |
Аминокислота |
Кодон |
Аминокислота |
Кодон |
|
Фенилаланин (F) |
UUU |
Серин (S) |
UCU |
Тирозин (Y) |
UAU |
Цистеин (C) |
UGU |
|
|
|
UUC |
|
UCC |
|
UAC |
|
UGC |
Лейцин (L) |
UUA |
|
UCA |
Стоп-кодон |
UAA |
Стоп-кодон |
UGA |
|
|
|
UUG |
|
UCG |
Стоп-кодон |
UAG |
Триптофан (W) |
UGG |
|
|
|
|
|
|
|
|
|
Лейцин (L) |
CUU |
Пролин (P) |
CCU |
Гистидин (H) |
CAU |
Аргинин (R) |
CGU |
|
|
|
CUC |
|
CCC |
|
CAC |
|
CGC |
|
|
CUA |
|
CCA |
Глутамин (Q) |
CAA |
|
CGA |
|
|
CUG |
|
CCG |
|
CAG |
|
CGG |
|
|
|
|
|
|
|
|
|
|
Изолейцин (I) |
AUU |
Треонин (T) |
ACU |
Аспарагин (N) |
AAU |
Серин (S) |
AGU |
|
|
AUC |
|
ACC |
|
AAC |
|
AGC |
|
|
AUA |
|
ACA |
Лизин (K) |
AAA |
Аргинин (R) |
AGA |
Метионин (M) |
AUG |
|
ACG |
|
AAG |
|
AGG |
|
|
|
|
|
|
|
|
|
|
|
Валин (V) |
GUU |
Аланин (A) |
GCU |
Аспарагиновая кислота (D) GAU |
Глицин (G) |
GGU |
|
|
|
GUC |
|
GCC |
|
GAC |
|
GGC |
|
|
GUA |
|
GCA |
Глутаминовая кислота (E) GAA |
|
GGA |
|
|
|
GUG |
|
GCG |
|
GAG |
|
GGG |
|
|
|
|
|
|
|
|
|
Создание праймеров |
|
Частота использования |
|
|||
|
|
кодонов некоторых |
|
|||
|
Выделенный белок |
аминокислот у различных |
||||
|
|
организмов |
|
|
|
|
|
Определение аминокислотной |
Амино- |
Кодон |
Вероятность |
||
|
последовательности белка |
|||||
|
кислота |
|
использования |
|||
|
или его участка |
|
||||
|
|
|
|
кодона, % |
||
|
Информация |
Glu, E |
GAG |
0,30 |
0,31 |
0,59 |
|
|
GAA |
0,70 |
0,69 |
0,41 |
|
|
о последовательности белка |
|
||||
|
|
Lys, K |
AAG |
0,24 |
0,43 |
0,60 |
|
|
|
AAA |
0,76 |
0,57 |
0,40 |
Синтез набора |
Набор всех возможных |
Pro, P |
CCG |
0,55 |
0,12 |
0,11 |
«вырожденных» |
последовательностей ДНК, |
|
CCA |
0,20 |
0,42 |
0,27 |
праймеров |
кодирующих изучаемый |
|
||||
Гибридизация |
полипептид |
|
CCU |
0,16 |
0,31 |
0,29 |
с банком ДНК |
N = любое основание |
|
||||
или кДНК |
|
CCC |
0,10 |
0,15 |
0,33 |
|
|
|
|
||||
|
Определение истинной |
|
|
|
|
|
|
последовательности кДНК |
E. coli |
|
|
|
|
|
|
|
|
|
|
|
|
|
S. cerevisiae |
|
|
|
|
|
|
Человек |
|
|
|
|
227
инженерии |
Эксперимент в генетической инженерии |
||
ВВЕДЕНИЕ. В генно-инженерных исследованиях при- |
меняют обратные транскриптазы с различными свой- |
||
|
|||
|
меняются очень многие методы. К наиболее часто |
ствами. Чаще всего используют ДНК-полимеразу, |
|
генетической |
используемым относятся следующие: 1) выделение |
выделенную из Thermus aquaticus. Этот фермент, ус- |
|
ДНК, ее амплификация, различные модификации с |
тойчивый при высокой температуре, в присутствии |
||
|
|||
|
помощью ферментов, установление нуклеотидной |
Mn2+ действует как обратная транскриптаза, достра- |
|
|
последовательности ДНК, осуществление химиче- |
ивая цепь ДНК на РНК-матрице. После завершения |
|
|
ского синтеза ДНК определенной последовательно- |
реакции полученный гибридный дуплекс мРНК–ДНК |
|
|
сти; 2) клонирование и экспрессия генов в эукариоти- |
обрабатывают ферментом РНКазой и получают одно- |
|
|
ческих и прокариотических клетках. |
цепочечную ДНК, которую можно использовать в ка- |
|
Методы |
ВЫДЕЛЕНИЕ ДНК, ЕЕ АМПЛИФИКАЦИЯ И ОБРАБОТКА |
честве матрицы для создания двухцепочечной ДНК в |
|
МОДИФИЦИРУЮЩИМИ ФЕРМЕНТАМИ. Количество |
обычной ПЦР. Для неспецифической амплификации |
||
|
|||
|
ДНК в клетке очень мало’ (одна молекула ДНК на |
эукариотических мРНК используют участок полиаде- |
|
|
прокариотическую клетку и один или два набора хро- |
нилирования на 5'-конце мРНК: в качестве затравки |
|
|
мосом на эукариотическую клетку), тем не менее |
для синтеза кДНК на матрице мРНК служит олиго- |
|
|
ДНК из клеток можно выделить химическими мето- |
мер, состоящий из тимидиновых оснований (polyT). |
|
|
дами, выполнить ее анализа и использовать в даль- |
ЭКСПРЕССИЯ. К настоящему времени разработано |
|
|
нейших исследованиях. Как правило, для работы не |
несколько методов встраивания ДНК в ДНК другого |
|
|
применяют длинные цепи ДНК, а обрабатывают ее |
хозяина. После репликации в процессе клеточного |
|
|
специальными ферментами, которые могут расщеп- |
деления происходит транскрипция ДНК, а затем в ре- |
|
|
лять ДНК по определенным сайтам, осуществлять ее |
зультате трансляции образуются белки, среди кото- |
|
|
модификации, соединять фрагменты ДНК, а также |
рых и белок, закодированный в клонированном фраг- |
|
|
переводить ДНК в мРНК. Большинство эксперимен- |
менте ДНК. Совокупность этих процессов называется |
|
|
тов требует достаточно больших количеств ДНК: с |
экспрессией клонированного гена. В качестве кле- |
|
|
помощью автоматических синтезаторов можно полу- |
ток-хозяев, как правило, используют бактериальные |
|
|
чить лишь небольшие фрагменты ДНК, размером до |
клетки. Такой выбор обусловлен следующими |
|
|
100 п.н., поэтому особое значение приобретает ме- |
особенностями бактерий: 1) их геном представлен |
|
|
тод ПЦР, позволяющий амплифицировать фрагмен- |
всего лишь одной двухцепочечной молекулой ДНК; |
|
|
ты ДНК размером в тысячи пар нуклеотидов. Важное |
2) для переноса генетического материала можно |
|
|
применение метода ПЦР – рекомбинация между |
использовать фаги или плазмиды; 3) молекулярно- |
|
|
фрагментами ДНК из различных источников, напри- |
генетические основы организации многих бактерий |
|
|
мер между ДНК, выделенной из живого организма, и |
достаточно хорошо изучены; 4) бактерии быстро раз- |
|
|
химически синтезированной ДНК. |
множаются, и в биореакторах можно выращивать |
|
|
СВОЙСТВА ДНК И СЕКВЕНИРОВАНИЕ. Основные |
очень большие количества бактериальных клеток. |
|
|
характеристики ДНК: 1) температура плавления (ДНК |
Наряду с Escherichia coli для клонирования и экспрес- |
|
|
с бо’ льшим содержанием пар GC денатурирует при бо- |
сии чужеродной ДНК используют и другие бактерии, |
|
|
лее высокой температуре по сравнению с ДНК, обога- |
например Bacillus, Lactobacillus, Pseudomonas и |
|
|
щенной парами АТ); 2) молекулярная масса (этот па- |
Streptomyces. В последнее время разработаны мето- |
|
|
раметр устанавливают путем электрофоретического |
ды введения ДНК и в эукариотические организмы, |
|
|
разделения фрагментов ДНК в присутствии фрагмен- |
такие как дрожжи, грибы, а также в клетки растений |
|
|
тов ДНК известного размера); 3) последовательность |
и животных. |
|
|
нуклеотидов, которую устанавливают путем секвени- |
|
|
|
рования ДНК; 4) белковый продукт или функциональ- |
|
|
|
ный элемент, закодированный в исследуемой ДНК; |
|
|
|
5) взаиморасположение сайтов расщепления эндону- |
|
|
|
клеазами рестрикции (карта рестрикции). |
|
|
|
КЛОНИРОВАНИЕ. Методы, позволяющие выделить из |
|
|
|
генома прокариот участок, кодирующий определен- |
|
|
|
ный белок, также применимы и для эукариот, однако |
|
|
|
в этом случае необходимо учитывать наличие интро- |
|
|
|
нов в большинстве эукариотических ДНК. Зрелую |
|
|
|
(после сплайсинга) мРНК выделяют из клетки, а за- |
|
|
|
тем с помощью фермента обратной транскриптазы |
|
|
228 |
(ОТ) в реакции ОT-ПЦР синтезируют комплементар- |
|
|
ную цепь ДНК (кДНК). В лабораторной практике при- |
|
||
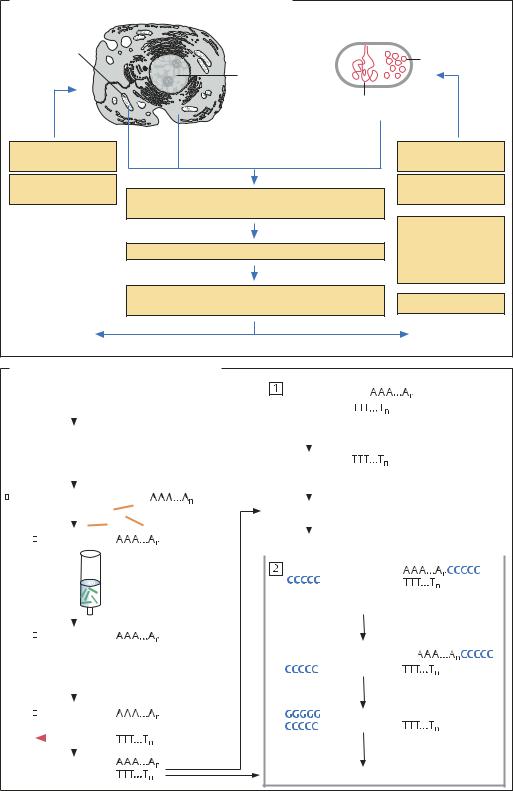
Основные стадии генно-инженерного эксперимента |
|
|
||
Эукариотическая клетка |
Прокариотическая клетка |
|||
Митохонд- |
|
|
|
|
риальная |
|
|
|
Плазмидная ДНК |
ДНК |
|
|
|
|
|
|
|
|
|
|
|
ДНК |
|
|
|
|
|
Нуклеоид, содержащий |
|
|
|
|
геномную ДНК |
|
|
Выде- |
Выделение мРНК |
Выде- |
|
Картирование генома |
ление |
и получение |
ление |
Картирование генома |
и секвенирование |
ДНК |
ее кДНК-копии |
ДНК |
и секвенирование |
Выключение |
|
|
|
Выключение |
определенных генов |
Обработка ДНК ферментами рестрикции |
|
определенных генов |
|
|
|
|
||
|
и/или амплификация фрагментов генома методом ПЦР |
|
||
|
|
|
|
Химический синтез |
|
Встраивание кДНК или фрагмента гена в векторную ДНК |
фрагментов ДНК |
||
|
и мечение праймеров |
|||
|
|
|
|
или ДНК-зондов |
|
Трансформация клеток-хозяев полученной векторной |
Секвенирование ДНК |
||
|
конструкцией, оптимизация условий экспрессии гена |
|||
Эукариотические |
|
|
|
Прокариотические |
клетки |
Трансформированные клетки синтезируют необходимый продукт |
клетки |
||
|
|
|||
Клонирование эукариотических генов |
|
|
||
|
Интрон |
|
Экзон |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Расщепление цепи |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Эукариотическая ДНК |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
РНК с помощью |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
Транскрипция |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
РНКазы H |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Синтез комплементарной |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Первичный РНК-продукт |
|
|
|
|
|
цепи ДНК с помощью |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ДНК-полимеразы |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
Кэпирование |
(содержащий интроны) |
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
и полиадени- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
лирование |
|
|
|
|
|
|
Обработка S1-нуклеазой |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
для получения фрагмента |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ДНК с «тупыми» концами |
||||||||||||
|
|
|
|
|
|
|
|
|
|
Сплайсинг |
Зрелый |
|
|
|
|
|
|
|
|
|
|
|
Двухцепочечная кДНК |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Встраивание в вектор/трансформация клеток E. coli |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
мРНК-продукт |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(не содержащий |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Элюиро- |
|
|
|
Олиго-dТ |
интронов) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
Обработка терминальной трансферазой для создания |
||||||||||||||||||||||||||
|
|
|
|
вание |
|
|
|
целлюлоза |
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
последовательности олиго-dС на концах |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Расщепление цепи РНК |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Очищенный |
|
|
|
|
|
|
|
|
|
|
|
|
|
с помощью РНКазы Н |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
препарат |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Синтез цепи, |
зрелой мРНК |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
комплементарной |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
мРНК, с помощью |
|
|
|
|
|
|
|
|
|
|
|
|
|
Синтез комплементарной |
||||||||||
|
|
|
|
|
|
|
|
|
|
обратной транскриптазы |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
цепи ДНК с помощью |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
фрагмента Клёнова |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Зрелая мРНК |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Праймер |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Обработка S1-нуклеазой |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
для получения фрагмента |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ДНК с «тупыми» концами |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Встраивание в вектор/трансформация клеток E. coli |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
229