Материал: Шмид Р. Наглядная биотехнология и генетическая инженерия
микробиологии |
Усовершенствование штаммов микроорганизмов |
||
ВВЕДЕНИЕ. Микроорганизмы, выделенные из при- |
антибиотика и с антибиотиком (например, с пеницил- |
||
|
|||
|
родной среды обитания, редко полностью отвечают |
лином). Основными преимуществами такого метода |
|
|
требованиям биотехнологического производства. По- |
является возможность проводить одновременный |
|
|
этому необходимым подготовительным этапом явля- |
анализ большого количества полученных мутантов |
|
Основы |
ется многократное повторение мутагенеза и последу- |
(несколько сотен на одной чашке). В результате дей- |
|
ющего отбора мутантов, обладающих искомыми |
ствия сильных мутагенных факторов часто происхо- |
||
свойствами. Наиболее часто задачей таких экспери- |
дят изменения в нескольких генах, поэтому необхо- |
||
ментов является получение штаммов, продуцирую- |
димо проверить не только способность мутантов |
||
щих больше целевого вещества и меньше побочных |
образовывать необходимый продукт, но и сохран- |
||
|
продуктов или обладающих лучшими технологиче- |
ность свойств, характерных для дикого штамма. Для |
|
|
скими характеристиками (сокращение времени фер- |
этого отобранные клетки выращивают в качалочных |
|
|
ментации, отсутствие нежелательной пигментации, |
колбах в условиях, максимально приближенных к та- |
|
|
устойчивость к бактериофагам и др.). Одним из пре- |
ковым в производственном процессе, и отбирают |
|
|
имуществ микроорганизмов является их короткий |
клетки, обладающие улучшенными свойствами. Пов- |
|
|
жизненный цикл (часто менее 1 ч). Это позволяет |
торение нескольких раундов мутагенеза с последую- |
|
|
достаточно быстро получать и анализировать боль- |
щим отбором позволяет отобрать штаммы, которые |
|
|
шое количество мутантов. При работе с эукариотиче- |
наилучшим образом удовлетворяют всем требовани- |
|
|
скими микроорганизмами (например, грибами) |
ям технологического процесса. Для устранения не- |
|
|
необходимо принимать во внимание процесс реком- |
нужных приобретенных свойств полученные штаммы |
|
|
бинации. Знание обмена веществ, его регуляции и |
скрещивают с дикими штаммами. |
|
|
структуры ДНК, кодирующей ферменты, позволяет |
СЕЛЕКЦИЯ В НЕПРЕРЫВНОЙ КУЛЬТУРЕ. Отбор мутан- |
|
|
модифицировать геном микроорганизмов, целена- |
тов можно проводить в непрерывной культуре в фер- |
|
|
правленно «выключая» или «активируя» те или иные |
ментере: для этого клетки микроорганизмов выращи- |
|
|
стадии обмена веществ (metabolic engineering). |
вают в среде с мутагеном и осуществляют при этом |
|
|
МУТАГЕНЕЗ. Вероятность спонтанной мутации в нор- |
селективное воздействие, например постепенно за- |
|
|
мальном гене (под действием естественных мутаге- |
меняют один источник углерода на другой. В таких |
|
|
нов или при репликации) составляет 10–6–10–7. Как |
условиях выживают лишь те микроорганизмы, кото- |
|
|
правило, такие мутации остаются «молчащими» из-за |
рые в результате мутагенеза приобрели способность |
|
|
генетической или функциональной супрессии или ста- |
утилизировать новый источник углерода. Описанный |
|
|
новятся мишенью системы репарации ДНК. Для усо- |
способ, однако, не позволяет проводить отбор мутан- |
|
|
вершенствования штаммов осуществляют более эф- |
тов с повышенным выходом продукта. |
|
|
фективный искусственный мутагенез: например, при |
|
|
|
ультрафиолетовом облучении или при введении мута- |
|
|
|
генных веществ. Путем изменения длительности му- |
|
|
|
тагенного воздействия и путем подбора мутагенных |
|
|
|
веществ удается варьировать частоту мутаций в клет- |
|
|
|
ках. В результате действия мутагенных факторов, как |
|
|
|
правило, 90–99% клеток погибают, а затем из остав- |
|
|
|
шихся клеток отбирают мутантов, которые обладают |
|
|
|
желаемыми фенотипическими признаками. |
|
|
|
ОТБОР МУТАНТОВ В ПОВЕРХНОСТНЫХ КУЛЬТУРАХ. |
|
|
|
Основным фенотипическим признаком, рассматри- |
|
|
|
ваемым при усовершенствовании штаммов микроор- |
|
|
|
ганизмов, является их способность образовывать |
|
|
|
большое количество продукта. Для отбора мутантов, |
|
|
|
удовлетворяющих этому требованию, разрабатывают |
|
|
|
систему отбора. В качестве признака для отбора мо- |
|
|
|
жет служить устойчивость к антибиотику, ядовитым |
|
|
|
веществам или фаговой инфекции. Полученные пос- |
|
|
|
ле проведения мутагенеза клетки высевают в чашки |
|
|
|
Петри на твердые селективные среды, где вырастают |
|
|
|
лишь те колонии, которые обладают необходимой ус- |
|
|
200 |
тойчивостью. Для отбора ауксотрофных мутантов ре- |
|
|
плики колоний помещают на питательную среду без |
|
||
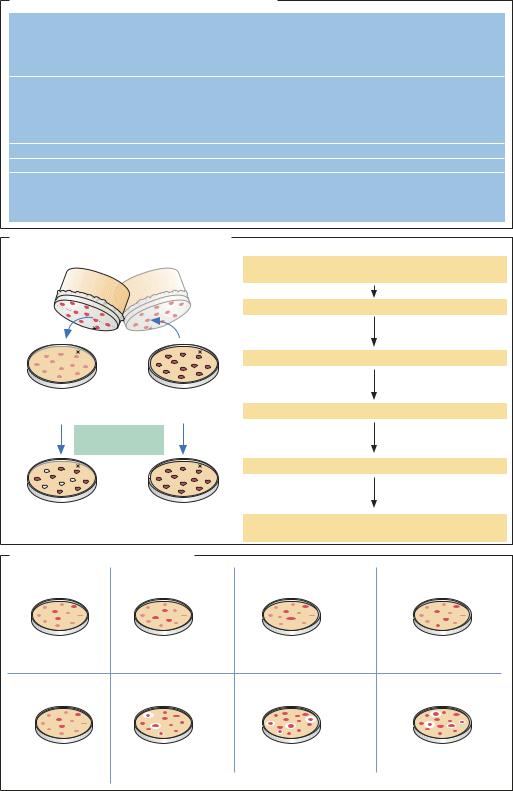
Усовершенствование штаммов микроорганизмов
Мутагенез |
Механизм |
Тип изменений |
|
|
|
Физический метод |
|
|
Ионизирующее (рентге- |
Образование одноили двухцепочечных |
Устойчивые генетические изменения |
новское) облучение |
разрывов в ДНК |
|
Ультрафиолетовое |
Образование димеров тимидина и цитозина Точечные мутации |
|
облучение (~254 нм) |
|
|
Химический метод |
|
|
Нитрит |
При дезаминировании аденина образуется |
Точечные мутации |
|
гипоксантин, а цитозина – урацил |
|
Алкилирующие агенты |
Алкилированные пурины |
Точечные мутации |
Аналоги оснований |
Включаются в ДНК при репликации |
Устойчивые генетические изменения |
Акридиновый оранжевый |
Интеркалирует в ДНК |
Устойчивые генетические изменения |
|
|
|
Биологический метод |
|
|
Транспозоны |
Переносят участки ДНК внутри хромосомы |
Маркирование генов |
||
Метод реплик и пенициллиновый метод |
Пенициллиновый метод |
|||
Получение реплики |
||||
Клеточная суспензия бактерий, чувствительных |
||||
Штемпель со |
|
|||
|
к действию ампициллина |
|||
стерильной |
|
|
Мутагенез |
|
бархоткой |
|
|
||
|
Смесь мутантных и диких клеток |
|||
|
|
|||
|
|
|
Выращивание в полной |
|
|
|
|
питательной среде |
|
|
|
Мутанты и клетки дикого типа |
||
|
|
|
Выращивание |
|
|
|
|
на минимальной среде |
|
Полная |
Полная |
|
с ампициллином |
|
питательная среда |
питательная |
Клетки дикого типа погибают под действием ампициллина |
||
с антибиотиком |
среда |
|||
|
Ампициллин удаляют из |
|||
Инкубация |
|
|||
|
среды, выращивание на |
|||
в термостате |
|
|||
|
полной питательной среде |
|||
|
|
|
||
|
|
Вырастают только мутанты |
||
|
|
|
Получение реплик |
|
|
|
|
и посев на минимальную |
|
Штаммы, устойчивые |
Контрольная чашка |
|
и полную среды |
|
Ауксотрофные мутанты вырастают только |
||||
к антибиотику |
с полной питательной |
|||
|
средой |
на полной питательной среде |
||
Селективные питательные среды |
|
|
||
Выращивание при |
Минимальная |
Питательная среда |
Питательная среда |
неоптимальной |
питательная среда |
с индикатором на метаболит |
с антиметаболитом |
температуре |
с метаболитами |
|
|
«Температурные» |
Ауксотрофные мутанты – «Катаболические» мутанты – Регуляторные мутанты – |
|
||
мутанты |
дефект в биосинтезе |
дефект фермента, разлагаю- |
измененная скорость синтеза |
|
|
некоторого компонента* |
щего определенный субстрат |
фермента или продукта |
|
Питательная среда, тес- |
Питательная среда и тес- |
Питательная среда и казеин |
Питательная среда |
|
товые штаммы патоген- |
товые штаммы патоген- |
|
и трибутирин |
|
ных микроорганизмов |
ных микроорганизмов |
|
|
|
и β-лак- |
|
|
|
|
тамаза |
|
|
|
|
«Лактамазная» устой- |
Повышенный выход |
Повышенный выход |
Повышенный выход липаз |
|
чивость: устойчивые |
антибиотика |
протеиназ |
|
|
к лактамазе продуцен- |
|
|
|
|
ты антибиотиков |
* Выводы делают после получения реплик и применения пенициллинового метода |
201 |
||
|
|
|
|
|
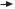






 температуры
температуры 
 нагревания или охлаждения реактора
нагревания или охлаждения реактора Отвод воды для нагревания или охлаждения реактора
Отвод воды для нагревания или охлаждения реактора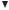 воздух
воздух