Материал: Шмид Р. Наглядная биотехнология и генетическая инженерия
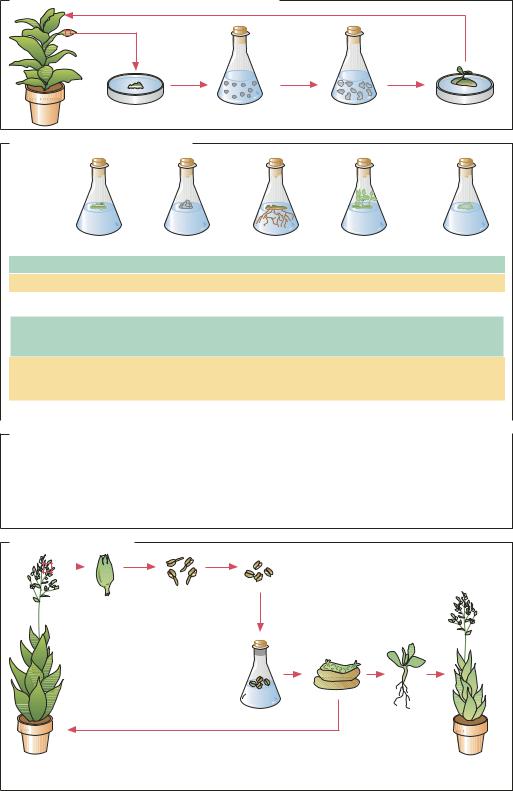
Получение и регенерация меристемной культуры |
|
|
|
Эксплант |
Отдельные клетки |
Клеточная культура |
Регенерация |
Влияние растительных гормонов |
|
|
|
Питательный 


 агар
агар 

|
|
Эксплант |
Каллус |
Корни |
Побеги |
Нет роста |
|
|||
|
Ауксин |
– |
3,00 мг/л |
3,00 мг/л |
0,03 мг/л |
– |
|
|||
|
Цитокинин |
– |
0,2 мг/л |
0,02 мг/л |
1,00 мг/л |
0,2 мг/л |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
Составу |
|
|
|
Функция* |
|
|
|
|
|
Ауксин |
3-Индолилуксусная кислота, |
Индуцирует рост в длину, в больших |
|
||||||
|
|
(2,4-дихлорфенокси)уксусная кислота |
концентрациях ингибирует образование |
|
||||||
|
|
(синтетический ауксин) и другие |
корней и деление клеток |
|
|
|||||
|
Цитокинины |
Кинетин, 6-бензаминопурин |
Стимулирует образование каллуса |
|
|
|||||
|
|
Абсцизовая кислота |
|
|
|
Стимулирует дифференцировку |
|
|
||
|
|
Гибберелин и другие |
Стимулирует деление клеток и рост в длину |
|
||||||
|
* Ауксин: образование каллуса. Цитокинин: незначительное деление клеток |
|
|
|||||||
|
|
|
|
|
||||||
|
Безвирусные растения, полученные из меристемной культуры* |
|
|
|
||||||
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
||
|
|
Исключен вирус |
|
|
|
Исключен вирус |
|
|
||
|
Томаты |
Вирус аспермии томата |
|
|
Хризантема |
Вирус В хризантем, |
|
|
||
|
Клубника |
Неповирус и др. |
|
|
|
stunt-вироид хризантем |
|
|
||
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
* В большинстве случаев с меристемными культурами работают при 40 °С
Гаплоидные культуры
Стерильное
удаление
цветков
Зародыш |
(гаплоидный) |
Выделение |
тычинок |
|
Колхицин или слияние протопластов |
Растение табака |
Растение табака |
(диплоидное) |
(гаплоидное) |
175
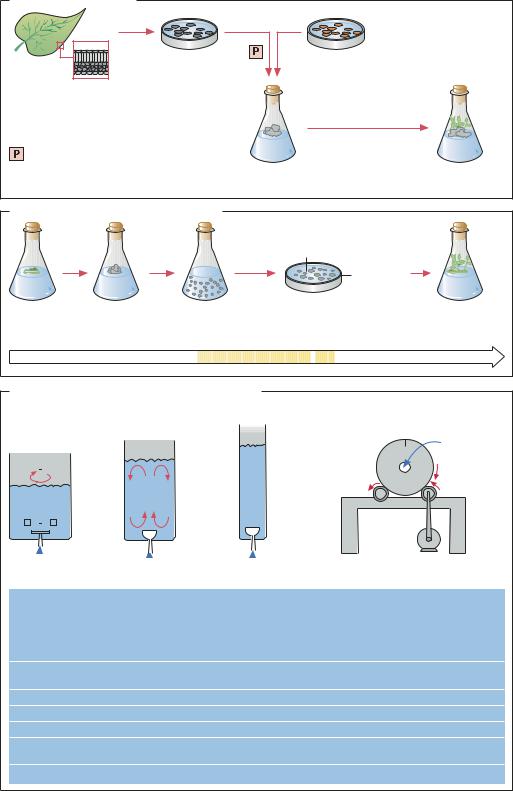
Слияние протопластов |
|
|
Культура |
Протопласты |
|
протопластов |
или цитопласты |
|
Получение протопластов |
другой клеточной линии |
|
|
|
|
(ферментативное разрушение |
|
|
клеточной стенки) |
|
|
Слияние протопластов |
|
|
при обработке |
Регенерация клеточной |
Каллусная культура |
полиэтиленгликолем |
||
или при электропорации |
стенки, каллусная культура |
гибридного растения |
Суспензионная культура для селекции |
|
|
|
|
|
Погибшие |
|
|
|
|
колонии |
|
|
|
|
Устойчивые |
|
|
|
|
колонии |
|
|
|
|
Факторы стресса: |
|
Эксплантат |
Каллус |
Клеточная |
соль, гербициды, |
Отбор |
|
|
культура |
фитотоксины, химикаты |
устойчивых |
|
|
|
|
растений |






















































































 Повышение концентрации
Повышение концентрации
 соли
соли














































































Типы биореакторов для растительных клеток
Реактор |
Эрлифтный |
Барботажная |
Ферментер с вращающимся |
с механическим |
реактор |
колонна |
барабаном |
перемешиванием |
|
|
|
|
|
|
Воздух |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Воздух |
Воздух |
Воздух |
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Растение |
Продукт |
Применение |
Масштаб производства, |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
выход продукта |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Digitalis lanata |
Метилдигоксин |
Лечение сердечно- |
Эрлифтный биореактор 300 л, |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
из метилдигитоксина |
сосудистых заболеваний |
полунепрерывный процесс, |
|||||||||||
|
|
|
|
|
|
|
|
|
(12β-гидроксилирование) |
|
|
|
|
выход ~ 75% за 40–60 ч |
||||||||
Lithospermum |
Шиконин |
Косметика |
Двустадийная реакция, |
|||||||||||||||||||
erythrorhizon |
|
|
|
|
|
|
|
|
|
|
биореакторы 200 и 750 л, 23 сут. |
|||||||||||
Berberis sp. |
Протоберберин |
Фармацевтика |
До 1,7 г/л |
|||||||||||||||||||
Panax ginseng |
Женьшень |
Медицина |
Биореактор 30 л |
|||||||||||||||||||
Coleus blumei |
Розмариновая кислота |
Фармацевтика |
— |
|||||||||||||||||||
Taxus sрp. |
Таксол |
Противоопухолевый агент |
110 мг/л за 14 сут. – |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 г/кг суспензии клеток |
|||
Vanilla planifolia |
Ванилин |
Ароматизатор |
16 мг/л за 45 сут. |
|||||||||||||||||||
177
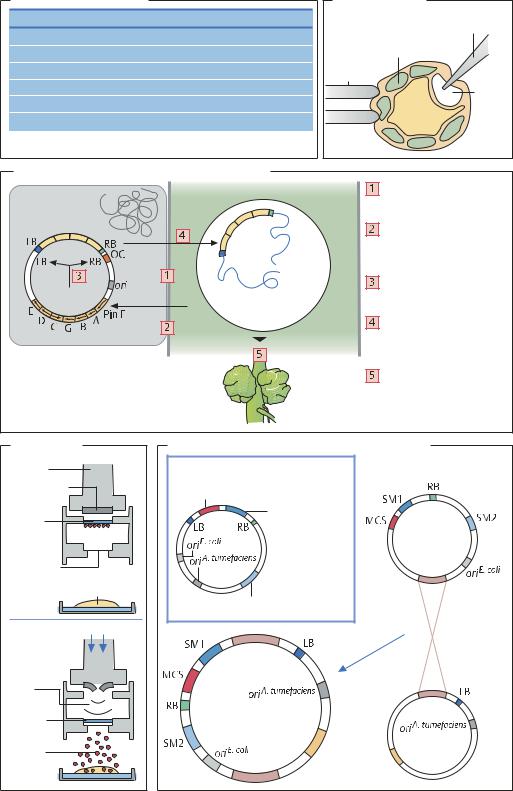
Методы трансформации |
|
|
Микроинъекция |
|
|
Однодольные |
Двудольные |
Микроинъекция |
|
Микроинъекции (протопласты) |
+ |
+ |
ДНК-конструкции |
|
|
|
|||
Трансфекция (протопласты, Са2+) |
0 |
+ |
Пластида |
|
Электропорация (протопласты) |
0 |
+ |
Удерживающий |
|
капилляр |
|
|||
|
|
|
|
|
Биолистика |
++ |
+ |
|
Клеточ- |
|
|
|
|
|
T-ДНК |
+ |
++ |
Вакуум |
ное |
Растительные вирусы |
0 |
0 |
Вакуоль |
ядро |
|
||||
0 – успешна лишь в незначительной степени; |
|
|
|
|
+ возможно; ++ рекомендуемый метод |
|
|
|
|
Заражение растения Agrobacterium tumefaciens
Бактериальная |
|
|
A. tumefaciens прикреп- |
|
|
|
ляется к поврежденной |
||
хромосома |
|
|
||
|
|
растительной клетке |
||
|
|
|
||
Ti-Плазмида |
|
|
Растительная клетка |
|
|
Т-ДНК |
|
синтезирует хемотокси- |
|
Т-Участок |
|
ческий сигнал и активи- |
||
Хромо- |
|
|||
|
|
рует область вирулентности |
||
|
сомная |
|
Область вирулентности |
|
|
ДНК |
|
||
Участок виру- |
|
|
Ti-плазмиды активирует |
|
лентности |
Клеточное ядро |
|
Т-участок |
|
|
|
|
|
|
|
|
|
Т-Участок встраивается |
|
|
|
|
в растительную хромосому |
|
|
Цитоплазма |
в виде линейного одно- |
||
Agrobacterium tumefaciens |
цепочечного участка |
|||
|
|
|
|
|
A–G = факторы вирулентности |
|
|
Ауксины и цитокинины |
|
Т-Участок содержит гены ауксина, |
|
|
||
|
|
инициируют рост опухоли, |
||
цитокинина и опина |
|
|
опин является источником |
|
ОС = разложение опина |
|
|
углерода для A. tumefaciens |
|
ori = точка начала репликации |
|
|
|
|
Биолистика |
Клонирующие вектора на основе A. tumefaciens |
|||
Камера высокого |
Бинарный вектор |
|
Система коинтегративных |
|
давления |
|
|||
|
|
векторов |
||
Закрывающая |
MCS = множественный |
|
||
|
|
|
||
сайт клонирования |
|
|
|
|
пленка |
|
|
|
|
|
|
|
|
|
Несущая |
Селективный |
|
|
|
маркер для |
|
|
Коинтег- |
|
пленка |
растений |
|
|
|
|
|
|
|
ративный |
Останавли- |
|
|
|
вектор |
|
|
|
|
|
вающая сеть |
|
|
|
|
Клетки или |
|
|
|
|
клеточная культура |
Селективный маркер |
|
|
|
|
|
|
|
|
|
для E. сoli и A. tumefaciens |
|
|
|
Механическое давление |
|
|
|
Гомологичная |
|
|
|
|
|
|
|
|
|
рекомбинация |
|
Рекомбинантная |
|
|
|
|
Ti-плазмида |
|
|
|
Волна |
|
|
|
|
давления |
|
|
|
|
Несущая |
Гены виру- |
|
|
|
пленка |
|
|
|
|
лентности |
|
|
Непатогенная |
|
|
|
|
||
Частицы |
|
|
|
|
|
Гены виру- |
Ti-плазмида |
||
ДНК |
|
|
||
|
|
лентности |
|
|
|
|
|
|
179 |