|
медицине |
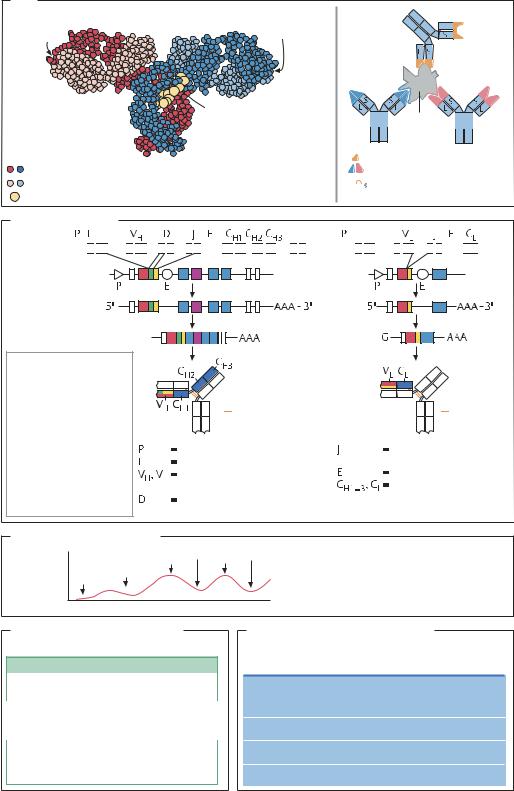
Моноклональные антитела |
|
которые представляют собой смесь различных анти- |
|
|
ВВЕДЕНИЕ. В отличие от поликлональных антител, |
|
в |
тел, продуцируемых В-лимфоцитами в ответ на |
|
Биотехнология |
|
введение животному антигена, препараты монокло- |
|
|
|
|
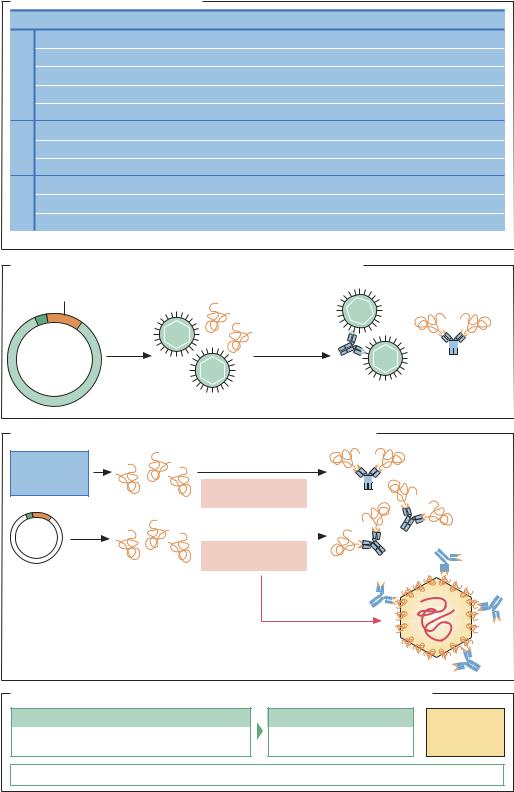
нальных антител гомогенны. Для их получения ис- |
|
|
пользуют гибридомную технологию, то есть создают |
|
|
«бессмертную» линию клеток, продуцирующих анти- |
|
|
тела определенной специфичности. |
|
|
ТЕХНОЛОГИЯ ГИБРИДОМ. Животных (обычно мышей) |
|
|
иммунизируют антигеном. Когда в организме живот- |
|
|
ного количество антител достигает высокого уровня, |
|
|
из селезенки выделяют лимфоциты. Затем осущест- |
|
|
вляют слияние этих клеток с клетками миеломной |
|
|
линии, которые обладают способностью к неограни- |
|
|
ченному росту. Часть полученных слитых клеток |
|
|
способны продуцировать антитела, как исходные |
|
|
лимфоциты, и обладают способностью к неограни- |
|
|
ченному росту, как клетки миеломы. Такие клетки |
|
|
удается выделить из смеси специальными иммуно- |
|
|
логическими методами селекции. Подходящие клоны |
|
|
замораживают при низкой температуре, и они сохра- |
|
|
няют способность к образованию антител в течение |
|
|
многих лет. |
|
|
ВЫДЕЛЕНИЕ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ. Клетки |
|
|
гибридомы обладают способностью к неограниченно- |
|
|
му росту. Их выращивают в культуре, а затем из |
|
|
культуральной жидкости выделяют моноклональные |
|
|
антитела (до 30 мг/л). В состав среды роста, кроме |
|
|
глюкозы и глутамина, входит сыворотка зародыша |
|
|
теленка, богатая важнейшими цитокинами и другими |
|
|
веществами, необходимыми для роста (например, |
|
|
лактоферрином). В настоящее время широкое рас- |
|
|
пространение получили сложные искусственные сре- |
|
|
ды. Клетки гибридомы обычно растут в аэробных ус- |
|
|
ловиях на поверхности среды, однако их можно |
|
|
выращивать и в суспензии. Для их роста необходимо |
|
|
постоянное поступление в среду кислорода и СО2. |
|
|
В лабораторных условиях клетки гибридомы выращи- |
|
|
вают в медленно вращающихся емкостях. Для |
|
|
получения антител в промышленных масштабах ис- |
|
|
пользуют биореакторы объемом до 10 м3 (в основ- |
|
|
ном реакторы с механическим перемешиванием или |
|
|
эрлифтные реакторы), в которых клетки гибридом |
|
|
культивируют на особых питательных средах с под- |
|
|
держанием постоянного уровня О2 и СО2. В период |
|
|
разработки технологии ферментации гибридом клет- |
|
|
ки выращивали на носителях с большой площадью |
|
|
поверхности, например керамических носителях с |
|
|
крупными порами, что защищало их от механическо- |
|
|
го повреждения, однако в настоящее время для про- |
|
|
мышленного получения антител, как правило, ис- |
|
|
пользуют суспензии свободных клеток гибридом. |
|
154 |
Процесс ферментации осуществляется в периодиче- |
|
ском или в непрерывном режиме, в последнем слу- |