Материал: Шмид Р. Наглядная биотехнология и генетическая инженерия
медицине |
Интерфероны |
|
||
личными клетками иммунной системы и служат сиг- |
||||
|
ВВЕДЕНИЕ. |
Интерфероны (IFN) секретируются раз- |
||
в |
нальными |
веществами: иммунный |
ответ клетки |
|
Биотехнология |
||||
обусловлен связыванием молекул |
интерферонов |
|||
|
||||
|
с INF-рецепторами. У млекопитающих выделяют |
|||
|
интерфероны трех типов: IFN-α, IFN-β и IFN-γ. Эти |
|||
|
молекулы вовлечены в регуляцию 20–30 генов и об- |
|||
|
ладают широким спектром иммунорегуляторных, |
|||
|
противовирусных и антипролиферативных (препятст- |
|||
|
вующих делению клеток) свойств. Молекулы IFN-α |
|||
|
и IFN-β стабильны при рН 5 и обладают сродством |
|||
|
к одному и тому же рецептору (IFN-рецептор I типа). |
|||
|
В отличие от IFN-α и IFN-β молекулы IFN-γ неустой- |
|||
|
чивы в кислой среде и связываются с рецепторами |
|||
|
другого типа (IFN-рецептор II типа). |
|
||
|
СВОЙСТВА И ПРИМЕНЕНИЕ. α-Интерфероны (IFN-α) |
|||
|
образуются в лейкоцитах. Их гены составляют семей- |
|||
|
ство из более 20 неаллельных генов, проявляющих |
|||
|
высокую степень гомологии. Молекулярная масса |
|||
|
этого полипептида –16 кДа, а гликозилированного до |
|||
|
26 кДа. В настоящее время IFN-α успешно применя- |
|||
|
ют для лечения гепатитов В и С, а также некоторых |
|||
|
злокачественных опухолей – рака мочевого пузыря, |
|||
|
меланомы, лейкемии и лимфомы. Объем мирового |
|||
|
рынка IFN-α в 2004 г. составил 3,2 млрд долл. США. |
|||
|
Синтез β-интерферона (IFN-β) происходит в фиб- |
|||
|
робластах. Полипептидная цепь IFN-β состоит из |
|||
|
166 аминокислотных остатков, а после гликозилиро- |
|||
|
вания ~20 кДа. IFN-β применяют при лечении рассе- |
|||
|
янного склероза. Объем рынка IFN-β достигает |
|||
|
1 млрд долл. США. Источником γ-интерферона слу- |
|||
|
жат активированные Т-лимфоциты. В свою очередь |
|||
|
IFN-γ активирует макрофаги. Белковая цепь содер- |
|||
|
жит 143 аминокислотных остатка, и в зависимости |
|||
|
от степени гликозилирования имеет молекулярную |
|||
|
массу 15–25 кДа. IFN-γ используют при лечении хро- |
|||
|
нического гранулематоза. Объем рынка IFN-γ состав- |
|||
|
ляет ~200 млн долл. США. В настоящее время ве- |
|||
|
дутся клинические испытания интерферонов в |
|||
|
терапии злокачественных опухолей (IFN-α, -β и -γ), |
|||
|
аутоиммунных заболеваний (IFN-α и -β), вирусных |
|||
|
инфекций (IFN-α и -β), ревматоидного артрита и ас- |
|||
|
тмы (IFN-γ). |
|
||
|
КЛОНИРОВАНИЕ И ЭКСПРЕССИЯ ГЕНОВ ИНТЕРФЕРО- |
|||
|
НОВ. Возможность терапевтического применения ин- |
|||
|
терферонов обсуждалась давно, однако традицион- |
|||
|
ный способ их получения путем фракционирования |
|||
|
донорской крови оказался неприменим для произ- |
|||
|
водства лекарственных препаратов. Лишь в 1986 г. с |
|||
|
помощью методов генетической инженерии удалось |
|||
|
наладить промышленное производство препаратов |
|||
|
интерферонов для клинического использования. |
|||
140 |
Клонирование генов этих белков, содержащихся в |
|||
крови в очень малых концентрациях, оказалось слож- |
||||
ной задачей, решение которой для IFN-α было найдено в 1982 г.. Процедура клонирования включала в себя следующие этапы. 1. Из лейкоцитов человека выделили мРНК, затем провели обратную транскрипцию и полученной кДНК трансформировали клетки Escherichia coli. Было получено 6000 клонов, которые разделили на группы. 2. Провели гибридизацию каждой группы клонов с неочищенным препаратом IFN-α-мРНК. 3. Осуществили трансляцию гибридных мРНК в бесклеточной системе и измерили противовирусную активность полученных белковых продуктов. 4. Провели экспрессию выбранных кДНК. Так как биологическая активность интерферона не зависит от степени его гликозилирования, для получения больших количеств белка часто используют клетки E. coli. В промышленных технологиях интерферонов используются и другие хозяева: Saccharomyces cerevisiae, Pichia pastoris, культуры животных клеток или молоко трансгенных животных.
ПОЛУЧЕНИЕ. В промышленности IFN-α начали получать с 1978 г. В качестве источника IFN-α использовали клетки лимфобластомы человека, индуцированные вирусом Сендай (клеточная линия Nawalma), в которых синтезировались по меньшей мере восемь различных изоформ IFN-α. В настоящее время почти все интерфероны получают из клеток рекомбинантных штаммов E. coli. Исключение – IFN-β1а, который получают из рекомбинантных клеток СНО. В клетках E. coli удается получать высокий выход продукта, затем белок очищают методами хроматографии. Так, фирма Roche производит интерферонα2а (Roferon A®) в рекомбинантных клетках E. coli К12. После выращивания клетки разрушают методом низкотемпературного замораживания, удаляют клеточные фрагменты центрифугированием, а белок очищают хроматографическими методами.
Copyright ОАО «ЦКБ «БИБКОМ» & ООО «Aгентство Kнига-Cервис»
Препараты интерферонов, допущенные к применению
Интерферон |
Назначение |
Фирма-производитель |
ПЭГ-IFN-α |
Гепатит В и С (ПЭГ: полиэтиленгликоль) |
Roche, Schering-Plough |
IFN-α2b |
Лейкоз, меланома, миелома |
Biogen, Yamanoochi, Enzon |
IFN-β |
Карцинома горла/носа, |
Rentschler |
|
вирусный энцефалит |
|
IFN-β1a |
Рассеянный склероз |
Biogen, Serono |
IFN-β1b |
Рассеянный склероз |
Berlex, Schering AG |
IFN-γ1a |
Ревматоидный артрит |
Rentschler |
IFN-γ1b |
Хронический гранулематоз |
Genentech, Boehringer-Ingelheim |
|
|
|
IFN-β1a производится с использованием культуры животных клеток СНО, остальные интерфероны синтезируются в рекомбинантных клетках E. coli
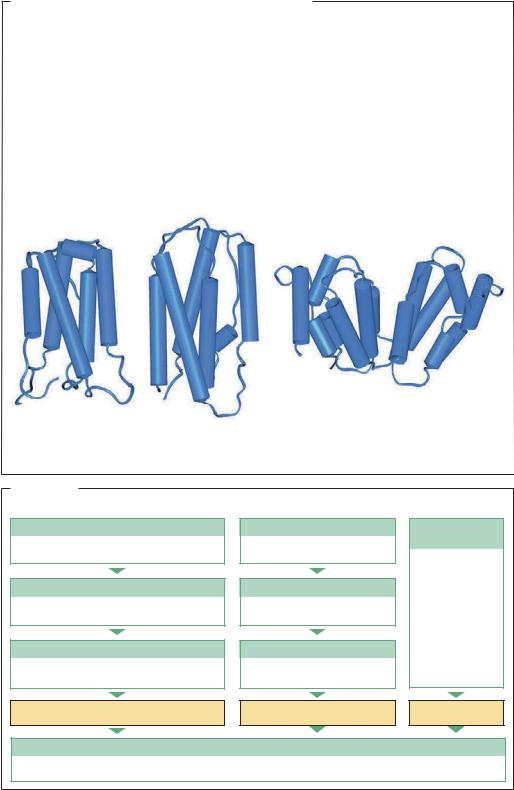
Структура молекулы |
Cтруктура молекулы |
|
Структура молекулы IFN-γ (IDC9) |
|
IFN-α (IITF) человека |
IFN-β (IA4I) свиньи; |
человека. Рентгеноструктурный |
||
по данным ЯМР |
рентгеноструктурный анализ, |
анализ, разрешение 0,3 нм |
||
|
разрешение 0,28 нм |
|
|
|
Получение |
|
|
|
|
IFN-α2a (Roche) |
|
IFN-γ1b (Boehringer-Ingelheim) |
IFN-γ |
|
Клетки E. coli |
|
Культура клеток СНО |
Трансгенные |
|
Рекомбинантные штаммы, различные |
Промотор SV40 |
козы |
||
|
||||
промоторы и сигнальные последовательности |
|
|
Вектор, несущий |
|
|
|
|
|
промотор |
Биореактор |
|
|
Биореактор |
β-лактоглобулина |
|
|
и ген IFN-γ |
||
Ферментация в среде |
|
Суспензия культуры |
человека |
|
|
|
|||
с высоким содержанием клеток |
|
|
|
|
Выделение |
|
|
Выделение |
|
Выделение телец включения, |
|
4–5 хроматографических |
|
|
методы обычной и иммунохроматографии |
разделений |
|
||
До 10 мг/л после 24 ч ферментации, |
До 1 мг/л жидкой культуры |
До 500 мг/л молока |
||
реализация с ПЭГ |
|
|||
|
|
|
|
|
|
Контроль качества продукта |
|
||
Иммунный анализ, пептидное картирование, НДС-ПЭГ-электрофорез, обращенно-фазовая ВЭЖХ, |
||||
спектрофотометрический анализ, масс-спектроскопия MALDI-TOF, проверка биологической активности |
||||
|
|
|
|
141 |
Биотехнология в медицине
142
Интерлейкины
ВВЕДЕНИЕ. Интерлейкины (IL) – сигнальные вещест- |
Действие интерлейкина-6 (IL-6) аналогично эффекту |
||
ва, которые вырабатываются одними клетками им- |
IL-1 и IL-2, кроме того, он активирует экспрессию раз- |
||
мунной системы и служат для регуляции активности |
личных белков (так называемых белков острой фазы) |
||
других клеток. Поэтому их часто называют «гормона- |
в гематоцитах и, вероятно, задействован в развитии |
||
ми иммунной системы». У человека охарактеризова- |
аутоиммунных заболеваний. Интерлейкин-10 (IL-10) |
||
ны более 20 типов интерлейкинов (IL-1–IL-23). Из |
является ингибитором синтеза других цитокинов. Ин- |
||
них IL-2 уже применяется в медицине, а другие ин- |
терлейкин-12 (IL-12) стимулирует синтез γ-интерфе- |
||
терлейкины находятся на стадии исследования. |
рона Т-лимфоцитами и NK-клетками и, как предпола- |
||
СВОЙСТВА И ПРИМЕНЕНИЕ. Интерлейкин-1 существу- |
гают, играет важную роль в осуществлении и |
||
ет в двух формах (IL-1α и IL-1β). Он синтезируется |
регуляции иммунного ответа. Подавляющее большин- |
||
фагоцитирующими клетками иммунной системы (ма- |
ство исследований, направленных на изучение воз- |
||
крофагами и моноцитами) в виде предшественника |
можности терапевтического применения рекомби- |
||
(молекулярная масса 31 кДа), который в результате |
нантных интерлейкинов, связано с терапией рака. |
||
протеолитического |
расщепления |
превращается |
Кроме того, интерлейкины могли бы применяться для |
в зрелую форму (молекулярная масса 17,5 кДа). |
заживления ран, активации иммунитета у больных |
||
Биологическая функция IL-1 заключается в стимуля- |
СПИДом и супрессии иммунной системы при транс- |
||
ции роста лимфоцитов, фибробластов, гематопоэти- |
плантации костного мозга и развитие многочисленных |
||
ческих клеток и тимоцитов. Обнаружены рецепторы |
антагонистов интерлейкинов. |
||
IL-1 двух типов: рецепторы I типа находятся на поверх- |
ПОЛУЧЕНИЕ ИНТЕРЛЕЙКИНОВ. Для осуществления |
||
ности Т-клеток и |
фибробластов, |
а рецепторы |
биологической функции IL-2 и для медицинских |
II типа – на В-лимфоцитах. Вероятный механизм дей- |
целей неважно, гликозилирован белок или нет, |
||
ствия IL-1 следующий: после того как макрофаг |
поэтому рекомбинантный IL-2 получают из клеток |
||
встретился с антигеном и осуществил его протеолити- |
Escherichia coli. В культурах со средней или повы- |
||
ческое расщепление, он начинает секретировать |
шенной плотностью клеток значительная часть экс- |
||
IL-1, который стимулирует пролиферацию и размно- |
прессированного белка оказывается в составе телец |
||
жение клеток иммунной системы. На следующей ста- |
включения, которые сначала очищают методом |
||
дии развития иммунного ответа решающая роль при- |
гель-хроматографии, затем солюбилизируют в вос- |
||
надлежит IL-2 – так называемому «фактору роста |
станавливающих условиях, а потом белок осаждают |
||
Т-клеток». IL-2 охарактеризован лучше других типов |
в окислительных условиях. Дальнейшую очистку |
||
интерлейкинов. Он вырабатывается активированными |
проводят методом ВЭЖХ, осаждением и гель- |
||
Т-клетками и стимулирует деление и рост Т- и В-кле- |
фильтрацией. Активность определяют по включению |
||
ток. Активированные Т-клетки секретируют IL-2, а так- |
Н3-меченого тимидина в IL-2-зависимые T-клетки |
||
же рецепторы, которые находятся на поверхности кле- |
мыши и развитию многочисленных антагонистов ин- |
||
ток, таким образом процесс пролиферации Т-клеток |
терлейкинов. |
||
может идти непрерывно. Другое действие IL-2 заклю- |
|
||
чается в стимуляции клеток-киллеров (NK-клеток – от |
|
||
англ. natural killer) и моноцитов с помощью рецепторов IL-2 на поверхности этих клеток. В настоящее время уже получены рентгеноструктурные данные для IL-2 – гидрофильного гликопротеина, МR 15,5 (133 аминокислотных остатка). В медицине IL-2 используют в терапии опухолей, в частности почечно-клеточного рака. IL-3 представляет собою гликопротеин, состоящий из 133 аминокислот. Он синтезируется активированными Т-лимфоцитами и действует на плюрипотентные стволовые клетки в костном мозге, стимулируя созревание лимфоцитов (нейтрофилов и макрофагов) и других клеток-предшественников иммунной системы. По этой причине IL-3 еще называют мультипотентным колониестимулирующим фактором. Ин- терлейкин-4 (IL-4) – гликопротеин, МR 20, который действует на В-клетки, активируя их дифференцировку с преимущественной продукцией IgG и IgE, а также способствует презентации антигенов моноцитами.
Интерлейкины
|
Клиническое применение |
Производитель |
Фаза испытаний |
IL-1 |
Гематопоэз |
Roche/Immunex |
Допущен к применению |
IL-1R |
Астма |
Immunex |
Допущен к применению |
IL-1RA |
Ревматоидный артрит |
Amgen |
Допущен к применению |
IL-2PEG |
ВИЧ |
Chiron |
Допущен к применению |
IL-2 |
Рак почек |
Chiron |
Допущен к применению |
IL-3 |
Трансплантация стволовых клеток |
Sandoz |
Фаза III |
IL-4 |
Рак легких |
Schering-Plough |
Фаза II |
IL-6 |
Тромбоцитопения |
Serono |
Фаза I/II |
IL-8RA |
Воспалительные процессы |
Repligen |
Последние стадии клинических испытаний |
IL-10 |
Злокачественные опухоли, |
Schering-Plough |
Последние стадии клинических испытаний |
|
аутоиммунные заболевания |
|
|
IL-11 |
Тромбоцитопения |
Genetics Institute, |
Фаза III |
|
|
Schering-Plough |
|
IL-12 |
ВИЧ, карциномы |
Genetics Institute, |
Фаза I/II |
|
|
Wyeth-Ayerst |
|
IL-15 |
Инфекционные болезни, |
Immunex |
Последние стадии клинических испытаний |
|
мукозит |
|
|
|
|
|
|
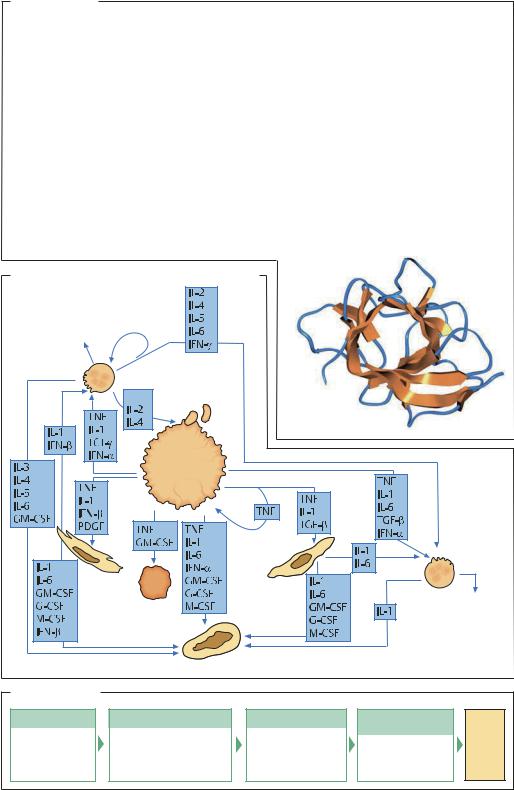
Система взаимодействий в иммунной системе
Стимуляция или подавление других Т- и В-клеток, макрофагов, уничтожение инфицированных клеток
Т-клетки
Бактерии, несущие специфические
 липополисахариды
липополисахариды
Макрофаги
Структура
IL-1α (2/1А). Рентгеноструктурный анализ, разрешение 0,20 нм
Клетки |
В-клетки |
|
эндотелия |
||
|
Фибробласты
Полиморфно- |
Пролиферируют |
|
и приобретают |
||
ядерные |
||
способность |
||
лейкоциты |
||
к образованию |
||
|
||
|
антител |
|
Костный мозг синтезирует новые клетки крови |
|
|
|
Получение IL-2 |
|
|
|
|
E. coli |
Биореактор |
Выделение |
Контроль |
|
|
|
|
качества продукта |
|
Рекомбинантный |
Объем до 1000 л, |
Получение фракции |
SDS-электрофорез, |
Чистый |
штамм, |
ферментация в среде |
телец включения, |
пептидное |
IL-2 |
устойчивый |
со средним или высоким |
хроматографические |
картирование, |
|
к тетрациклину |
содержанием клеток |
методы |
ELISA и т. д. |
|
|
|
|
|
143 |
Биотехнология в медицине
144
Эритропоэтин и другие факторы роста
ВВЕДЕНИЕ. Развитие техники работы с культурами клеток привело к обнаружению большого числа факторов роста (colony stimulating factors, CSF, колониестимулирующие факторы), которые стимулировали рост клеток в результате взаимодействия с рецепторами на клеточной поверхности. Эти факторы представляют собой цитокины – вещества, которые синтезируются клетками в очень малых количествах. Методами генетической инженерии можно получать их в необходимых количествах с целью изучения свойств, природы и механизма взаимодействия, а также возможностей терапевтического применения: особый интерес представляет направленное влияние на рост определенных типов клеток (клеток кожи, нервных клеток, эритроцитов, клеток костей и т.д.). Так, эритропоэтин, фактор роста гранулоцитов (G-CSF) и фактор роста гранулоцитов и макрофагов (GM-CSF) уже успешно применяются в медицине. Эритропоэтин стимулирует образование эритроцитов, G-CSF – нейтрофильных гранулоцитов, а GM-CSF – эозинофильных и нейтрофильных гранулоцитов, моноцитов и макрофагов. Эти факторы назначают пациентам с анемией, которая часто возникает при проведении диализа. В Германии около 40 000 пациентов принимают эритропоэтин и около 100 000 – GM-CSF. Мировой объем рынка эритропоэтина составляет около 10 млрд долл. США, G-CSF и GM-CSF – около 3 млрд долл. США (2004 г.). ЭРИТРОПОЭТИН (ЕРО) – фактор роста эритроцитов. Интенсивность биосинтеза эритропоэтина в клетках эндотелия почек и клетках Купфера в печени зависит от парциального давления кислорода в крови. Под действием ЕРО гематопоэтические стволовые клетки костного мозга теряют ядра, и в них начинается синтез гемоглобина: так происходит созревание эритроцитов. Таким образом, ЕРО стимулирует обновление клеток крови, и поэтому он используется при лечении малокровия, развивающегося у пациентов, которым проводят диализ крови (искусственная почка). В последнее время наряду с эритропоэтином при лечении таких пациентов успешно используется комбинированный препарат: факторы роста GM-CSF или G-CSF, факторы роста гранулоцитов, макрофагов и моноцитов. Ген эритропоэтина из клеток костного мозга человека клонирован в 1984 г. Гликопротеин с молекулярной массой 34 кДа представляет собой полипептид из 165 аминокислотных остатков, который гликозилирован по трем атомам азота и одному атому кислорода. На углеводные цепи приходится около 40% молекулярной массы этого гликопротеина и они, по-видимому, имеют важное функциональное значение. По этой причине поиск клеток-хозяев для экспрессии биологически активного эритропоэтина оказался чрезвычайно сложной задачей. Высокий выход функционального гликопротеина был получен в клет-
ках СНО. Кристаллическая структура эритропоэтина, связанного с внеклеточными доменами его рецепторов, представлена в таблице.
ФАКТОРЫ РОСТА. Гликопротеины, входящие в состав большой группы факторов роста, специфически стимулируют размножение и созревание клеток соединительной ткани, а также нервных, костных и других клеток. К настоящему времени гены многих факторов роста клонированы, и некоторые рекомбинантные белки уже применяются в медицине или находятся на стадии клинических испытаний. Препараты, полученные на основе этих белков, используют для лечения невропатий, остеопороза и язвенной болезни. Исследуется возможность применения фактора роста эпителия для заживления ран, в том числе после удаления катаракты. Были получены трансгенные овцы, в которых активность фактора роста эпителия увеличена по сравнению с нормой, в результате рост шерсти у таких овец значительно усилился.
ПОЛУЧЕНИЕ. Эритропоэтин получают в биореакторах объемом до 1000 л с использованием культуры животных клеток, прежде всего – рекомбинантных СНО-клеток (клетки яичника китайского хомяка). Необходимость использования животных клеток для получения эритропоэтина связана с тем, что биологически активный белок должен быть гликозилирован. Процесс ферментации продолжается 30 сут, после чего рекомбинантный белок подвергают четырехстадийной хроматографической очистке. Физиологическое действие других факторов роста не зависит от того, гликозилированы они или нет, поэтому в качестве клеток-хозяев для получения таких рекомбинантных белков используют микроорганизмы. Так, GM-CSF и G-CSF получают в клетках рекомбинантных штаммов E. coli.