Материал: Шмид Р. Наглядная биотехнология и генетическая инженерия
медицине |
Антикоагулянты и тромболитики |
|
ВВЕДЕНИЕ. Образование тромбов (инфаркт миокар- |
||
да, инсульт, закупорка сосудов) является самой |
||
в |
распространенной причиной смерти в большинстве |
|
Биотехнология |
||
развитых стран. В Германии от тромбозов ежегодно |
||
|
||
|
умирают 60 000 человек. Антикоагулянты препятст- |
|
|
вуют образованию первичных тромбов (в том числе |
|
|
при операциях), а тромболитики осуществляют про- |
|
|
теолитическое разрушение тромбов. В медицине |
|
|
находят применение такие антикоагулянты, как |
|
|
гепарин и производное кумарина, а также рекомби- |
|
|
нантные ингибиторы тромбина – гирудин (природ- |
|
|
ный источник – медицинские пиявки) и антитром- |
|
|
бин III человека (АТ-III). В качестве тромболитиков |
|
|
используют бактериальную стрептокиназу, а также |
|
|
препараты урокиназы и тканевого активатора плаз- |
|
|
миногена (tPA и rPA), полученные методами гене- |
|
|
тической инженерии. |
|
|
ГЕПАРИН – серосодержащий глюкозоаминогликан |
|
|
(мукополисахарид) с MR от 3 до 60 кДа. Его экстра- |
|
|
гируют из кишечника свиней или легких крупного ро- |
|
|
гатого скота. Гепарин синтезируется тучными клетка- |
|
|
ми и, оказавшись в плазме крови, активирует АТ-III, |
|
|
который в свою очередь связывается с тромбином и |
|
|
препятствует образованию фибрина. |
|
|
ГИРУДИН – ингибитор тромбина, обнаруженный в |
|
|
секрете слюнных желез медицинской пиявки. В на- |
|
|
стоящее время рекомбинантный гирудин получают |
|
|
ферментацией в клетках Escherichia coli и в других |
|
|
организмах-хозяевах. Действие гирудина аналогично |
|
|
действию АТ-III: он связывается с тромбином, тем са- |
|
|
мым препятствуя образованию фибрина из фибрино- |
|
|
гена. |
|
|
ТКАНЕВОЙ АКТИВАТОР ПЛАЗМИНОГЕНА (tissue plas- |
|
|
minogen activator, tPA). Расщепление фибрина при |
|
|
заживлении раны осуществляется сериновой протеи- |
|
|
назой плазмином. Активная форма плазмина образу- |
|
|
ется из плазминогена под действием тканевого акти- |
|
|
ватора плазминогена (tPA, MR 72). Это еще одна |
|
|
сериновая протеиназа, которая специфически расще- |
|
|
пляет пептидную связь между остатками аргинина и |
|
|
валина (в положениях 561 и 562) в молекуле плаз- |
|
|
миногена. Белок построен из пяти доменов, функции |
|
|
которых установлены на основании гомологии с дру- |
|
|
гими изученными белками. Функция двух доменов, |
|
|
имеющих форму торов, заключается в связывании с |
|
|
молекулой фибрина, а так называемый протеазный |
|
|
домен содержит активный центр фермента. Ген tPA |
|
|
человека был клонирован в 1982 г., а с 1988 г. пре- |
|
|
параты этого белка поступили на рынок. Наличие |
|
|
в зрелом tPA восьми дисульфидных связей и трех |
|
|
крупных углеводных компонентов, составляющих |
|
|
~25% массы и необходимых для связывания с суб- |
|
130 |
стратом, не позволяет использовать бактериальные |
|
клетки в качестве клеток-хозяев. Для получения |
рекомбинантного tPA выбирают клетки мышей или клеточные линии СНО, а образующийся белок очищают различными способами, включающими осаждение в кислой среде, а также ионообменную, гидрофобную и аффинную хроматографию. Мутанты производят фермент с искусственно измененным сайтом гликозирирования и четырьмя аминокислотными заменами (TNK-tPATM), который прочно связывается с фибрином и имеет более продолжительное время полураспада в сыворотке. В этой связи вместо использования инфузии можно провести однократное введение. Мутанты E. coli с нарушенной функцией гликозилирования синтезируют фермент, лишенный петлевого-1 и eGF-доменов (RepilysinTM), однако его выделение из телец включения оказывается затруднительным. По сравнению с tPA время пребывания этого белка в сыворотке в 3–4 раза больше, а аллергенные свойства выражены слабее. tPA также секретируется с молоком трансгенных коз и овец, которые трансформированы вектором, содержащим фрагмент tPA-кДНК под промотором лактальбумина. Белок tPA, кроме того, получают из молока трансгенных коз и овец, в которых ген tPA клонирован за промотором лактальбумина. Для контроля однородности полученного таким способом tPA требуется применение специальных аналитических методов.
ДРУГИЕ ТРОМБОЛИТИКИ. Урокиназа – сериновая протеиназа; в виде проурокиназы присутствует в сыворотке крови и в моче. Подобно tPA, урокиназа гидролизует плазминоген с образованием плазмина. Обнаружены две формы белка с MR 54 и 30: белок меньшего размера образуется из большего при автолизе, и обе формы обладают биологической активностью. Урокиназу выделяют из мочи, культуры клеток почек человека или в виде рекомбинантного продукта из клеток E. coli. Стрептокиназа образуется в различных гемолитических стрептококках. Этот белок не обладает каталитической активностью, однако вызывает конформационные изменения в молекуле плазминогена, что приводит к автолизу с образованием плазмина. Стрептокиназу получают из культур стрептококков методами хроматографии. Применение других, более дешевых способов очистки белка, связано с риском возникновения сильных иммунных реакций.
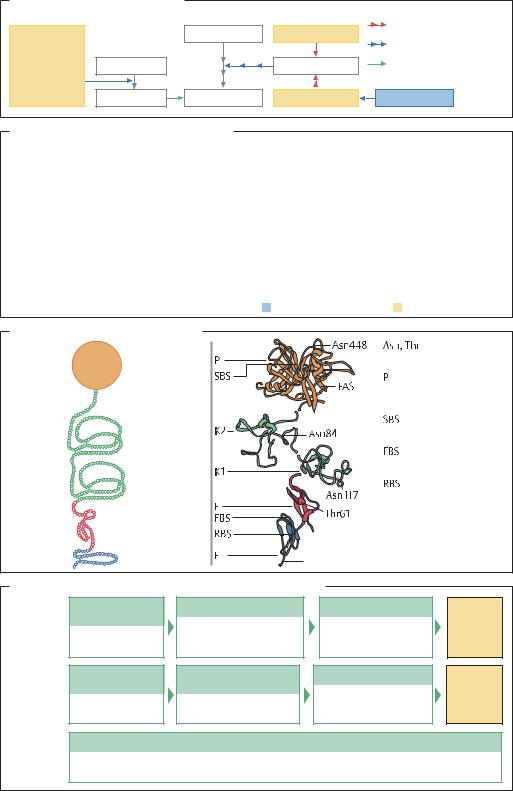
Упрощенная схема тромболиза |
|
|
||
|
Тромболиз |
Свертывание крови |
|
Ингибирование |
|
|
Фибриноген |
Гирудин |
|
Тканевой |
|
Активация |
||
|
|
|
||
активатор |
|
|
Тромбин |
Протеолитическое |
плазминогена, |
Плазминоген |
|
||
урокиназа, |
|
|
|
расщепление |
стрептокиназа |
Плазмин |
Фибрин |
Антитромбин-III |
Гепарин |
|
||||
Антикоагулянты (А) и тромболитики (Т) |
|
|
||
|
Тип |
Действие |
Производитель |
Гепарин |
А |
Серосодержащий полисахарид, связывается |
Celsus |
|
|
с антитромбином III и инактивирует тромбин |
|
Гирудин |
А |
Ингибирует тромбин |
Novartis, Behringwerke* |
Антитромбин-III |
А |
Ингибирует тромбин |
Genzyme Transgenic Corp. |
Стрептокиназа |
Т |
Активирует плазминоген |
Kabi Upjoin* |
Урокиназа |
Т |
Активирует плазминоген |
Grüenenthal* |
Тканевой активатор |
T |
Активирует плазминоген |
Genentech*, Boehring, |
плазминогена |
|
|
Ingelheim*, Roche* |
|
|
|
|
* Препарат разрешен к применению |
Природное соединение |
Рекомбинантный белок |
||||
Тканевой активатор плазминогена |
|
|
|
|||
|
Ретеплаза – |
|
|
Участки |
||
|
|
|
гликозилирования |
|||
Протеазный |
мутантный белок, |
|
||||
|
|
|
||||
домен |
не содержащий |
|
Домен с протео- |
|||
|
домена |
|
|
|||
|
|
|
литической |
|||
|
фактора роста |
|
||||
|
|
активностью |
||||
|
и «тора 1», |
|
|
|||
|
|
|
|
|
||
|
может |
|
|
Участок связыва- |
||
|
существовать |
|
||||
«Тор 2» |
|
ния субстрата |
||||
в крови в 3 раза |
|
|||||
|
дольше, чем |
|
|
Участок связыва- |
||
|
нативный белок |
|
||||
|
|
ния с фибрином |
||||
|
|
|
|
|||
«Тор 1» |
|
|
|
Участок связыва- |
||
|
|
|
|
|||
|
|
|
|
ния с рецептором |
||
Фактор роста |
|
|
|
|
|
|
(домен Е) |
|
|
|
|
|
|
«Палец» |
|
|
N-Конец |
|
|
|
(домен F) |
|
|
|
|
||
Получение тканевого активатора плазминогена (пример) |
|
|
||||
|
Рекомбинантные |
Клеточный реактор |
Выделение и очистка |
Выход |
||
Клеточный |
клетки СНО |
|
|
|
||
Реактор объемом до 20 м3, |
Многостадийная |
|
продукта |
|||
реактор |
|
|
||||
Вектор |
сложная питательная |
иммунохроматография |
несколько |
|||
|
||||||
|
СНО-NEOSPLA |
среда, 37°С, 20 сут. |
|
|
мг/л в сут. |
|
|
Трансгенное |
Характеристика |
Выделение и очистка |
Выход |
||
Трансгенные |
животное |
животного |
|
|
||
Осаждение в кислых |
продукта |
|||||
козы |
|
|
||||
Вектор LSAP + PA |
|
до 30 г/л |
||||
|
Период лактации 240 дней, |
условиях, бутилсефароза, |
||||
|
|
3–4 л молока в день |
иммунохроматография |
молока |
||
|
|
|
||||
|
|
Контроль качества |
|
|
||
|
Обращенно-фазовая ВЭЖХ, электрофорез в денатурирующих условиях, ELISA, |
|
||||
|
пептидное картирование, определение степени гликозилирования и другие методы |
|
||||
|
|
|
|
|
131 |
|
Copyright ОАО «ЦКБ «БИБКОМ» & ООО «Aгентство Kнига-Cервис»
Биотехнология в медицине
132
Ингибиторы ферментов
ВВЕДЕНИЕ. В современной медицине широко используются ингибиторы ферментов. Например, ингибитор протеаз апротинин, получаемый из отходов при переработке мяса, применяют для терапии шоковых состояний, а рекомбинантный α1-антитрипсин в будущем, возможно, найдет применение для лечения эмфиземы легких. Множество микробных ингибиторов протеаз (лейпептины, пепстатин, антипаин, химостатин, эластиналь) пока не нашли применения
вмедицине, однако активно используются в фундаментальных исследованиях. Ингибитор α-гликозидазы акарбозу успешно применяют при лечении диабета, а ингибитор панкреатической липазы тетрагидролипстатин – при лечении ожирения.
АПРОТИНИН – полипептид, состоящий из 58 амино-
кислот (МR 6511), ингибирует такие протеазы как трипсин, химотрипсин и плазмин. Другое название апротинина – панкреатический ингибитор трипсина. Константа ингибирования трипсина с помощью апротинина составляет 10–11 М. Лекарственные препараты, содержащие апротинин (Trasylol®), применяют для лечения панкреатитов, при трансплантации органов, а также при сильных кровотечениях и шоковых состояниях. Перспективным считается применение апротинина в работе с культурами животных клеток:
вэтом случае апротинин препятствует протеолитическому расщеплению рекомбинантных белков. Апротинин экстрагируют из поджелудочной железы или легких крупного рогатого скота, а затем очищают хроматографическими методами. Белок негликозилирован, следовательно, может быть получен как рекомбинантный продукт в бактериальных клетках, в том числе в Escherichia coli.
α1-АНТИТРИПСИН (α-АТ). Этот гликопротеин (МR 54 кДа), закодированный в 14-й хромосоме человека, образуется в печени и при концентрации ~2 г/л ингибирует более 90% всей ферментативной
активности, проявляющейся во фракции α1-глобули- нов сыворотки крови. Одним из субстратов α1-анти- трипсина является эластаза, образующаяся в нейтрофильных гранулоцитах и осуществляющая протеолитическое расщепление эластина – основного структурного компонента легочной ткани. Таким образом, α-АТ предотвращает разрушение ткани легких. В Северной Европе у населения нередко встречается генетический дефект α-АТ – замена Lys53 на Glu (такой α-АТ называется α-АТ Z-типа). В случае такой мутации значительно снижается уровень секреции α-АТ из клеток печени, и его содержание в крови составляет лишь 15% нормы. Наличие α-антитрипсина Z-типа особенно опасно для курящих, так как в табаке содержатся вещества, окисляющие Met358 α-АТ, который играет важную роль при ингибировании эластазы. Под действием эластазы в легочной ткани
развиваются эмфиземы, что в большинстве случаев вызывает удушье и смерть. Внутривенное введение ингибиторов эластазы (около 200 г в год) позволяет замедлить развитие болезни. Основным источником α-АТ является кровь доноров. Для получения рекомбинантного ингибитора предпочитают клетки Saccharomyces cerevisiae, так как биологически активный α-АТ должен быть гликозилирован, следовательно, продукт, образующийся в клетках E. coli, оказывается неактивным. Экономически выгодна экспрессия рекомбинантного α-АТ, слитого с β-лактальбумином, в молочных железах овцы.
АКАРБОЗА (Glucobay®) – это псевдотетрасахарид, получаемый из культур Actinoplanes utahensis. Акарбоза является конкурентным ингибитором α-глюко- зидаз. Под действием акарбозы в желудочно-кишеч- ном тракте снижается уровень глюкозы, поэтому ее применяют в качестве антидиабетического средства. Производство акарбозы основано на микробной ферментации. К настоящему времени клонированы некоторые гены, участвующие в биосинтезе акарбозы.
ЛИПСТАТИН (ЛИПОСТАТИН) – липофильный эфир, содержащий β-лактоновое кольцо и боковую цепь, несущую N-формил-L-лейцин. Это вещество получают из культуры Streptomyces toxytricinii. В результате каталитического гидрирования из липстатина образуется тетрагидролипстатин (Xenical®). Оба вещества (липстатин и тетрагидролипстатин) ковалентно связываются с остатком серина в активном центре липаз. При оральном применении этих веществ в желудочно-кишечном тракте происходит ингибирование панкреатической липазы, осуществляющей гидролиз триглицеридов, а переваривание свободных жирных кислот не нарушается. По этой причине при ожирении назначают прием тетрагидролипстатина. Липстатин и тетрагидролипстатин получают химическим синтезом или ферментацией в клетках Streptomyces toxytricinii с последующей экстракцией и хроматографической очисткой. Объем рынка в США составляет около 500 млн долл. (2004 г.).
Copyright ОАО «ЦКБ «БИБКОМ» & ООО «Aгентство Kнига-Cервис»
|
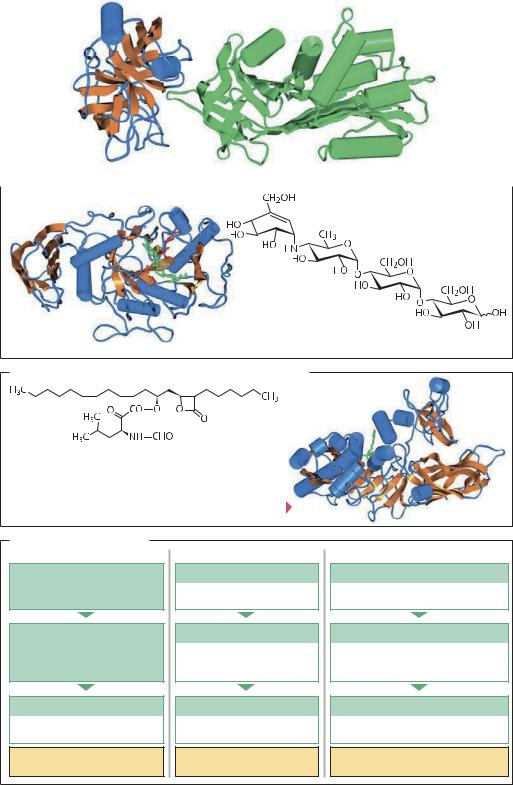
α1-Aнтитрипсин – ингибитор протеаз |
|
|
|
|
Зеленым показана |
|
Структура эластазы |
структура |
||
человека, установ- |
α1-антитрипсина |
||
ленная методом |
человека |
||
рентгено- |
(разрешение |
||
структурного |
0,16 нм) (1-ATS) |
||
анализа, |
|
||
с разрешением |
|
||
0,16 нм (1-EGS) |
|
||
|
|
|
MR = 54 кДа |
|
|
|
Код CAS = 9041-92-3 |
|
|
|
|
|
Акарбоза – ингибитор α-глюкозидазы |
|
|
|
MR = 645,61 |
||
|
|
|
|
|
|
|
Код CAS = 56180-94-0 |
Акарбоза |
Акарбоза взаимодействует с модельной мишенью |
(зеленый цвет) панкреатической амилазы свиньи (1PAA). |
По данным рентгено-структурного анализа с разрешением 0,23 нм |
Тетрагидроксилипстатин (Xenical®) – ингибитор липаз |
MR = 495,74 |
Код CAS = 96829-58-2 |
Структура комплекса тетрагидроксилипстатина |
(зеленый цвет) с панкреатической липазой |
человека (1 HUP). Разрешение 0,23 нм |
Получение ингибиторов |
|
|
|
α1-Антитрипсин |
Акарбоза |
Тетрагидроксилипстатин |
|
Трансгенные овцы |
Предферментация |
Предферментация |
|
Штамм–cуперпродуцент |
Штамм–cуперпродуцент |
||
«Tracy» |
|||
|
Actinoplanes utahensis |
Streptomyces toxytricinii |
|
|
Биореактор |
Биореактор |
|
Молоко |
Объем несколько кубометров; |
Объем несколько кубометров; среда, |
|
среда, содержащая крахмал; |
содержащая крахмал, или декстрин; |
||
|
|||
|
мальтоза, 5–6 сут при 28 °С |
соевая мука, 124 ч при 28 °С |
|
Выделение и очистка |
Выделение и очистка |
Выделение и очистка |
|
Осаждение казеина, |
Фильтрация, ионообменная |
Фильтрация, экстракция этилацетатом, |
|
хроматография |
хроматография |
обращенно-фазовая хроматография |
|
Выход продукта: 10 мг чистого |
Выход продукта: |
Выход продукта: |
|
α1-антитрипсина/л молока |
несколько г/л |
несколько г/л |
|
|
|
133 |
медицине |
Иммунная система |
|
организмы от инфекционных болезней и многих пато- |
||
|
ВВЕДЕНИЕ. Иммунная система защищает высшие |
|
в |
генов. Функционирование иммунной системы обеспе- |
|
Биотехнология |
||
чивают специализированные клетки, которые сообща- |
||
|
||
|
ются между собой и другими клетками организма с |
|
|
помощью особых сигнальных веществ-регуляторов. |
|
|
Цитотоксические Т-клетки иммунной системы способ- |
|
|
ны узнавать не только возбудителей болезни, но и |
|
|
собственные поврежденные клетки организма (апоп- |
|
|
тоз), в том числе раковые клетки. Т-клетки также при- |
|
|
нимают участие в отторжении чужеродной ткани при |
|
|
трансплантации. Генетически запрограммированное |
|
|
разнообразие и изменчивость иммунной системы |
|
|
позволяет ей приспосабливаться к изменяющимся |
|
|
условиям окружающей среды. Нарушения функцио- |
|
|
нирования иммунной системы приводят к различ- |
|
|
ным патологиям, среди которых иммунодефицит, |
|
|
аллергии, аутоиммунные болезни. В регуляции им- |
|
|
мунной системы принимают участие множество ве- |
|
|
ществ (цитокины, факторы роста и др.), некоторые |
|
|
уже доступны как рекомбинантные продукты. |
Внастоящее время изучаются возможности их терапевтического применения.
КЛЕТКИ ИММУННОЙ СИСТЕМЫ. В костном мозге продуцируются гематопоэтические стволовые клетки, которые затем дифференцируются в миелоидные или лимфатические стволовые клетки. Миелоидные стволовые клетки дают начало тромбоцитам, гранулоцитам и макрофагам, а из лимфатических стволовых клеток образуются лимфоциты, поступающие в кровь
илимфатическую систему. В организме здорового взрослого человека присутствует около 1012 «наивных» лимфоцитов, которые еще не вступали в контакт с антигенами. При взаимодействии таких клеток с антигеном (или под действием сигнальных веществ) происходит активация лимфоцитов, и путем селективного клонирования образуется большое количество дочерних клеток, специфических к этому антигену. Лимфоциты продложают дифференцировку до В-кле- ток и Т-лимфоцитов. Созревшие в костном мозге В-клетки поступают в селезенку или лимфатические узлы и в ответ на действие антигена синтезируют антитела (гуморальный иммунный ответ). Клеточный иммунный ответ осуществляется Т-лимфоцитами. Т-лимфоциты созревают в тимусе. Там они взаимодействуют с молекулами главного комплекса гистосовместимости (major histocompatibility complex, MHC), экспонированными на поверхности клеток.
Врезультате этого взаимодействия образуются специфические поверхностные структуры с различными функциями. В создании клеточного иммунного ответа важная роль принадлежит цитокинам – они секретируются Т-лимфоцитами. Например, клетки-помощни-
134 ки (Т-хелперы) выделяют интерлейкины, которые ак-
тивируют деление и созревание В-клеток. Т-хелперы несут на своей поверхности гликопротеин CD4. Цитотоксические Т-лимфоциты (клетки-киллеры) обладают способностью лизировать зараженные вирусом клетки и выделять цитокины: γ-интерферон и лимфотоксин α. На поверхности клеток-киллеров находится гликопротеин CD8.
ИММУННЫЙ ОТВЕТ И ЦИТОКИНЫ. В организме существуют различные специфическе механизмы иммунного ответа на инфекции, вызываемые вирусами, бактериями или паразитами. Антитела обладают способностью специфически связываться с внеклеточными патогенами или их токсинами, и такие комплексы служат сигналом для макрофагов, которые уничтожают патоген. Внутриклеточные патогены, например микобактерии или вирусы, а также трансформированные клетки, экспрессирующие гетерологичный белковый продукт, разрушаются по другому механизму: в результате встречи таких патогенов с макрофагом на его поверхности оказываются экспонированными фрагменты лизированных клеток. Это запускает целый каскад реакций, приводящих к разрушению инфицированных клеток цитотоксическими Т-лимфоцитами. При диабете II типа (аутоиммунное заболевание) собственные белки β-клеток поджелудочной железы воспринимаются иммунной системой как чужие и разрушаются под действием клеток-кил- леров. Взаимодействие большого количества клеток, участвующих в формировании иммунного ответа, осуществяется посредством цитокинов. Клетки иммунной системы несут на своей поверхности рецепторы для цитокинов. Формирование иммунного ответа в организме регулируется по сложному механизму. Факторы роста, специфические для различных типов клеток, обеспечивают образование новых клеток иммунной системы. В настоящее время активно изучаются возможности использования рекомбинантных цитокинов и факторов роста в медицинских целях, и в некоторых случаях уже разработаны стратегии их терапевтического применения.