Материал: Шмид Р. Наглядная биотехнология и генетическая инженерия
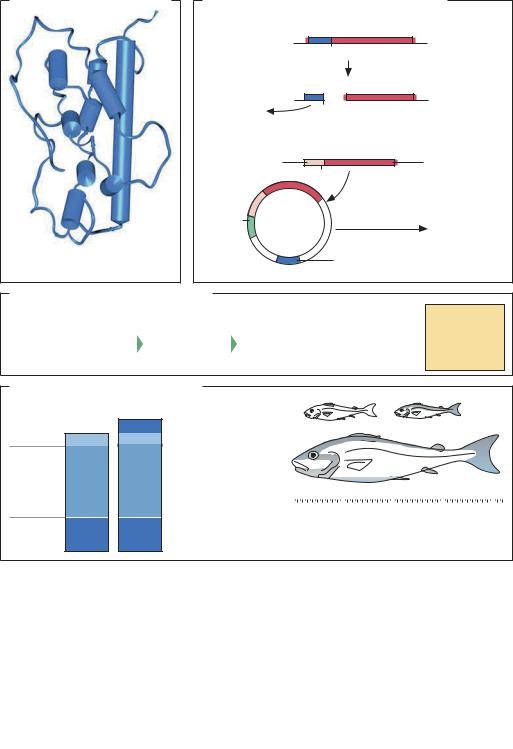
Соматотропин (гормон роста)
Соматотропин человека. Разрешение 0,25 нм (1HGU)
Клонирование гена соматотропина человека |
|||||
a Получение фрагментов кДНК соматропина |
|
||||
|
0 |
24 |
|
191 |
|
|
|
HaeIII* |
|
||
|
|
|
Расщепление рестриктазой HaeIII |
||
|
0 |
24 |
24 |
191 |
|
Удаление |
|
|
Фрагмент не расщеплен |
||
фрагмента |
|
|
|
|
|
б Экспрессия |
0 |
24 |
191 |
|
|
Синтетическая |
кДНК |
||||
|
|
|
|||
препоследова- |
|
|
|
|
|
тельность |
|
|
|
|
|
|
|
|
Трансформация |
||
Промотор |
|
|
клеток E. coli |
Синтез |
|
|
|
|
|
соматотропина |
|
|
|
|
Селективный маркер |
||
* HaeIII – рестриктаза, выделенная из Haemophilus aegyptius |
|||||
Получение и очистка гормонов роста
Cтартовая культура |
|
Биореактор |
|
Выделение |
Клетки E. coli K12, |
|
Питательная |
|
Лизис клеток, хроматография, |
трансформированные |
|
среда для |
|
индуцированное изменение заряда |
плазмидой, несущей ген |
|
E. coli, 37 °С |
|
молекулы, гель-хроматография |
гормона роста человека |
|
|
|
и ионообменная хроматография |
Гормон роста человека (например, нордитропин)
Соматотропин и выработка молока
Прибыль |
при 25 л |
при 35 л |
|
|
молока/сут |
молока/сут |
|
|
|
|
|
|
|
|
|
Нефикси- |
В расходы |
|
рованные |
||
на корм скоту |
||
расходы |
||
включены инъекции |
||
|
||
|
соматотропина |
|
|
1 раз в неделю |
Фиксированные расходы
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
10 |
|
20 |
|
30 см 40 |
|
|||||||||
Трансгенный лосось, несущий клонированный ген гормона роста лосося (наверху – контрольные экземпляры)
|
Другие гормоны, полученные в виде рекомбинантных продуктов |
|
|
|
|||
|
|
|
|||||
|
|
|
|
|
|
||
|
|
Применение |
Фирма-производитель |
Внедрение |
|
|
|
|
Глюкагон |
Гипогликемия |
Novo |
Допущен к применению |
|
|
|
|
Фолликулостимулирующий |
Бесплодие |
Serono, Organon и др. |
Допущен к применению |
|
|
|
|
гормон |
|
|
|
|
|
|
|
Кальцитонин (лососевый) |
Остеопороз |
Novartis |
Допущен к применению |
|
|
|
|
Фрагмент паратиреоидного |
Остеопороз |
Eli Lilly |
Допущен к применению |
|
|
|
|
гормона (ПТГ) |
|
|
|
|
|
|
|
Ингибин |
Контрацептив |
|
Исследоание |
|
|
|
|
Лептин/Адипонектин |
Средство, снижающее |
Исследование |
|
|
||
|
|
аппетит |
|
|
|
|
|
|
Тироидстимулирующий |
Рак щитовидной |
Genzyme |
Средство для лечения редкого |
|
|
|
|
гормон |
железы |
|
заболевания (орфанный препарат) |
|
|
|
|
Атриальный |
Почечная |
Genetech/Scios |
Исследование |
|
|
|
|
(предсердный) натрий- |
недостаточность |
|
|
|
|
|
|
уретический пептид |
|
|
|
|
|
125 |
|
|
|
|
|
|
|
|
Биотехнология в медицине
126
Гемоглобин, сывороточный альбумин и лактоферрин
ВВЕДЕНИЕ. Кровь состоит из плазмы и клеток (эрит- |
становятся мишенью для действия клеточных проте- |
роцитов, лейкоцитов и тромбоцитов). Для организма |
иназ. Сейчас ведутся исследования с целью исправ- |
кровь – самая главная жидкая среда, обеспечиваю- |
ления этих существенных недостатков, например, пу- |
щая транспорт веществ, регуляцию температуры, |
тем микрокапсулирования гемоглобина для его |
водно-солевой обмен и кислотно-щелочное равнове- |
направленной доставки. |
сие, а также защиту от патогенных факторов. Более |
СЫВОРОТОЧНЫЙ АЛЬБУМИН. Этот негликозилиро- |
20% всех генов человека кодируют белки крови. |
ванный белок (МR 69) синтезируется в печени в ви- |
Гемоглобин эритроцитов служит для доставки кисло- |
де преальбумина. Сывороточный альбумин составля- |
рода к 1013 клеткам организма. Для транспорта в ор- |
ет значительную часть белков плазмы крови (около |
ганизме нерастворимые в воде вещества часто свя- |
60%), поэтому он играет решающую роль в поддер- |
зываются с сывороточным альбумином. В настоящее |
жании осмотического давления крови. Способность к |
время разработаны генно-инженерные методы полу- |
комплексообразованию позволяет этому белку |
чения многих белков крови, например ингибитора α- |
выполнять транспортную функцию путем связывания |
антитрипсина, который переносится кровью и служит |
с такими труднорастворимыми веществами, как, на- |
для защиты легочной ткани от действия эластазы, и |
пример, липиды. Препараты, содержащие сыворо- |
антибактериального агента лактоферрина, содержа- |
точный альбумин, используют прежде всего при |
щегося в молоке. Синтез антител и размножение |
шоковых состояниях, вызванных большой кровопоте- |
клеток, участвующих в иммунном ответе, регулиру- |
рей, а также при различных заболеваниях почек и пе- |
ются посредством цитокинов. Гормоны осуществля- |
чени. Источником сывороточного альбумина служит |
ют регуляцию многих клеточных функций с высокой |
кровь доноров, из которой белок выделяют в резуль- |
специфичностью, например под действием факторов |
тате многоступенчатой хроматографической очистки |
роста происходит стимуляция роста тех или иных ти- |
и высаливания. Прогреванием препаратов при 60 °С |
пов клеток. Вязкость крови регулируется сложным |
в течение нескольких часов удается обезвредить |
каскадом белковых взаимодействий. В норме эта си- |
большинство вирусов и других патогенных факторов, |
стема предотвращает агрегацию тромбоцитов, а в |
которые могут присутствовать в крови донора, однако |
случае повреждения кровеносного сосуда способст- |
известны случаи, когда при переливании крови про- |
вует их связыванию с фибрином. Дефекты такого |
исходило заражение пациента. Этим объясняются |
комплекса приводят к различным заболеваниям. |
многочисленные попытки получить сывороточный |
Развитие методов генетической инженерии впервые |
альбумин как рекомбинантный белок в процессе фер- |
позволило детально изучить процесс поддержания |
ментации. Так были получены рекомбинантные штам- |
необходимой вязкости крови и разработать препара- |
мы Bacillus subtilis, E. coli, пекарских дрожжей и Pichia |
ты для терапии нарушений в этой системе. |
pastoris, продуцирующие сывороточный альбумин, и |
ГЕМОГЛОБИН – белок эритроцитов, обеспечивающий |
выведены трансгенные растения и животные (козы), в |
перенос кислорода в организме. Гемоглобин взрос- |
которых синтезируется этот белок. Однако такие пре- |
лого человека негликозилирован и построен из двух |
параты пока находятся на стадии испытаний и не до- |
идентичных α- и двух идентичных β-цепей, вместе |
пущены к медицинскому применению. |
составляющих тетрамер α2β2 с молекулярной мас- |
ЛАКТОФЕРРИН (МR 69) обладает антибактериаль- |
сой 64 кДа. Каждая из цепей несет гемовую группу. |
ными и противовоспалительными свойствами, веро- |
Связывание молекулы кислорода с одной гемовой |
ятно, благодаря своей способности связывать ионы |
группой повышает сродство остальных гемовых групп |
Fe3+. В материнском молоке содержится до 100 мг/л |
к кислороду (аллостерическая регуляция). При силь- |
лактоферрина. Для получения рекомбинантного лак- |
ных кровопотерях пациент получает жизненно необ- |
тоферрина его ген встраивали под промотор αs1-ка- |
ходимое количество гемоглобина в форме концент- |
зеина в молочных железах коровы, выход белка в |
ратов эритроцитов или путем переливания крови. |
молоке таких трансгенных коров составлял до 30 г/л. |
Однако при этом велика вероятность заражения |
Предложено применение этого препарата как обще- |
вирусными заболеваниями и возникновения имму- |
укрепляющего средства, его следует принимать пе- |
нных реакций. Поэтому особенно важным оказалось |
рорально. |
клонирование гена гемоглобина человека в клетках |
|
Escherichia coli, дрожжей и в трансгенных свиньях. |
|
Перед использованием в медицинских целях экс- |
|
прессированный гемоглобин тщательно очищают ме- |
|
тодами хроматографии. Выделенный белок токсичен |
|
для клеток печени, а также нестабилен вне эритроци- |
|
тов: он легко превращается в αβ-димеры, которые |
|
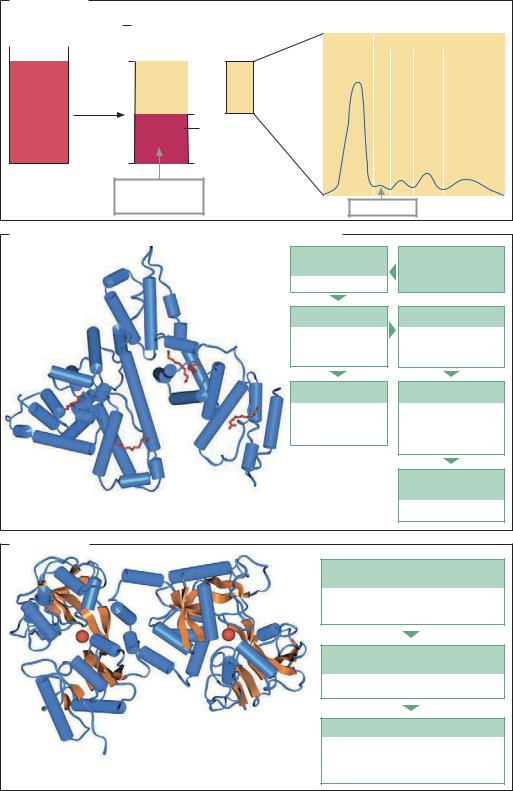
Белки крови |
|
|
|
Электрофоретическое |
|
|||
|
а = Гематокрит |
|
|
|
||||
Кровь |
Плазма |
|
разделение белков |
|
|
|||
|
b |
|
|
Альбумин |
|
|
Глобулин |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
α1 |
α2 |
β |
γ |
|
а |
|
65–80 г/л |
60% |
4% 8% |
12% |
16% |
|
|
Плазма |
|
|
|
|
|
|
|
Центрифу- |
|
белков |
|
|
|
|
|
|
|
|
(100%) |
|
|
|
|
|
|
гирование |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Клетки |
|
|
|
|
|
|
|
|
крови |
|
|
|
|
|
|
|
b |
|
|
|
|
|
|
|
Основной белок – |
|
|
|
|
|
|
|
|
|
гемоглобин |
|
|
Лактоферрин |
|
|||
|
|
|
|
|
||||
Получение альбумина фракционированием донорской крови |
|
|
|
|
||||
|
|
|
|
Фильтрация, |
|
|
Донорская кровь: |
|
|
|
|
|
высаливание |
|
|
плазма |
|
|
|
|
обессоленная плазма |
|
|
|
||
|
|
|
|
ДЭАЭ-сефароза |
|
|
ДЭАЭ-сефароза |
|
|
|
|
рН 5,2: иммуно- |
|
рН 4,4: фракция, |
|||
|
|
|
глобулины |
|
обогащенная |
|
||
|
|
|
|
|
|
альбумином |
|
|
|
|
|
|
ДЭАЭ-сефароза |
|
|
СМ-сефадекс |
|
|
|
|
рН 4,0: |
|
Градиент концентра- |
|||
|
|
|
гликопротеины, |
|
ции соли, рН 4,2–8,1: |
|||
|
|
|
церулоплазмин |
|
разные белки; |
|||
|
|
|
|
|
|
рН 5,5: альбумин |
||
|
|
|
|
|
|
Ультрафильтрация, |
||
|
|
|
|
|
|
|
сефакрил |
|
Сывороточный альбумин человека: разрешение 0,24 нм; |
|
|
|
Чистый альбумин |
||||
красным показаны 5 остатков миристиновой кислоты (1 HSA) |
|
|
||||||
|
|
|
|
|
||||
Лактоферрин |
|
|
|
|
|
|
|
|
|
|
|
|
Трансгенные животные |
||||
|
|
|
|
(крупный рогатый скот) |
||||
|
|
|
|
В геном под контролем промоторов |
||||
|
|
|
|
αS1-казеиновых генов клонирована |
||||
|
|
|
|
кДНК лактоферрина человека |
|
|||
|
|
|
|
Выделение из молока |
|
|||
|
|
|
|
трансгенного животного |
||||
|
|
|
|
Добавление 0,4 М NaCl к молоку |
||||
|
|
|
|
и очистка на S-сефарозе |
|
|||
|
|
|
|
Контроль качества |
|
|||
|
|
|
|
Пептидное картирование, |
|
|||
Лактоферрин человека: разрешение 0,24 нм; |
|
масс-спектроскопия MALDI-TOF, |
||||||
|
двумерный гель-электрофорез, |
|
||||||
красным показаны ионы Fe (1 BJ5) |
|
|
|
|||||
|
|
анализ гликозилирования |
|
|||||
|
|
|
|
127 |
||||
|
|
|
|
|
|
|
|
|
Биотехнология в медицине
128
Факторы свертывания крови
ВВЕДЕНИЕ. Для предотвращения кровопотери при повреждении сосудов существует эффективный механизм, заключающийся в образовании тромба. Этот процесс, называемый гемостазом, представлен сложным набором реакций, проходящим в несколько этапов: активация зимогенов (предшественников протеиназ), протеолиз и ингибирование протеолиза. Cложная система регуляции свертывания крови предотвращает образование тромбов в неповрежденных сосудах. При свертывании крови растворимый белок фибриноген превращается в нерастворимый полимер фибрин путем протеолиза, катализируемого сериновой протеиназой тромбином. В таком «мягком» тромбе фактор XIIIа (фермент трансглутаминаза) обеспечивает формирование амидных связей, что приводит к формированию нерастворимого сгустка. В свою очередь тромбин образуется из протромбина под действием фактора Xа, а в регуляции этого процесса принимают участие белки фактора VIII. Мутации в генах белков фактора VIII являются причиной наиболее распространенных генетических заболеваний крови – гемофилии А и В.
ГЕМОФИЛИЯ. Первые упоминания об этой болезни встречаются на глиняных дощечках, дошедших до нас из Древнего Египта. Существует три клинических типа заболевания: гемофилия А, гемофилия В и болезнь фон Виллебранда. Гемофилия А встречается только у мужчин с частотой 1 на 5000. Причина патологии заключается в нарушении биосинтеза фактора VIII. У больных гемофилией А содержание фактора VIII в крови составляет менее 1% нормы, по этой причине спонтанное кровотечение, как правило, приводит к смерти. В генах фактора VIII, расположенных на Х-хромосоме, у больных гемофилией А обнаруживается инверсия интрона F8A, которая и приводит к нарушению биосинтеза белка в клетках печени. Фактор VIII – это гликопротеин (МR 300), представляющий собой одну полипептидную цепь из 2332 аминокислотных остатков. Она содержит 25 участков гликозилирования, и содержание сахара может достигать 35%. Его пространственная структура установлена с помощью электронной криомикроскопии. Ген фактора VIIIa имеет размер ~186 т.п.н. и содержит 26 экзонов. Посттрансляционное гликозилирование особенно важно в В-домене белка, который под действием тромбина отщепляется, что и приводит к активации фактора VIII. Болезнь фон Виллебранда, встречающаяся с частотой 1 на 1000 среди мужчин и женщин, вызвана нарушениями биосинтеза фактора фон Виллебранда (vWF) на внутренней стенке кровеносных сосудов. Ген vWF находится в хромосоме 12. Фактор фон Виллебранда, как и фактор VIII, – гликопротеин большого размера со сложной структурной органи-
зацией. Около 100 молекул vWF связываются с молекулой фактора VIII, и образующийся комплекс vWF–VIII активирует систему факторов X/IXа, которая обеспечивает агрегацию тромбоцитов при образовании тромба. При гемофилии В, встречающейся только у мужчин с частотой 1 на 25 000, нарушен синтез фактора IX – гликопротеина с молекулярной массой 55 кДа. Наряду с фактором VIII фактор IX участвует в активации фактора X. Ген, кодирующий фактор IX, расположен на X-хромосоме (Xq27) и имеет размер ~34 т.п.н.
КЛОНИРОВАНИЕ. При клонировании факторов крови, впервые осуществленного в 1982 г. компаниями Genentech и Genetic Institutes, оказалось, что главное затруднение связано с очень низким содержанием мРНК (лишь 10–5 от всей мРНК в печени). Полную кДНК удалось выделить из клеток лимфомы методом «прогулки по геному», а затем была создана векторная система, включающая в себя элементы вируса SV40 и аденовируса. Такая система позволила экспрессировать факторы крови в CHO- и BHKклетках.
ПРОИЗВОДСТВО. Производство лекарственных препаратов, содержащих факторы крови, началось в 1964 г. Факторы VIII, IX и vWF получали криопреципитацией из крови доноров, а затем очищали методами иммунохроматографии. Однако при этом значительно возрастала степень риска заражения реципиента через кровь донора, так как, например, для обеспечения одного больного гемофилией А фактором VIII в течение года требовалась кровь нескольких тысяч доноров. В результате более 60% пациентов, которые использовали донорские факторы крови, приобрели инфекционные заболевания. По этой причине генно-инженерный метод получения факторов VIII
иIX, разработанный в 1992 г., имеет огромное значение. Из-за высокого уровня гликозилирования фактора VIII синтез его биологически активной формы возможен исключительно в животных клетках (CHO-
иBHK-клетках), где уровень экспрессии чрезвычайно низок и составляет микрограммы продукта на литр клеточной культуры. Объем его рынка составляет около 500 млн долл. США в год (2004 г.).
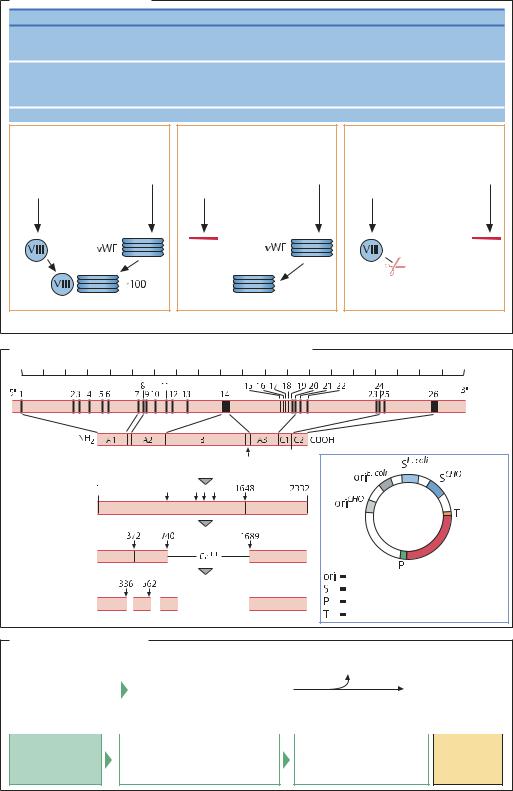
Тяжелые болезни крови |
|
|
|
|
|
|
||
|
|
Гемофилия А |
Болезнь фон Виллебранда |
Гемофилия В |
||||
Наследуемость |
|
1:5000, только мужчины |
1:1000, мужчины и женщины, |
1:25000, преиму- |
||||
|
|
|
|
как правило аутосомно- |
|
щественно мужчины |
||
|
|
|
|
доминантный тип наследования |
|
|
||
Клинические |
|
Мышечные и суставные |
Кровотечения из носа, значи- |
В детстве спонтанные |
||||
проявления |
|
кровотечения, крово- |
тельные потери крови в менстру- |
кровоизлияния |
||||
|
|
излияния в мозг |
альном цикле, продолжительные |
в суставы |
||||
|
|
|
|
кровотечения при порезах |
|
|
||
Хромосомный локус |
Xq28 |
|
12р12 |
|
Xq27 |
|||
Нормальный синтез |
Дефектный синтез |
Дефектный синтез при болезни |
||||||
комплекса фактора VIII |
при гемофилии А |
фон Виллебранда |
||||||
|
Хромосома 12: |
|
|
Хромосома 12: |
|
|
Хромосома 12: |
|
X-хромосома: |
|
ген фактора |
X-хромосома: |
ген фактора |
X-хромосома: |
ген фактора |
||
ген |
фон Виллебранда |
ген |
|
фон Виллебранда |
ген |
|
фон Виллебранда |
|
фактора VIII |
Внутренняя |
фактора VIII |
|
Внутренняя |
фактора VIII |
Внутренняя |
||
Клетки |
|
стенка |
Клетки |
|
стенка |
Клетки |
стенка |
|
кровеносного |
|
кровеносного |
кровеносного |
|||||
печени |
|
сосуда |
печени |
сосуда |
печени |
сосуда |
||
|
|
|
Блокирован |
|
|
|
|
Блокирован |
|
|
|
|
|
|
|
|
Быстрая |
|
|
|
|
|
|
|
|
деградация |
|
|
|
|
|
|
|
|
в отсутствие vWF |
Полноценный фактор VIII |
Только vWF |
|
|
|
||||
Комплекс фактора VIII состоит из фактора VIII и фактора фон Виллебранда (vWF) |
|
|
||||||
Фактор VIII: структура гена и экспрессирующий вектор |
|
|
|
|||||
0 |
|
50 |
100 |
|
150 |
|
200 т.п.н. |
|
|
|
|
|
|
|
|
|
Ген |
|
|
|
|
|
|
|
|
содер- |
|
|
|
|
|
|
|
|
жит 26 |
|
|
|
|
|
|
|
|
экзонов |
Одноцепо- |
|
|
|
|
|
|
|
|
чечный |
|
|
|
|
|
|
|
|
фактор VIII |
|
Связывание с фактором |
Связывание |
|
|
|
||
|
|
с фосфоли- |
|
|
|
|||
|
|
|
фон Виллебранда |
|
|
|
||
|
|
|
пидами |
|
|
|
||
|
|
|
|
|
|
|
|
|
Белок плазмы |
|
110–200 кДа |
|
80 кДа |
|
|
|
|
|
|
|
Тромбин |
|
|
|
|
|
Активация |
|
50 кДа 43 кДа |
|
|
73 кДа |
|
|
|
|
|
|
Активация белка С |
|
Точка начала репликации |
|||
|
|
|
|
Селективный маркер |
||||
|
|
|
|
|
|
|||
Инактивация |
45 кДа |
|
|
73 кДа |
Промотор (из генома аденовируса) |
|||
|
|
|
|
|
|
Терминатор |
|
|
Получение фактора VIII |
|
|
|
|
|
|
||
Из крови доноров |
|
|
Фактор фон Виллебранда |
|
|
|
|
||||
500 доноров |
|
|
|
Очистка |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|||
100 л плазмы, |
|
|
|
Осажение, многоступенчатая |
|
|
1 мг фактора VIII |
||||
1 кг криопреципитата |
|
|
|
иммунохроматография |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рекомбинантный фактор VIII |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Биореактор с культурой клеток |
|
Очистка |
|
|
Около 2 мг |
||
Рекомбинантные |
|
|
|
|
|
|
|
фактора VIII |
|||
200 ч, 35 °С, |
|
Осажение, многоступенчатая |
|||||||||
клетки CHO |
|
|
|
из 1 л клеточ- |
|||||||
|
|
|
|
сложная питательная среда |
|
иммунохроматография |
|
|
ной культуры |
||
129