Материал: Шмид Р. Наглядная биотехнология и генетическая инженерия
среда |
Микробиологическое выщелачивание руд и биокоррозия |
||||||||||
|
|
|
|
|
|
|
|
|
|
||
окружающая |
ВВЕДЕНИЕ. В США, Канаде, Австралии и Мексике для |
веденных местах, куда руда транспортируется. В дру- |
|||||||||
|
|||||||||||
|
выщелачивания бедных руд (то есть для извлечения |
гом способе используют отработанные шахты. Хоро- |
|||||||||
|
отдельных составляющих руды путем их растворе- |
шо разработан метод чанового бактериального выще- |
|||||||||
|
ния) используются тиобактерии. Около 25% всего |
лачивания. Его преимущество по сравнению с |
|||||||||
|
мирового объема меди, более 10% золота и 3% ко- |
другими способами заключается в высокой эффек- |
|||||||||
|
бальта и никеля добываются с помощью биовыщела- |
тивности извлечения ценных металлов и экологиче- |
|||||||||
и |
чивания. |
ской безопасности процесса. Изучается также метод |
|||||||||
МИКРОБИОЛОГИЯ И ФИЗИОЛОГИЯ ПРОЦЕССА. Тио- |
выщелачивания гетеротрофными микроорганизма- |
||||||||||
Биотехнология |
|||||||||||
бактерии осуществляют выщелачивание руд; эти хе- |
ми. В основе метода лежит секреция активных хела- |
||||||||||
|
|||||||||||
|
молитотрофные грамотрицательные палочки, как |
тирующих веществ (таких, как лимонная или глюко- |
|||||||||
|
правило, фиксируют СО2. Для получения энергии эти |
новая кислоты), например штаммами пеницилла, |
|||||||||
|
микроорганизмы окисляют восстановленные соеди- |
которым для роста требуются органические источни- |
|||||||||
|
нения серы, например сульфиды, в результате чего |
ки углерода. |
|
|
|
|
|
|
|||
|
образуется серная кислота. В отличие от Thiobacillus |
БИОКОРРОЗИЯ. В круговороте веществ в природе |
|||||||||
|
thiooxidans бактерии Т. ferroоxidans способны окис- |
один из важных процессов – анаэробное окисление |
|||||||||
|
лять не только восстановленные соединения серы, но |
металлического железа с образованием FeS (биокор- |
|||||||||
|
и растворимые соли Fe2+. Оба вида бактерий растут |
розия). Реакцию |
|
|
|
||||||
|
в кислой среде и устойчивы при рН 2. Сульфидные и |
|
|
|
2– |
|
+ 2H2O + 2Н+ → FeS + 3Fe(OH)2 |
||||
|
оксидные компоненты руды, такие как пирит (серный |
4Fe + SO4 |
|
||||||||
|
или железный колчедан, FeS2), халькозин (CuS2), |
осуществляют анаэробные микроорганизмы, способ- |
|||||||||
|
ковеллин (медный блеск, CuS), сфалерит (цинковая |
ные восстанавливать сульфат, например Desulfovib- |
|||||||||
|
обманка, ZnS), галенит (свинцовый блеск, PbS), мо- |
rio vulgaris. В анаэробных условиях железо также |
|||||||||
|
либденит (молибденовый блеск, MoS2), антимонит |
окисляется до Fe2+: |
|
|
|
||||||
|
(сурьмяный блеск, Sb2S3), сульфид кобальта (CoS) |
4Fe + 8H |
+ |
|
2+ |
+ 4H2 |
|||||
|
и уранинит (UO2) могут выщелачиваться посредст- |
|
→ 4Fe |
||||||||
|
Образующаяся в этом процессе водородная пленка |
||||||||||
|
вом тиобактерий. При прямом микробиологическом |
||||||||||
|
выщелачивании происходит непосредственный кон- |
защищает железо от |
дальнейшего разрушения. |
||||||||
|
такт между бактериями и сульфид-содержащим ми- |
В присутствии сульфата Desulfovibrio окисляет H2: |
|||||||||
|
нералом. Окисление до сульфата происходит в не- |
4H |
2 |
+ SO2– |
→ H S + 2H |
2 |
O + 2OH–, |
||||
|
сколько стадий согласно следующему суммарному |
|
|
4 |
|
2 |
|
|
|||
|
уравнению: |
что приводит к образованию нерастворимых сульфи- |
|||||||||
|
MS + 2O2 → MSO4 |
да железа и гидроксида железа: |
|||||||||
|
4Fe2+ + H2S + 2OH– + 4H2O → |
||||||||||
|
Непрямое бактериальное выщелачивание заключа- |
||||||||||
|
ется в химическом превращении сульфидсодержа- |
|
|
|
|
|
|
FeS + 3Fe(OH) + 6H+ |
|||
|
|
|
|
|
|
|
|
|
2 |
||
|
щих минералов в растворимые сульфаты и свобод- |
Биокоррозия существенно разрушает железные тру- |
|||||||||
|
ную серу: |
бы подземных коммуникаций. |
|
|
|||||||
|
MS + Fe2(SO4)3 → MSO4 + 2FeSO4 + S° |
|
|
|
|
|
|
|
|
|
|
|
Образующееся двухвалентное железо Fe2+ окисля- |
|
|
|
|
|
|
|
|
|
|
|
ется бактериями до Fe3+ и снова может участвовать |
|
|
|
|
|
|
|
|
|
|
|
в окислительном процессе в кислых условиях. При |
|
|
|
|
|
|
|
|
|
|
|
рН 2–3 микробное окисление Fe2+ происходит в |
|
|
|
|
|
|
|
|
|
|
|
105–106 раз эффективнее, чем химическое окисле- |
|
|
|
|
|
|
|
|
|
|
|
ние. На практике два описанных способа выщелачи- |
|
|
|
|
|
|
|
|
|
|
|
вания руд часто проводят одновременно, так как ру- |
|
|
|
|
|
|
|
|
|
|
|
ды имеют сложный состав. |
|
|
|
|
|
|
|
|
|
|
|
ТЕХНИЧЕСКИЕ ХАРАКТЕРИСТИКИ. Для процесса вы- |
|
|
|
|
|
|
|
|
|
|
|
щелачивания руд оптимальны следующие условия: |
|
|
|
|
|
|
|
|
|
|
|
руда подходящего состава с требуемым размером |
|
|
|
|
|
|
|
|
|
|
|
частиц, проведение реакций в кислых условиях и при |
|
|
|
|
|
|
|
|
|
|
|
температуре около 30 °С, интенсивная аэрация. На |
|
|
|
|
|
|
|
|
|
|
120 |
практике выщелачивание руды проводят in situ непо- |
|
|
|
|
|
|
|
|
|
|
средственно на рудном отвале или в специально от- |
|
|
|
|
|
|
|
|
|
||
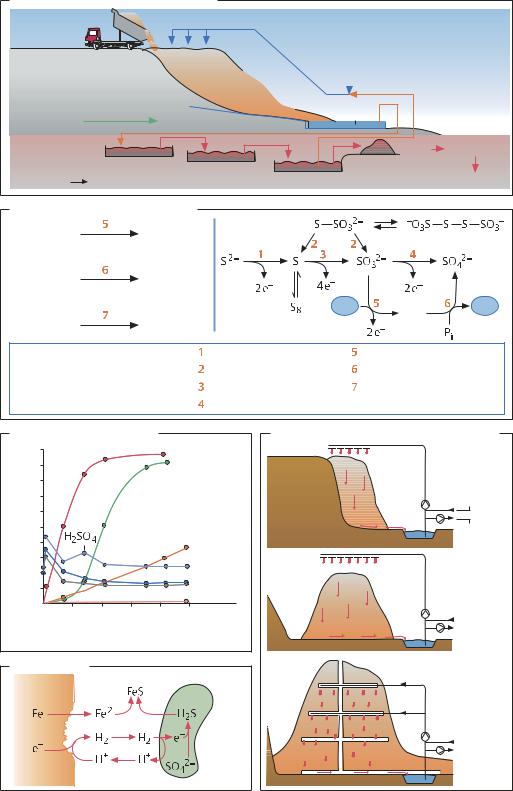
Биологическое выщелачивание руды |
|
|
|
||||||||
Выщелачивание |
|
Вскрыша |
|
|
|
|
|||||
рудного отвала |
|
|
|
|
|
|
Добавление воды |
|
|||
Нетронутый |
|
|
|
|
Выщела- |
|
Анализ, |
|
|||
породный массив |
|
|
|
|
|
контроль |
|
||||
|
|
|
|
чивание |
|
|
|||||
|
|
|
|
|
|
|
|
процесса |
|
||
|
|
|
|
|
|
|
|
Отвал, в который |
|
||
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
внесены микро- |
|
|
|
|
|
|
Thiobacillus |
|
|
|
организмы |
|
|
|
|
Сульфид меди |
ferrooxidans |
Сульфат меди |
Кислота |
|
|||||||
Плавка |
|
|
|
|
|
|
|
|
Высу- |
Расплавление |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
Железный шлам |
Осаждение |
|
шива- |
|
||||
|
|
|
|
ние |
|
||||||
|
Fe° + Cu2+ |
Cu+ + Fe2+ |
|
|
Медный шлам |
Электролиз |
|||||
|
|
|
|
|
|
||||||
Стадии биохимического процесса |
|
|
|
|
|||||||
SO32– + АМФ |
|
АФС + 2е– |
|
|
|
|
|||||
АФС + P |
i |
|
АДФ + SO2– |
|
|
|
|
||||
|
|
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
АМФ |
АФС |
АДФ |
2АДФ |
|
|
АМФ + АТФ |
|
|
|
|||||
|
|
|
|
|
|
||||||
|
АМФ – аденозинмонофосфат |
|
|
|
Сульфидоксидаза |
AФС-редуктаза |
|
||||
|
АДФ – аденозиндифосфат |
|
|
|
Тиосульфатгидролаза |
Сульфатаденилилтрансфераза |
|||||
|
АФС – аденозинфосфосульфат |
|
|
|
Серная оксидаза |
Аденилаткиназа |
|||||
|
|
|
|
|
|
|
|
Сульфитоксидаза |
|
|
|
Кинетика выщелачивания |
|
|
|
|
Варианты осуществления выщелачивания |
||||||
|
100 |
|
|
|
|
T. ferrooxidans |
а |
|
Выщелачивание |
||
|
90 |
|
|
|
|
T. ferrooxidans + |
|
|
рудного отвала |
||
|
80 |
|
|
|
|
T. thiooxidans |
|
|
|
||
% |
|
|
|
|
|
|
|
|
|
|
|
70 |
|
|
|
|
|
|
|
|
|
|
|
урана, |
|
|
|
|
|
|
|
|
|
Подача |
|
60 |
|
|
|
|
|
|
|
|
|
|
|
50 |
|
|
|
|
|
|
|
|
|
|
|
Экстракция |
|
|
|
|
|
|
|
|
|
Отвод |
|
40 |
|
|
|
|
|
T. thiooxidans |
|
|
|
||
30 |
|
|
|
|
|
|
|
Выщелачивание |
|||
|
|
|
|
|
|
|
б |
|
|||
20 |
|
|
|
|
|
|
|
|
|
складированного |
|
|
|
|
|
|
|
|
|
|
|
шлама |
|
|
10 |
|
|
|
|
|
Стерильные |
|
|
||
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
условия |
|
|
|
|
|
|
10 |
20 |
30 |
40 |
|
50 |
сут. |
|
|
|
Культуры в качалочных колбах, |
|
|
|
|
|
|
|
||||
5% урановой руды, зерна < 600 мм |
|
|
|
|
|
|
|||||
Биокоррозия |
|
|
|
|
|
|
в |
|
Выщелачивание |
||
Металлическое |
|
|
|
|
|
|
|
|
in situ |
||
|
|
|
|
|
|
|
|
|
|||
железо |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Desulfo- |
|
|
|
|
|
|
|
|
|
|
|
vibrio |
|
|
|
121
медицине |
Инсулин |
|
рующий уровень глюкозы крови. При лечении сахар- |
||
|
ВВЕДЕНИЕ. Инсулин – это пептидный гормон, регули- |
|
в |
ного диабета (Diabetes mellitus) инсулин незаменим. |
|
Биотехнология |
||
До 1985 г. инсулин получали из отходов мясной про- |
||
|
||
|
мышленности (поджелудочная железа крупного рога- |
|
|
того скота и свиней). Современная технология произ- |
|
|
водства инсулина основана на использовании |
|
|
рекомбинантных штаммов Escherichia coli и Saccharo- |
|
|
myces cerevisiae. Объем рынка инсулина составляет |
|
|
около 8 тонн в год и оценивается в 5 млрд долларов |
|
|
США. |
|
|
DIABETES MELLITUS (сахарный диабет). Это заболева- |
|
|
ние вызвано нарушениями образования или секреции |
|
|
инсулина в кровь. Более распространен диабет II типа, |
|
|
при котором лечение заключается в дополнительной |
|
|
стимуляции синтеза гормона в организме. При диабе- |
|
|
те I типа образование собственного инсулина наруше- |
|
|
но из-за генетического дефекта, вирусной инфекции |
|
|
или аутоиммунного заболевания, и для поддержания |
|
|
нормального уровня глюкозы крови пациенту необхо- |
|
|
димы регулярные инъекции инсулина. В мире от диа- |
|
|
бета страдают 170 млн человек, из которых 60 млн |
|
|
больны диабетом I типа (в Германии ~400 000 паци- |
|
|
ентов с диабетом I типа). Более 2% населения инду- |
|
|
стриальных регионов Земли являются диабетиками II |
|
|
типа (в Германии – 2,4 млн). |
|
|
БИОСИНТЕЗ ИНСУЛИНА. Синтез препроинсулина про- |
|
|
исходит в β-клетках поджелудочной железы живот- |
|
|
ных. Образовавшийся в результате внутриклеточного |
|
|
процессинга проинсулин запасается в аппарате Голь- |
|
|
джи. При недостатке глюкозы в крови проинсулин |
|
|
расщепляется мембранными протеазами на три поли- |
|
|
пептидные цепи – А, В и С. Цепи А и В (21 и |
|
|
30 аминокислотных остатков соответственно) сближа- |
|
|
ются и соединяются посредством трех дисульфидных |
|
|
мостиков, а центральная С-цепь (31 аминокислотный |
|
|
остаток) под действием ферментов отщепляется. Так |
|
|
образуется активная форма инсулина. |
|
|
ПОЛУЧЕНИЕ ИНСУЛИНА. Возможность использова- |
|
|
ния инсулина при терапии диабета была продемонст- |
|
|
рирована в 1922 г. Традиционная методика получе- |
|
|
ния инсулина заключалась в экстракции бутанолом |
|
|
из поджелудочной железы крупного рогатого скота |
|
|
или свиней, последующей кристаллизации цинксо- |
|
|
держащей формы инсулина с дальнейшей очисткой |
|
|
гормона методами хроматографии. Количества инсу- |
|
|
лина, полученного из поджелудочной железы одной |
|
|
свиньи, хватает больному диабетом на 3 дня, а инсу- |
|
|
лина из одной коровы – на 10 дней. Однако свиной и |
|
|
коровий инсулин по аминокислотному составу отли- |
|
|
чаются от инсулина человека (в положениях 1 и 2 со- |
|
|
ответственно), поэтому при длительном приеме чу- |
|
122 |
жеродного инсулина у больных может развиваться |
|
иммунная реакция. Метод химического синтеза |
инсулина, полностью аналогичного человеческому, был предложен еще в 1964 г., однако осуществление в промышленном масштабе такого сложного и дорогостоящего синтеза оказалось экономически нецелесообразным. В 1975 г. был разработан метод получения из поджелудочной свиньи инсулина, полностью идентичного инсулину человеку. Для этого происходит ферментативное замещение остатка Ala30 в В-цепи на остаток Thr30 с помощью иммобилизованной карбоксипептидазы Y. Промышленное получение инсулина методами генетической инженерии стало возможным с 1985 г. В качестве клеток-хозяев, продуцирующих инсулин, были выбраны клетки Escherichia coli К12. Частота встречаемости кодонов аминокислот в клетках человека и бактерии значительно различается, поэтому, несмотря на то что кДНК препроинсулина можно выделить из культуры β-клеток человека (она составляет 75% фракции суммарной мРНК этих клеток), для создания экспрессирующего вектора более целесообразно оказалось получать кДНК методом химического синтеза. В ранних методах синтеза А- и В-цепи экспрессировали раздельно, очищали, а затем после химического окисления цистеина и образования дисульфидных мостиков получали активный инсулин. В современном производстве проинсулин в клетках Escherichia coli синтезируется в виде белка, слитого с триптофансинтазой, которую впоследствии отщепляют протеолизом. Такой проинсулинсодержащий слитый белок составляет до 40% клеточной массы оптимизированных штаммов-продуцентов, таким образом из 40 м3 клеточной культуры после очистки методом обращенно-фазовой хроматографии удается получить около 100 г чистого инсулина. Разработан способ получения укороченного, так называемого «мини-проин- сулина» в клетках Saccharomyces cerevisiae.
НОВЫЕ ТИПЫ ИНСУЛИНА. Было показано, что препарат инсулина человека, содержащего в В-цепи Lys28Pro29 вместо Pro28Lys29 значительно быстрее усваивается организмом, что помогает больным диабетом планировать свое питание. Такой лизпро-инсу- лин, как и обычную форму, получают в рекомбинантном штамме E. coli. В настоящее время изучаются возможности терапевтического применения других производных инсулина: Pro28Asp (инсулин аспарт – короткого действия, разрешен к применению), Asn3LysLys29Glu (В-цепь, инсулин глулизин – аналог инсулина быстрого действия, фаза III), Thr30Arg31Arg (В-цепь) Asn21Gly (А-цепь, инсулин гларгин – длительного действия), а также инсулина, содержащего Thr30delLys29, ацетилированного жирной кислотой (препарат «Инсулин Детемир»).
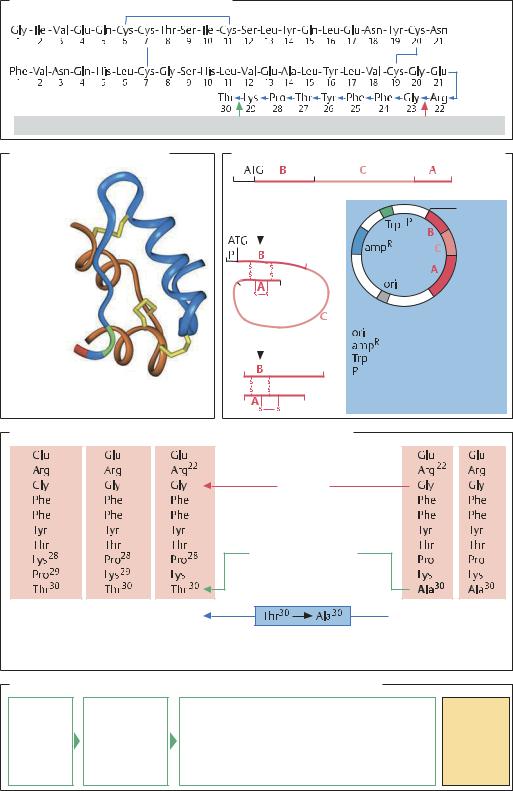
Первичная структура инсулина человека |
|
|
||
А-цепь |
|
|
|
|
В-цепь |
|
|
|
|
С-концевой Thr отщепляется карбоксипептидазой Y, а октапептид – трипсином |
||||
Пространственная структура |
Биосинтез инсулина и экспрессирующая плазмида |
|||
молекулы инсулина |
|
|
|
|
Структура инсулина |
Препосле- |
Препроинсулин |
Проинсулин = ВСА |
|
дователь- |
|
|
||
свиньи была |
|
ATG |
||
ность |
|
|||
установлена путем |
|
|||
Спонтанное |
кодирует |
|||
рентгено- |
||||
Met |
||||
стркутурного |
расщепление |
|
||
анализа моно- |
|
|
|
|
кристалла |
|
|
|
|
с разрешением |
|
|
|
|
0,18 нм (9INS) |
|
|
|
|
Коричневым |
Протео- |
Точка начала репликации |
||
цветом |
литическое |
Селективный маркер |
||
показана |
||||
расщепление |
Промотор |
|||
А-цепь, |
|
|
||
голубым – В-цепь, |
|
|
Препоследовательность Р |
|
желтым – дисульфидные мостики, |
|
|
с кодоном ATG |
|
красным – замена Ala30 (инсулин свиньи) |
|
Инсулин |
для расщепления |
|
на Thr30 (инсулин человека) |
|
с помощью BrCN |
||
|
|
|||
Структура инсулина из различных источников (С-конец В-цепи) |
|
|||
|
|
|
Трипсин |
|
|
|
|
Заменен С-концевой |
|
|
|
|
октапептид |
|
|
|
|
Карбоксипептидаза Y |
|
|
|
|
Заменен С-концевой остаток |
|
|
|
|
аланина на треонин |
|
Замена Lys |
Рекомбинант- |
Природный |
Инсулин |
Инсулин |
на Pro – |
ный инсулин |
инсулин |
свиньи |
крупного |
инсулин |
человека, |
человека |
|
рогатого |
с повышенной |
полученный |
|
|
скота* |
биологической |
в клетках |
|
|
|
активностью |
E. coli K12 |
|
* Дополнительные замены двух аминокислотных остатков в А-цепи |
|
Получение рекомбинантного инсулина человека в клетках E. coli K12 |
|
|||
Биореактор |
|
Выделение |
|
|
Обработка |
|
|
Объем 40 м3, |
Выделение телец |
1. |
Расщепление слитого белка по остатку метионина |
~ 2,5 г |
|||
30 ч, 37 °C, |
включения, |
|
с помощью CNBr |
инсулина |
|||
|
человека |
||||||
источник |
удаление |
2. |
Получение S-сульфопроизводных |
||||
на 1 м3 |
|||||||
углерода |
клеточных |
3. |
Восстановление S-сульфоцистеина до цистеина |
||||
за 30 ч |
|||||||
и источник |
фрагментов |
4. Образование дисульфидных мостиков (O2, рН 10,6) |
|||||
|
|||||||
азота |
|
|
5. |
Трипсин/карбоксипептидаза В, удаление С-пептида |
|
||
123
медицине |
Гормон роста и другие гормоны |
|
пин; ГР; англ. Н или GF), как и инсулин – один из са- |
||
|
ВВЕДЕНИЕ. Гормон роста (фактор роста, соматотро- |
|
в |
мых важных гормонов, получаемых методами гене- |
|
Биотехнология |
||
тической инженерии. В организме синтез этого |
||
|
||
|
гормона происходит в передней доле гипофиза. Гор- |
|
|
мон роста принимает участие в регуляции многих об- |
|
|
менных процессов. В основе его действия лежат два |
|
|
механизма: при полноценном питании гормон роста |
|
|
ингибирует синтез жиров, а неизрасходованная энер- |
|
|
гия используется для белкового синтеза, например, в |
|
|
молочных железах. Этим свойством пользуются в |
|
|
животноводстве: добавление гормона роста стимули- |
|
|
рует лактацию, а также позволяет получать менее |
|
|
жирное мясо, обогащенное белком. Другой функцио- |
|
|
нальный эффект гормона заключается в стимуляции |
|
|
роста в результате действия инсулиноподобного фа- |
|
|
ктора роста IGF-1, синтезирующегося в клетках пече- |
|
|
ни. Этот фактор индуцирует клеточное деление в |
|
|
большинстве тканей организма. |
|
|
ГОРМОН РОСТА ЧЕЛОВЕКА – полипептид, состоящий |
|
|
из 191 аминокислотного остатка, имеет два дисуль- |
|
|
фидных мостика. В 0,1% случаев причина наруше- |
|
|
ний роста – пониженная секреция гормона роста в |
|
|
гипофизе; причем нормальный рост удается восста- |
|
|
новить при парентеральном введении гормона. Бо- |
|
|
лее частой причиной нарушений роста являются де- |
|
|
фектные рецепторы гормонов роста. Избыточное |
|
|
образование гормона роста в детском и переходном |
|
|
возрасте приводит к гигантизму, а у взрослых его |
|
|
избыток вызывает акромегалию – непропорцио- |
|
|
нальное разрастание пальцев, носа и ушей. Объем |
|
|
рынка гормона роста человека составляет около |
|
|
1 млрд долл. США (2004 г.). |
|
|
ЖИВОТНЫЙ СОМАТОТРОПИН. Бычий гормон роста |
|
|
(bGF) отличается от гормона роста человека по |
|
|
67 аминокислотным остаткам. С 1990 г. в США и |
|
|
многих других странах, за исключением Японии и |
|
|
стран ЕС, бычий гормон роста используется в живот- |
|
|
новодстве для стимуляции образования молока у ко- |
|
|
ров. Свиной гормон роста применяют при откорме |
|
|
свиней для увеличения мышечной массы, а не жира. |
|
|
Усиление лактации и наращивание мышечной массы |
|
|
происходит в результате того, что гормон роста инги- |
|
|
бирует синтез жиров, и неизрасходованная энергия |
|
|
используется для синтеза мышечных белков или мо- |
|
|
лочного белка. К настоящему времени нет данных, |
|
|
какое побочное биологическое действие может ока- |
|
|
зать свиной и бычий соматотропин на человека, в то |
|
|
время как действие гормона роста человека на других |
|
|
млекопитающих считается доказанным. Вероятность |
|
|
биологического воздействия гормона роста, содержа- |
|
|
щегося в мясной гастрономии, на человека очень ма- |
|
124 |
ла, так как в пищеварительном тракте белки инакти- |
|
вируются в результате протеолиза и не поступают в |
ткани. В результате генно-инженерных манипуляций был получен трансгенный лосось, у которого гормон роста находится под сильным промотором anti-freeze белка. Такой лосось в 3–10 раз больше по размеру обычных экземпляров этой рыбы. Благодаря строгой изоляции, а также стерильности выведенного лосося риски экологических последствий такого эксперимента невысоки.
ФЕРМЕНТАЦИЯ И ПОЛУЧЕНИЕ РЕКОМБИНАНТНОГО БЕЛКА. До развития методов генетической инженерии единственным источником гормона роста человека был гипофиз, поэтому гормон был доступен в очень небольших количествах и в недостаточно чистом виде. С 1984 г. началось производство гормона роста человека методом ферментации с использованием клеток Escherichia coli. Разработка системы клонирования оказалась очень сложной задачей, так как и сам гормон, и кодирующая его мРНК синтезируются в организме в очень малом количестве. Кроме того, рестрикционный анализ полученной кДНК выявил всего один сайт узнавания рестриктазой. Проблема была решена, когда удалось получить штамм E. coli К12, который мог нарабатывать «полусинтетический» гормон роста человека. Фрагмент ДНК, кодирующий первые 24 аминокислоты, был синтезирован химически, и непосредственно за стартовым кодоном был введен триплет, кодирующий метионин. Оставшийся фрагмент, содержащий аминокислотные остатки 25–191, был получен при синтезе кДНК на матрице мРНК из клеток гипофиза человека. Таким образом, эти бактерии создают гормон роста, идентичный гипофизарному, но содержащий дополнительный остаток метионина. Эта замена могла приводить к возникновению иммунных реакций. Современные методы генетической инженерии позволяют получать рекомбинантный гормон роста человека, полностью идентичный природному. Перед использованием полученные гормоны обязательно подвергаются хроматографической очистке.
ДРУГИЕ РЕКОМБИНАНТНЫЕ ГОРМОНЫ. В настоящее время клонированы гены многих гормонов человека, и исследуется возможность их применения в медицине и сельском хозяйстве. С появлением рекомбинантных гормонов открываются новые возможности в терапии многих заболеваний, например применение паратгормона для лечения остеопороза. Фолликулостимулирующий гормон человека (ФГС, или англ. FSH) применяется при диагностике бесплодия, от которого страдают 50–80 млн человек. Объем рынка этого рекомбинантного гетеродимерного гликопротеина, получаемого в культуре клеток CHO, составляет 600 млн долл. США.