Материал: Шандра О.А. Нормальна фізіологія. Вибрані лекції _ навч. посіб. _ О.А. Шандра, Н.В. Общіна _ О._ОГМУ, 2005. - 322 с
ся тільки незначним скороченням м’яза. Тривалий час вважалося, що при тонічному скороченні не підвищується обмін речовин у м’язі. Встановлено, що при тонічному скороченні втрачається дуже мало енергії. Якби м’язи стінок кров’яних судин знаходилися в тетанічному скороченні, необхідно було б затрачувати весь добовий харчовий раціон. Тільки тому, що вони знаходяться в стані тонічного скорочення, відбувається економія енергії. В процесі еволюції там, де необхідне тривале скорочення, відбувається тонічне скорочення, а там, де необхідне сильніше, але періодичне скорочення, відбувається тетанічне скорочення.
При тетанічному скороченні швидко розвивається втома, при тонічному скороченні втома не настає.
4. Контрактура — це тривале скорочення неритмічної природи, патологічне, стан зворотного стаціонарного скорочення, що не поширюється, це скорочення відрізняється від тетанусу відсутністю поширення ПД. При цьому відбувається тривала локальна деполяризація м’я- зової мембрани. Наприклад, при викликаній за допомогою кофеїну контрактурі МП може бути близьким до рівня ПД.
Контрактура — це скорочення, яке знаходиться на межі з патологією та виникає при ненормальних умовах. Це тривале скорочення, яке не поширюється, неритмічної природи, при якому м’яз довго не повертається до нормальної довжини і виникає за несприятливих умов. Зустрічається тоді, коли на м’яз діє велике подразнення, при тривалій роботі м’яза, наприклад, контрактура від втоми, контрактура від дії хімічних речовин, скажімо, підвищення концентрації іонів К+, від дії нікотину (нікотинова контрактура), від дії кислот, кофеїну, хініну, при різних захворюваннях. Наприклад, якщо у людини внаслідок поранення було тривале вимушене положення, розвивається контрактура.
Механізм скорочення
Будова м’яза. Як відомо, структурною одиницею скелетних м’язів є м’язове волокно (діаметр від 10 до 100 мікрон, довжина від кількох міліметрів до кількох сантиметрів). Скорочувальним апаратом м’язового волокна є міофібрили — тонкі нитки діаметром 0,5–2 мкм, довжина відповідає довжині м’язового волокна. Завдяки скороченню міофібрил відбувається скорочення м’язового волокна, а отже і рух.
Міофібрили складаються із товстих і тонких міониток, утворених скорочувальними білками — актином і міозином. Один грам тканини скелетного м’яза становить близько 100 мг скорочувальних білків
— актину (молекулярна маса 42 000) та міозину (мол. маса — 500 000, рис. 11). Теорія ковзаючих ниток, розроблена Хакслі та Ходжкіним,
39
Саркомер А-смуга
1 |
|
|
Z- |
Товсте |
Тонке |
волокно |
||
лінія |
волокно |
|
3 |
М-лінія |
|
Актин |
|
Міозин |
|
ІІ |
|
|
|
СР |
|
|
СР |
|
|
|
|
Са++ |
|
Са++ |
А |
|
|
|
|
|
|
|
М |
|
|
|
ГММ |
Са++ |
а |
Са++ |
|
|
|
|
|
Са++ |
|
|
Са++ |
|
|
|
М |
Са++ |
|
|
Са++ |
б |
|
|
|
Са++ |
|
|
Са++ |
|
|
|
М |
Са++ Са++
в
І
Актин Міозин Актин
2
Z-лінія |
У розслаб- Z-лінія |
У скороче- |
|
леному |
ному стані |
|
стані |
|
4 |
Тропоміозин |
Тропонін |
|
|
Актин |
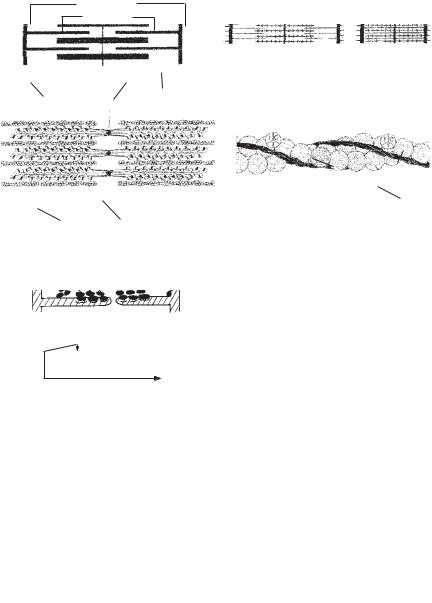
Рис. 11. І — Будова м’язового волокна і механізм скорочення (за В. Ганон «Фізіологія людини», Львів, 2002):
1 — взаємне розташування тонких (актинових) і товстих (міозинових) протофібрил у скелетному м’язі; 2 — ковзання актинових протофібрил по міозинових під час скорочення, Z — лінії наближаються; 3 — детальніша схема взаємодії між актином і міозином, М — лінії (посередині саркомера) змінюють полярність; 4 — схематичне зображення взаємного розташування актину, тропоміозину та трьох субодиниць протоніну (і, С, Т).
ІІ — Саркомер у розслабленому стані(а), в процесі підготовки до скорочення (б) і в стані скорочення (в):
СР — саркоплазматичний ретикулум; Са++ — іони кальцію, що запускають процес скорочення; А — актинові фібрили; М — міозинові фібрили; ГММ — головки містків міозину
40
пояснює механізм взаємодії між цими білками під час елементарного акту м’язового скорочення. Перегородки (пластинки) розділяють міофібрили на кілька компартментів довжиною приблизно 2,5 мкм, які називаються саркомерами. Світловий мікроскоп виявляє в саркомері світлі та темні смужки і диски, які правильно чергуються. Згідно з теорією Хакслі та Ходжкіна (1954), ця поперечна смугастість міофібрил зумовлена особливою регулярною організацією ниток актину і міозину. В середині кожного саркомера розташовані кілька тисяч товстих ниток міозину, кожна діаметром приблизно по 10 нм (нанометр — міліардна частина мікрона 1 (Г9 мк), на обох кінцях саркомера знаходиться близько 2000 тонких (товщиною 5 нм) ниток актину, прикріплених до 2 пластинок, подібно до щетинок у щітці. Пучок ниток міозину довжиною 1,6 мкм у середині саркомера виглядає в світловому мікроскопі як темна смужка, завдяки властивості подвійного променезаломлення в поляризованому світлі (тобто анізотропії), вони називаються А-диском. По обидві сторони від А-диска знаходяться ділянки, які мають тільки тонкі нитки і тому є світлими, це ізотропні І-диски, які тягнуться до Z-пластинок. Завдяки такому періодичному чергуванню світлих та темних смуг у саркомерах, що безкінечно повторюються, міофібрили волокон серцевого та скелетного м’язів мають вигляд поперечносмугастих. У м’язі, який перебуває в спокої, кінці товстих та тонких ниток лише незначно перекриваються на межі між А- і І-дисками.
М’яз укорочується внаслідок скорочення багатьох саркомерів, сполучених послідовно в міофібрилах. При укороченні тонкі актинові нитки ковзають уздовж товстих міозинових ниток, рухаючись між ними до середини пучка та саркомера. Під час ковзання самі нитки актину та міозину не укорочуються. Це основне положення теорії ковзаючих ниток. Довжина ниток не змінюється і при розтягненні м’язів. Замість цього пучки тонких ниток, ковзаючи, виходять із проміжків між товстими нитками, так що ступінь їх перекриття зменшується. Яким же чином відбувається «різнонаправлене ковзання» актинових ниток у сусідніх половинках саркомера?
Міозинові нитки мають поперечні виступи довжиною близько 20 нм, з головками приблизно із 150 молекул міозину; вони відходять від нитки біполярно (див. рис. 11, ІІ). У стані спокою місток не може приєднатися до актину, бо між ними розміщують білки тропонін і тропоміозин, які блокують місце приєднання. При підвищенні концентрації іонів Са2+ та у присутності АТФ тропонін змінює свою конфігурацію і відсовує молекулу тропоміозину, створюючи умови для з’єднання головки містка з актином. Це супроводжується зміною положення головки і переміщенням нитки актину з подальшим розриванням містка
(див. рис. 11, ІІ).
41
Таким чином, під час скорочення кожна головка міозину (або поперечний місток) може зв’язувати міозинову нитку з сусідньою — актиновою. Нахили головок утворюють об’єднане зусилля і відбувається «гребок», який переміщує актинову нитку до середини саркомера. Біполярна організація молекул міозину в двох половинах саркомера вже забезпечує можливість ковзання актинових ниток у протилежному напрямку в лівій та правій половині саркомера. При ізотонічному скороченні м’яза жаби саркомери укорочуються на 1 мкм, тобто на 50 % довжини за 1/10 с. Для цього поперечні містки повинні виконувати щойно описані гребні рухи не один раз за такий проміжок часу, а 50 разів. Поперечні містки відіграють роль свого роду «зубчастого колеса», яке протягує одну групу ниток по іншій.
Тільки ритмічне від’єднання і прикріплення головок міозину зможе «гребти», або тягнути актинову нитку до середини саркомера так, як група людей тягне довгу мотузку, перебираючи її руками. Коли принцип «витягування мотузки» діє для багатьох послідовних саркомерів, молекулярні рухи поперечних містків, які повторюються, призводять до макроскопічного руху. Коли м’яз розслаблюється, головки міозину відходять від актинових ниток. Подовження м’яза під час розслаблення є пасивним. Такі основні положення теорії ковзаючих ниток.
М’язи — це механізм, який перетворює хімічну енергію безпосередньо в механічну, тобто роботу в теплоту. Яким же чином м’яз перетворює хімічну енергію в механічну? Сьогодні це найактуальніше питання в сучасних молекулярних судженнях.
Прямим, безпосереднім джерелом енергії для скорочення м’язів є АТФ. Доведено, що під час м’язового скорочення відбувається гідролітичне розщеплення АТФ до аденозиндифосфату і фосфату. Всі інші реакції, що забезпечують енергію в м’язі (наприклад, аеробне та анаеробне розщеплення вуглеводів та розпад креатинфосфату), не можуть розглядатися як прямі джерела енергії для м’язового механізму. Вони служать тільки для постійного відновлення справжнього пального для цього механізму — АТФ. У скелетних м’язах вміст АТФ невеликий, достатній на 10 поодиноких скорочень. Тому потрібний постійний ресинтез АТФ. Існує 3 шляхи:
1)ресинтез АТФ за рахунок розщеплення креатинфосфату (КФ). Ця реакція відбувається дуже швидко, тому за кілька секунд можна виконати велику роботу (наприклад, спринтер);
2)гліколітичний шлях ресинтезу, який пов’язаний з анаеробним розщепленням глюкози до молочної кислоти, внаслідок чого утворюються 2 молі АТФ на 1 моль глюкози;
3)аеробне окиснення глюкози та ліпідів у циклі Кребса відбувається в мітохондріях. У середньому на 1 моль глюкози утворюється близь-
42
ко 38 молів АТФ, а внаслідок окиснення 1 моля жирної кислоти — близько 128 молів АТФ.
Під впливом АТФ-ази — ферменту міозину — АТФ гідролітично розщеплюється. Цей процес активується актином. АТФ — єдина речовина в м’язі (винятком є рідкі нуклеозидтрифосфати), яка може прямо утилізуватися скорочувальними білками. Механізм, за допомогою якого донор енергії АТФ забезпечує переміщення поперечних містків, сьогодні інтенсивно вивчається.
Можливо, молекула АТФ зв’язується з поперечними містками після завершення його «гребного» руху. І це забезпечує енергію для розподілу, розриву компонентів, які беруть участь у реакції, — актину та міозину. Майже одразу ж після цього головки міозину відокремлюються від актину. Потім АТФ розщеплюється до АДФ і фосфату проміжним утворенням комплексу фермент-продукт. Розщеплення є обов’язковою умовою для подальшого прикріплення поперечного містка до актину з вивільненням АДФ і фосфату та гребним рухом містка. Коли рух містка завершується, з ним зв’язується нова молекула АТФ, і починається новий цикл. Циклічна активність поперечних містків, тобто ритмічне прикріплення та від’єднання містків, що забезпечує м’язове скорочення, можлива тільки доти, доки продовжується гідроліз АТФ, тобто доки відбувається активація АТФ-ази. Якщо розщеплення АТФ блоковане, містки не можуть повторно прикріплюватися, сила м’язового волокна падає до нуля, і м’яз розслаблюється. Після смерті вміст АТФ у м’язових клітинах знижується; коли він переходить критичний рівень, поперечні містки виявляються стійко прикріпленими до актинової нитки (поки не відбудеться аутоліз). У такому стані актинові та міозинові нитки дуже сильно сполучені одна з одною — м’яз перебуває в стані трупного задубіння.
Роль кальцію в механізмі м’язового скорочення
Збудження м’язів часто відбувається при проходженні ПД від іннервуючих мотонейронів через нервово-м’язові синапси. Передача сигналів про скорочення від збудженої клітинної мембрани до міофібрил у глибині клітини називається електромеханічним спряженням. Воно складається з кількох послідовних процесів, ключову роль у яких відіграють іони Са2+.
Механізм дії Са2+: внутрішньоклітинна ін’єкція кальцію викликає скорочення м’язових волокон. Однак інтактні м’язові волокна не є потрібним об’єктом для демонстрації прямого впливу кальцію на міофібрили. Більше підходять для цієї мети волокна без або з порушеною клітинною мембраною. Для одержання таких волокон або «обдирають» мембрану механічним шляхом, або діють детергентами; такі демембра-
43