Материал: РЕШЕННОЕ ЦТ по Биохимии
Г. Должны поступать в организм с пищей |
|
Д. Синтезируются из других соединений |
|
7. Для реакции трансаминирования аминокислот необходим кофермент: |
Г |
А. FAD |
|
Б. Биотин |
|
В. ТДФ |
|
Г. Пиридоксальфосфат |
|
Д. NAD+ |
|
8. К нарушению трансаминирования приведет недостаток витамина: |
Г |
А. Рибофлавина |
|
Б. Никотинамида |
|
В. Биотина |
|
Г. Пиридоксина |
|
Д. Тиамина |
|
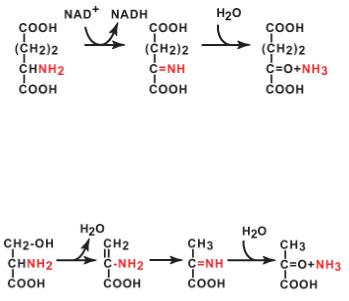
9. прямому окислительному дезаминированию подвергается |
В |
А. Аланин |
|
Б. Фенилаланин |
|
В. Глутамат |
|
Г. Треонин |
|
Д. Глицин |
|
10. в прямом окислительном дезаминировании принимает участие: |
Г |
А. Серинтреониндегидратаза |
|
Б. Карбамоилфосфатсинтетаза |
|
В. Глутаматдекарбоксилаза |
|
Г. Глутаматдегидрогеназа |
|
Д. Глутаминсинтетаза |
|
11. Для прямого окислительного дезаминирования необходим |
В |
кофермент: |
|
А. FAD |
|
Б. Пиридоксальфосфат |
|
В. NAD+ |
|
Г. Тиаминдифосфат |
|
Д. Биотин |
|
12. Данную реакцию катализирует фермент: |
Б |
А. Сериндегидратаза |
|
Б. Глутаматдегидрогеназа |
|
В. Треониндегидратаза |
|
Г. Гистидаза |
|
Д. Аланинаминотрансфераза |
|
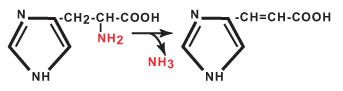
13. Приведенную реакцию катализирует фермент: |
Б |
А. Глутаматдегидрогеназа |
|
Б. Сериндегидратаза |
|
В. Треониндегидратаза |
|
Г. Гистидаза |
|
Д. Аспартатаминотрансфераза |
|
|
|
14. Приведенную реакцию катализирует фермент: |
Г |
А. Сериндегидратаза |
|
Б. Глутаматдегидрогеназа |
|
В. Треониндегидратаза |
|
Г. Гистидаза |
|
Д. Аланинаминотрансфераза |
|
15. При ацидозе в почках активируется фермент: |
Б |
А. Аргиназа |
|
Б. Глутаминаза |
|
В. Карбамоилфосфатсинтетаза |
|
Г. Глутаминсинтетаза |
|
Д. Глутаматдегидрогеназа |
|
16. Основное количество аммиака в почках образуется: |
Д |
А. При трансаминированиии аминокислот |
|
Б. Из солей аммония |
|
В. При катаболизме нуклеотидов |
|
Г. При инактивации биогенных аминов |
|
Д. Из глутамина |
|
17. Главный путь обезвреживания аммиака в печени: |
Б |
А. Синтез аспарагина |
|
Б. Синтез карбамоилфосфата |
|
В. Восстановительное аминирование α-кетоглутарата |
|
Г. Образование солей аммония |
|
Д. Образование аланина из пирувата |
|
18. Основная реакция обезвреживания аммиака в печени: |
В |
А. Аммиак + Глутамат + АТФ → Глутамин + АДФ + Н3РО4 |
|
Б. α-Кетоглутарат + Аммиак + NADН → Глутамат + NAD+ + Н2О |
|
В. Аммиак + 2АТФ + СО2 → Карбамоилфосфат +2АДФ + H3PO4 |
|
Г. Аммиак → Хлорид аммония |
|
Д. Аммиак + Аспартат → Аспарагин |
|
19. Азот аминокислот в составе аланина транспортируется, в основном, |
Г |
в: |
|
А. Кишечник |
|
Б. Почки |
|
В. Мозг |
|
Г. Печень |
|
Д. Мышцы |
|
20. Азот аминокислот транспортируется в кровь из печени в составе: |
Г |
А. Аланина |
|
Б. Глутамата |
|
В. Аспартата |
|
Г. Мочевины |
|
Д. Аммонийных солей |
|
21. Возврат фумарата в орнитиновый цикл происходит с помощью |
В |
реакций: |
|
А. Фумарат → Малат → Оксалоацетат → Глутамат |
|
Б. Фумарат → Сукцинат → α-кетоглутарат → Глутамат |
|
В. Фумарат → Малат → Оксалоацетат → Аспартат |
|
Г. Фумарат → Малат → оксалоацетат → пируват |
|
Д. Фумарат → аргинин → мочевина |
|
22. Наследственное заболевание цитруллинемия обусловлена: |
Д |
А. Снижением скорости синтеза аргинина |
|
Б. Повышением концентрации аммиака в крови |
|
В. Повышением концентрации цитруллина в крови |
|
Г. Нарушением реакции трансаминирования аминокислот |
|
Д. Дефектом аргининосукцинатсинтетазы |
|
23. при дефекте фермента аргининосукцинатлиазы в моче повышается |
Г |
содержание: |
|
А. Цитруллина |
|
Б. Аргинина |
|
В. Глутамина |
|
Г. Аргининосукцината |
|
Д. Карбамоилфосфата |
|
24. При наследственных гипераммониемиях в крови уменьшается |
Г |
концентрация: |
|
А. Аспартата |
|
Б. Аланина |
|
В. Аммиака |
|
Г. Мочевины |
|
Д. Глутамина |
|
25. Предшественником серина является: |
Д |
А. Фумарат |
|
Б. Ацетил-КоА |
|
В. α-кетоглутарат |
|
Г. Оксалоацетат |
|
Д. 3-фосфоглицерат |
|
26. Обмен глицина связан с использованием: |
В |
А. Тиамина |
|
Б. биотина |
|
В. фолиевой кислоты |
|
Г. NAD+ |
|
Д. пиридоксина |
|
27. Для регенерации метионина необходим: |
Б |
А. метилен-Н4-фолат |
|
Б. метил-Н4-фолат |
|
В. формил-Н4-фолат |
|
Г. Н4-фолат |
|
Д. метенил-Н4-фолат |
|
28. Выберите недостающий в реакции компонент: |
В |
метионин + ? → S-аденозилметионин |
|
А. АДФ |
|
Б. цАМФ |
|
В. АТФ |
|
Г. NAD+ |
|
Д. FAD |
|
29. в норме при катаболизме фенилаланина образуется: |
Б |
А. три |
|
Б. тир |
|
В. фенилпируват |
|
Г. тре |
|
Д. фениллактат |
|
30. катаболизм фен и тир наиболее активно идет в: |
А |
А. печени |
|
Б. надпочечниках |
|
В. эпителии |
|
Г. щитовидной железе |
|
Д. нервной ткани |
|
31. В реакции дезаминирования гистидина участвует фермент: |
В |
А. трансаминаза |
|
Б. декарбоксилаза |
|
В. гистидаза |
|
Г. трансметилаза |
|
Д. дегидратаза |
|
32. для синтеза гистамина необходима аминокислота: |
В |
А. сер |
|
Б. фен |
|
В. гис |
|
Г. тир |
|
Д. три |
|
33. ГАМК синтезируется из аминокислоты: |
Б |
А. сер |
|
Б. глу |
|
В. фен |
|
Г. тир |
|
Д. ала |
|
34. Аминокислотой - предшественником серотонина является: |
Г |
А. ала |
|
Б. тир |
|
В. сер |
|
Г. три |
|
Д. глу |
|
35. Для активации метионина необходим: |
В |
А. NAD+ |
|
Б. цАМФ |
|
В. АТФ |
|
Г. ГТФ |
|
Д. FAD |
|
36. Для превращения гистидина в гистамин необходим фермент: |
Б |
А. трансаминаза |
|
Б. гистидиндекарбоксилаза |
|
В. трансметилаза |
|
Г. гистидаза |
|
Д. дегидрогеназа |
|
37. Пищевая ценность белка зависит от: |
Г,Д |
А. Молекулярной массы |
|
Б. Наличия всех заменимых аминокислот |
|
В. Порядка чередования аминокислот |
|
Г. Наличия всех незаменимых аминокислот |
|
Д. Возможности расщепления в желудочно-кишечном тракте |
|
38. Соляная кислота в желудке выполняет следующие функции: |
Б, В, Г, Д |
А. Расщепляет специфические пептидные связи в белках пищи |
|
Б. Вызывает денатурацию белков пищи |
|
В. Активирует гидролиз пептидных связей в пепсиногене |
|
Г. Создает оптимум рН желудочного сока |
|
Д. Оказывает бактерицидное действие |
|
39. К группе эндопептидаз относятся: |
А, В, Д |
А. Пепсин |
|
Б. Аминопептидаза |
|
В. Трипсин |
|
Г. Карбоксипептидаза |
|
Д. Химотрипсин |
|
40. Клетками поджелудочной железы секретируются протеазы: |
А, Б, В |
А. Трипсиноген |
|
Б. Химотрипсиноген |
|
В. Прокарбоксипептидаза |
|
Г. Аминопептидаза |
|
Д. Дипептидаза |
|
41. В ходе активации пепсиногена происходит: |
А, Б, В |
А. Изменение конформации фермента |
|
Б. Гидролиз специфических пептидных связей в пепсиногене |
|
В. Отщепление пептида от N-конца пепсиногена |
|
Г. Присоединение HCl к аллостерическому центру профермента |
|
Д. Изменение pH желудочного сока |
|
42. пары "активатор - активируемый фермент" составлены правильно: |
Б, В, Д |
А. Трипсин - аминопептидаза |
|
Б. Трипсин - химотрипсиноген |
|
В. HCl - пепсиноген |
|
Г. Химотрипсин - эластаза |
|
Д. Энтеропептидаза – трипсиноген |
|
43. Белки секреторных клеток защищены от действия активных |
А, Б, В |
протеаз: |
|
А. Тем, что протеазы образуются в виде проферментов |
|
Б. Наличием слизи |
|
В. Присутствием на мембранах сложных белков - гликопротеинов |
|
Г. Присутствием в секреторной клетке активаторов протеаз |
|
Д. Отсутствием специфических ингибиторов протеаз |
|
44. Транспорт аминокислот через мембрану клеток слизистой |
В, Г, Д |
кишечника происходит: |
|
А. Простой диффузией |
|
Б. Облегченной диффузией |
|
В. Активным транспортом |
|
Г. С затратой энергии АТФ |
|
Д. С помощью белка-переносчика |
|
45. к белковой недостаточности приведет отсутствие в пище |
В, Г, Д |
аминокислот: |
|
А. Ала |
|
Б. Глу |
|
В. Фен |
|
Г. Лиз |
|