Материал: Разработка проекта технических условий на катализатор на сонове высоко кремнеземного цеолита
Для температуры 340°С обнаружено небольшое уменьшение селективности в отношении алифатических углеводородов и увеличение селективности в отношении ароматических углеводородов с ростом концентрации сильных кислотных центров Бренстеда. Селективность в отношении С3 углеводородов уменьшается, а в отношении С4 - увеличивается. На другие алифатические углеводороды изменение этого параметра не влияет. Среди ароматических углеводородов увеличивается селективность в отношении толуола и бензола при увеличении концентрации сильных кислотных центров Бренстеда, в то время как в отношении триметилбензола и ксилолов селективность уменьшается [36].
Силикатный модуль Si/Al катализатора оказывает значительное влияние на распределение продуктов конверсии этанола. Большой избыток кислотных центров Бренстеда в цеолите H-ZSM-5 с низким силикатным модулем является желательным для превращения легких олефинов в ароматические углеводороды и парафины. Низкие значения силикатного модуля обеспечивают большее образование ароматических соединений С6+, а также парафинов С1 - С5. При низкой кислотности катализатора образуется небольшое количество высших углеводородов. Высокие значения силикатного модуля катализатора способствуют высоким выходам легких олефинов: этилена, С3 и С4 [37].
Дезактивация катализатора.
Во время конверсии этанола происходит дезактивация катализатора H-ZSM-5, которая влияет на распределение продуктов. Для образования жидких углеводородов посредством каталитического превращения водного раствора этанола требуются высокие температуры, при которых наблюдается заметная дезактивация катализатора в связи с образованием кокса. Из-за дезактивации катализатора выход С5+-соединений уменьшается, в то время как выход этилена увеличивается вплоть до 100% [40].
Процесс дезактивации можно замедлить добавлением воды к сырью. Использование незначительно дистиллированного биоэтанола в качестве сырья приводит к появлению дополнительного количества воды в реакторе, что заметно снижает скорость дезактивации катализатора и позволяет использовать сырье с меньшей концентрацией этанола [30].
Влияние присутствия избытка воды в реакционной среде на дезактивацию катализатора неоднозначно. С одной стороны, в присутствии воды происходит уменьшение отложений кокса. Однако при температуре свыше 400°С наличие воды приводит к необратимой дезактивации катализатора, сопровождающейся изменением кристаллической структуры H-ZSM-5.
На реакцию дегидратации этанола дезактивация катализатора, вызванная образованием кокса, не влияет, однако она влияет на стадии образования остальных продуктов, а именно на реакции олигомеризации, крекинга, циклизации, ароматизации. Это объясняется тем, что реакция дегидратации этанола протекает на слабых кислотных центрах катализатора. Несмотря на отложения кокса на катализаторе, сохраняется остаточная кислотность, в первую очередь на внешней поверхности гранул, в то время как последующие стадии процесса превращения этанола в углеводороды требуют наличия активных центров с высоким уровнем кислотности. Последние дезактивируются в первую очередь, поскольку в основном они расположены на внутренней поверхности гранул цеолита, которая в течение реакции постепенно блокируется тяжелыми углеводородами и коксом.
При увеличении температуры реакции возникает проблема необратимой дезактивации катализатора, которая обусловлена деалюминированием цеолита H-ZSM-5. Авторы [40] показали, что при температуре 400°С не происходит необратимой дезактивации во всем исследованном ими диапазоне значений времени пребывания (от 0,5 до 6 часов) и содержания воды в сырье (от 6 до 75% масс в сырье). Тем не менее, при 500°С происходит необратимая дезактивация катализатора, даже если сырье содержит только этанол (без воды) и процесс ведется при малых значениях времени пребывания (минимальное образование воды), дезактивация является следствием деалюминирования катализатора водой, находящейся в реакционном объеме. Исследование процесса при температуре 450°С при использовании сырья с различным содержанием воды показало, что при этой температуре содержание воды в сырьевой смеси не должно превышать 50% масс для того чтобы необратимая дезактивация путем деалюминирования оставалась на незначительном уровне [40].
Обратимая дезактивация катализатора может быть предотвращена с помощью парового дистилляционного освобождения тяжелых продуктов водой как добавленной к сырьевому потоку, так и образованной в ходе реакции дегидратации. Полезное влияние воды проявляется внутри пор цеолита и на его внешней поверхности, где в случае цеолита H-ZSM-5 образуется кокс [39].
Увеличение содержания этилена в газообразных продуктах свидетельствует о дезактивации катализатора, которая происходит из-за отложений кокса, образованного вследствие реакций крекинга. Катализатор может восстановить свою активность, если его подвергнуть продувке потоком воздуха в течение нескольких часов при температуре 500-550°С [1].
Механизм конверсии этанола на катализаторе H-ZSM-5.
Среди продуктов процесса конверсии этанола на катализаторе H-ZSM-5 присутствует большое число разнообразных парафинов, олефинов, циклических и ароматических углеводородов, типичная хроматограмма содержит свыше 100 пиков соответствующих различным углеводородным продуктам. Это указывает на наличие ряда сложных реакций в процессе конверсии этанола на катализаторе H-ZSM-5 приводящих к такому разнообразию.
Показано, что все ароматические и неароматические продукты могут быть получены из этилена, а образование парафинов и ароматики из олефинов происходит одновременно [37].
Первой стадией процесса конверсии этанола на катализаторе H-ZSM-5 является дегидратация этанола. Кислотные центры Бренстеда являются активными центрами для реакции дегидратации этанола. Хотя механизм реакции дегидратации этанола еще до конца не объяснен, из эксперимента становится очевидным, что процесс может протекать по двум реакционным путям. Первый путь реакции включает в себя образование диэтилового эфира, как промежуточного соединения, который впоследствии превращается в этилен дегидратацией. Второй путь реакции приводит к прямому образованию этилена из этанола, этот процесс возможен при одновременном присутствии и основных, и кислотных активных центров на поверхности катализатора (таким катализатором как раз и является цеолит H-ZSM-5).
При температуре реакции ниже 260-270°С двухстадийный механизм реакции, включающий образование диэтилового эфира в качестве промежуточного соединения, существует совместно с прямым превращением этанола в этилен. При температурах выше 260-270°С в основном реакция протекает по второму механизму [42]. Следовательно, при протекании реакции конверсии этанола в углеводороды (интервал температур от 350 до 600°С [31]) осуществляется прямая дегидратация этанола до этилена.
Механизм процесса дегидратации этанола на цеолите H-ZSM-5 показан на рис. 1.
Молекула этанола сначала обратимо хемосорбируется на активном центре
Бренстеда цеолита H-ZSM-5, образуя оксониевый ион с частичным положительным
зарядом на кислороде этанола и частичным отрицательным зарядом на мостиковом
кислороде (II). При отщеплении молекулы воды (III) на поверхности цеолита
образуется этоксильная группа. Этот процесс может дать выход этилену при
значительно высоких температурах с образованием первоначального активного
центра Бренстеда (IV) [3].
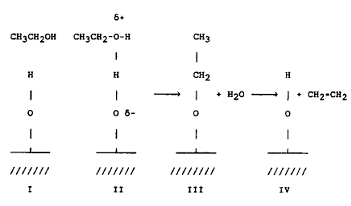
Рис. 1. Схема дегидратации этанола до этилена
Взаимодействие молекулы этанола с кислотной гидроксильной группой может быть подтверждено тем, что при контакте с этанолом соответствующая гидроксильная группа цеолита H-ZSM-5 немедленно исчезает. Было обнаружено, что адсорбированный катализатором H-ZSM-5 спирт находится в стехиометрическом соотношении: одна молекула спирта на один атом алюминия [43].
При низких температурах (160 - 240°С) молекула этанола на поверхности
цеолита может также реагировать со второй молекулой этанола (рис. 2) с
образованием хемосорбированного диэтилового эфира и воды (V). Молекула
диэтилового эфира может десорбироваться или разложиться на этилен и
хемосорбированную молекулу этанола, которая в дальнейшем также может
продиссоциировать. При более высоких температурах газообразный этилен может
присоединиться к адсобированной молекуле этанола, таким образом, произойдет
построение более или менее длинных алифатических цепей, которые могут
десорбироваться или превратиться в ароматические соединения или парафины [3].
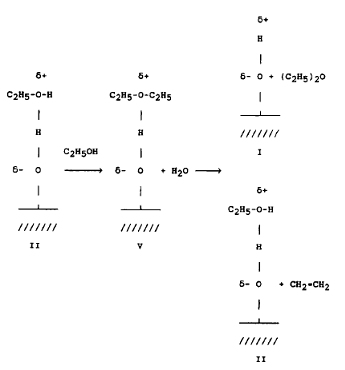
Рис. 2. Схема взаимодействия молекулы этанола, хемосорбированной на
поверхности цеолита, со второй молекулой этанола
Этилен и другие олефины могут рассматриваться как исходные реагенты из-за высокой скорости дегидратации этанола и их абсолютной независимости от реакций образования остальных углеводородов. Дальнейшие реакции образования ароматических углеводородов и парафинов из олефинов происходят практически одновременно [1].
Высокая активность цеолитов в процессе конверсии спиртов в углеводороды и то обстоятельство, что процесс можно замедлить присутствием азотных оснований или ионов натрия, указывают на протекание процесса через образование карбениевых ионов. Особая структура цеолитов с сильными электростатическими полями, которые способствуют образованию и устойчивости ионов карбения, является подтверждением этой гипотезы [1].
Авторами [33] было проведено обобщение результатов, полученных различными исследователями, в результате было доказано, что в процессе дальнейшего превращения низших олефинов происходит образование ионов карбения с различной степенью насыщенности (аллильных, диенильных и полиенильных).
Рассматривают два возможных пути образования аллильных катионов из олефинов:
) отрыв гидрид-иона от классического алкильного карбокатиона, который в свою очередь образуется при протонировании молекул олефина на бренстедовских кислотных центрах;
) непосредственное взаимодействие олефина с льюисовским кислотным центром цеолита, также сопровождающееся отщеплением гидрид-иона.
Первый из этих путей более вероятен. Общая схема образования и
последующего превращения аллильных и диенильных (подобно аллильным ионам,
диенильные катионы представляют собой гибридные структуры, в которых заряд
делокализован на пяти атомах углерода) катионов включает стадии
депротонирования димерного иона карбения и отрыв гидрид-иона от молекулы диена:
СН2![]() СН
СН![]() СН2 + СН3-СН
СН2 + СН3-СН![]() СН2 → СН3-СН-СН
СН2 → СН3-СН-СН![]() СН
СН![]() СН2 → СН3-С
СН2 → СН3-С![]() СН-СН
СН-СН![]() СН2 → СН2
СН2 → СН2![]() С
С![]() СН
СН![]() СН
СН![]() СН2
СН2
Эта схема демонстрирует также, каким образом может происходить рост углеродной цепи с образованием из молекул низших олефинов олигомеров с большей молекулярной массой.
Схема олигомеризации этилена на катализаторе H-ZSM-5 представлена на рис.
3, где Н-OZ - это бренстедовский кислотный центр.
![]()
Рис. 3. Схема олигомеризации этилена на H-ZSM-5
Согласно схеме, катион (IV) взаимодействует с молекулой этилена из газовой фазы, образуя н-бутильный катион (V). Эта реакция протекает сравнительно легко и приводит к образованию линейного олигомера. Дальнейший рост углеродной цепи происходит путем присоединения молекулы этилена к катиону (VI) с образованием разветвленного олигомера (VII), который легко изомеризуется в третичный ион карбения (VIII). Разветвленные олигомеры могут подвергаться изомеризации с участием промежуточного соединения, содержащего протонированное циклопропановое кольцо (VIII - XII). Подобные превращения приводят к образованию линейных продуктов при олигомеризации пропилена, изобутилена и 2-метилбутена-1.
Общая схема превращения низших олефинов в олигомерные и ароматические
продукты на цеолитах приведена на рис. 4.
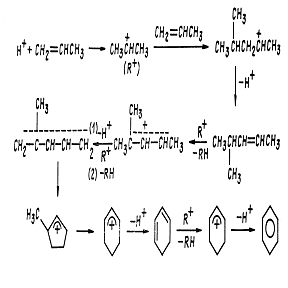
Рис. 4. Общая схема превращения низших олефинов в олигомерные и
ароматические продукты на цеолитах
Образование высокомолекулярных ионов карбения описывается посредством реакций конденсации их с олефинами. Процесс будет продолжаться до тех пор, пока размер их молекул не достигнет достаточного для проведения реакции циклизации с образованием ароматических углеводородов и водорода. При добавлении водорода к олефинам получаются парафины.
Данный механизм представляет собой взаимодействие между газообразными олефинами и адсорбированными ионами карбения, в результате которого получаются жидкие и газообразные углеводороды [1].
Образование ароматических углеводородов, полициклических соединений и полиалкилнафталинов, которые могут действовать как предшественники кокса, может быть описано механизмами олигомеризации и полимеризации. Но благодаря природе молекулярных сит катализатора эти процессы не реализуются, так как предотвращаются реакции конденсации между ионами карбения и олефинами, если каждый из них содержит более 6 атомов углерода [1].
Обнаружено, что скорость образования кокса пропорциональна скорости образования ароматических углеводородов. Концентрация кокса, накопленного в течение 12 часов при температуре 340°С, имеет линейную зависимость от скорости образования ароматических углеводородов, из чего можно сделать вывод, что реакции коксообразования и ароматизации протекают по одному реакционному пути [36].
Из проведенного обзора литературы следует, что биоэтанол может быть успешно превращен в углеводороды на катализаторе H-ZSM-5. Процесс конверсии этанола на H-ZSM-5 представляет собой совокупность реакций дегидратации, олигомеризации, ароматизации, алкилирования, изомеризации, перераспределения водорода, крекинга и т.д.
При низких температурах (около 250°С) этилен является основным продуктом, получаемым на выходе, а при высоких температурах последовательные реакции этилена приводят к образованию ароматических углеводородов и парафинов с максимальным выходом при температуре около 350°С. Со временем катализатор дезактивируется. Однако необходимо отметить, что при этом уменьшаются только выходы ароматических соединений и парафинов, а выход этилена увеличивается вплоть до 100% при полной конверсии этанола. Даже полностью закоксованный катализатор будет продолжать дегидратировать этанол до этилена еще долгое время. Можно сделать вывод, что дегидратация и дальнейшие последовательные реакции катализируются разными активными центрами [3].
Цеолит H-ZSM-5 способен превращать этанол в присутствии воды в ряд углеводородов как алифатических, так и ароматических. Конверсия на цеолите H-ZSM-5 может быть альтернативным способом переработки ферментационных смесей, содержащих этанол, не включающим энергоемкую стадию дистилляции [39]. Однако главным вопросом при использовании таких смесей будет устойчивость структуры цеолита к действию пара. Под воздействием пара происходит деалюминирование цеолита H-ZSM-5 и потеря им активности после нескольких циклов реакция/регенерация при использовании в качестве сырья очень разбавленных водных растворов спирта. Чтобы избежать необратимой дезактивации катализатора необходимо использовать сырье с содержанием воды, не превышающим 50% масс. и при температуре не более 500°С [3].