Материал: Пат. анатомия боевых поражений_2002
Патоморфология первого периода ожоговой болезни.
Макроскопическая картина патологических изменений у обожженных, умерших в периоде шока, за исключением местных изменений, скудная.
Непораженная кожа бледная, сухая. Кровенаполнение внутренних органов неравномерное, что соответствует различной плотности α- и β-адренергических рецепторов. В слизистой оболочке желудка часто обнаруживают эрозии и ост- рые язвы. В случаях желудочных кровотечений содержимое желудка имеет цвет «кофейной гущи». В мочевом пузыре может содержаться мало мочи темно- бурого цвета с запахом гари. Петли тонкой кишки вздуты из-за пареза.
Микроскопически обнаруживают белково-водяночную дистрофию гепа- тоцитов, нефроцитов, кардиомиоцитов. В легких можно обнаружить, наряду с другими признаками, проявления дистресс-синдрома взрослых с десквамацией альвеолоцитов в просвет альвеол, появлением в альвеолах многочисленных макрофагов, иногда — гиалиновых мембран. В случаях, когда длительно суще- ствует гипотензия, в печени отмечают некрозы центральных отделов долек. В слизистых оболочках кишок часто встречают мелкоочаговые кровоизлияния.
2.5.2.2. В т о р о й п е р и о д о ж о г о в о й б о л е з н и
Второй период — последствий шока, ожогового и инфекционно-вос-
палительного эндотоксикоза рассматривают как два самостоятельных периода:
1)период «ожоговой токсемии» — до начала отторжения струпа или до некрэктомии;
2)период «септикотоксемии» — до закрытия гранулирующих ран транс-
плантатами и эпителизации промежутков между ними.
При этом имеется в виду то, что в первые две недели (или более), когда происходит формирование демаркационной линии, отмечается отравление ор- ганизма т. н. «ожоговыми токсинами», а в последующие сроки значение приоб- ретают гнойные осложнения. По-видимому, «ожоговые токсины» образуются в дерме, так как при обширных поверхностных ожогах токсичные продукты в плазме не обнаруживают. Наличие ожогового токсина подтверждается рядом исследований. Например, из обожженной кожи крыс выделен гликопротеид с молекулярной массой 290000, который длительно блокирует систему фагоци- тирующих мононуклеаров, резко увеличивает проницаемость клеточных мем- бран, угнетает миграцию лейкоцитов, обладает гипотензивным действием /113/.
Но в первые две недели нельзя отрицать и роль зкзотоксинов микроорганизмов в эндотоксикозе. Микрофлора ожоговых ран находит благоприятную среду в очагах влажного некроза, которые часто прилежат к струпу, или в участках влажного некроза, характерного для воздействия горячих жидкостей, пара, тле-
121
ния одежды. Поэтому разграничение второго периода на «ожоговую токсемию» и «септикотоксемию» требует более четкого обоснования.
Патоморфология второго периода ожоговой болезни.
Вслучаях, когда не проводят некрэктомию с последующей дерматомной ау- топластикой свежих ран сплошными лоскутами, с клинической и морфологической точек зрения второй период целесообразно представить в виде четырех стадий:
1 стадия — формирования зоны демаркационного воспаления (про- должительностью около двух недель);
2 стадия — отторжения струпа (продолжительностью 2 — 3 недели); 3 стадия — гранулирующих ран (до закрытия ран трансплантатами); 4 стадия — очаговых некрозов аутотрансплантатов, отторжения алло-
или ксенотрансплантатов, повторной аутопластики и эпителизации ран.
Взависимости от тяжести ожоговой травмы, продолжительности ожогово- го и инфекционно-воспалительного эндотоксикоза, у больных с ожогами отме- чается различная степень истощения, гипопротеинемия. Нередко наблюдается желтуха — за счет повышения уровня непрямого (несвязанного) билирубина в связи с гипоальбуминемией. По завершении самостоятельного отторжения стру- па ожоговые раны выполняются грануляционной тканью, поверхностный слой которой (лейкоцитарно-некротический) всегда бактериально загрязнен. Несмот- ря на инфицированность ожоговых ран, грануляционная ткань, если в ней не возникают выраженные гнойно-некротические процессы, является оптимальным ложем для трансплантатов. Приживление лоскутов значительно ухудшается, ес- ли грануляции отечные, атрофичные или, наоборот, гипертрофированы.
При оценке микроскопических признаков следует учитывать, что они наслаиваются на изменения, возникшие в периоде шока.
Нарушение микроциркуляции в головном мозге вследствие токсемии ве- дет к отеку и ухудшению газообмена, гипоксии и развитию диффузно-очаговой дистрофии нейроцитов. Возможны также моноцеллюлярные некрозы, гистоло- гические признаки которых — кариолизис и базофилия цитоплазмы /66/.
Вмиокарде — отек стромы, белково-водяночная дистрофия, обуслов- ленные анемией, электролитными нарушениями и токсемией. Ультраструктур- ные изменения характеризуются разрушением мембран органелл и фрагмента- цией миофибрилл, гиперплазией и гипертрофией митохондрий.
Влегких морфологические признаки послешоковых изменений и эндо-
токсикоза могут приобретать характер наслаивающихся однотипных признаков респираторного дистресс-синдрома — с повторным накоплением в альвеолах белковой жидкости, макрофагов и появлением новых гиалиновых мембран. Частым осложнением является очаговая пневмония.
Впечени обнаруживают более обширные некрозы центров долек. В гепа- тоцитах и звездчатых ретикулоэндотелиоцитах выявляют гемосидерин, его со- держание зависит от количества перелитой крови. Электронномикроскопически
122
в гепатоцитах — гигантские митохондрии с признаками фрагментации крист, большое число миелиноподобных структур на месте разрушенных органелл.
Впочках повышение проницаемости капилляров клубочков приводит к повышению фильтрации альбуминов, микроглобулинов, лизоцима, а также к проникновению в просветы капсул крупномолекулярных белков, эритроцитов.
Всвязи с избыточной реабсорбцией белков, а также потребностями удаления продуктов аутолиза некротизированной кожи, нефроциты проксимальных ка- нальцев гипертрофируются, при электронной микроскопии в них отмечают ги- перплазию и гипертрофию митохондрий.
Вподжелудочной железе, в слизистых оболочках желудка и кишок
микроскопически обнаруживают признаки отека, кровоизлияния, дистрофиче- ские изменения в эпителии. В костном мозге уменьшено число кроветворных элементов на единицу площади, отмечают гемосидероз. В вилочковой железе, лимфатических узлах и в селезенке — атрофия лимфоцитарных структур.
Осложнения второго периода ожоговой болезни.
К осложнениям второго периода относятся:
— флегмоны, абсцессы, сепсис;
— острые язвы желудка и двенадцатиперстной кишки, при которых воз- можны перфорация, кровотечение;
— острый холецистит;
— истощение с потерей до 30 — 40 % массы тела;
— тромбозы брыжеечных сосудов;
— гипопластическая анемия, геморрагический синдром;
— вирусный гепатит (В, В и D, С, F);
— иммунные осложнения, в том числе гломерулонефриты — в связи с избытком циркулирующих иммунных комплексов.
2.5.2.3. Т р е т и й п е р и о д о ж о г о в о й б о л е з н и
Третий период ожоговой болезни — период реконвалесценции — во многом определяется эффективностью дерматопластических операций. Через неделю после пересадки лоскутов на границе трансплантата и ложа обнаружи- вают анастомозы сосудов, вступивших в контакт друг с другом под углом. Ар- терии, артериолы, капилляры и венозные сосуды имеют обычный для кожи вид, что свидетельствует о сохранении собственной сосудистой сети и восстановле- нии в ней кровообращения. В случаях аутопластического закрытия гранули- рующих ран под трансплантатами через неделю обнаруживают слой беспоря- дочно расположенных фибробластов, а глубже — горизонтальных фибробла- стов, переходящих в рубцовый слой.
После восстановления кожного покрова трансплантатами и завершения эпителизации ран, не закрытых трансплантатами, начинается длительный пери-
123
од нормализации микроциркуляции и регенерации клеточных элементов во внутренних органах и системах. Клинически при этом наблюдают медленное восстановление их функций. Этот период растягивается на месяцы, многие функции нормализуются через несколько лет.
Местные изменения нередко требуют консервативного и хирургического лечения. Даже при полном закрытии ран сплошными дерматомными ауто-
трансплантатами и успешном их приживлении возможны рубцовые изменения восстановленного кожного покрова. Грубые рубцы могут формироваться также между «марками» и «полосками», при неполном закрытии ран лоскутами. Руб- цовые изменения являются причиной различных деформаций и контрактур, вызывающих косметическую и функциональную неполноценность опера- тивно восстановленного кожного покрова лица, шеи, суставов /15/.
Через 3 месяца после операции под сплошными лоскутами, независимо от того, на какие раны произведена пересадка кожи — гранулирующие или свежие операционные, обнаруживается рубцовая ткань, имеющая строение как обычных, так гипертрофических и келоидных рубцов. Отмечается уменьшение площади и сморщивание восстановленного кожного покрова из-за укорочения пучков колла- геновых волокон рубцового слоя в процессе созревания соединительной ткани.
Обычные рубцы состоят из рыхлых пучков коллагеновых волокон. Гипертрофические рубцы более грубые, имеют строение тесно приле-
гающих коллагеновых пучков, и напоминают сухожилия.
Келоидные рубцы (рис. 72) имеют иные микроскопические особенности
— среди обширных полей грубоволокнистой соединительной ткани располага- ются так называемые «узлы роста» /16/. Они состоят из множества функцио- нально активных фибробластов, вокруг которых располагаются многочислен- ные толстые короткие коллагеновые пучки, напоминающие остеоидные балки.
Обычные рубцы под трансплантатами в сроки от четырех до двенадцати ме- сяцев после пересадки кожи частично рассасываются, в связи с чем восстановлен- ный кожный покров приобретает вид и свойства, близкие к нормальной коже.
Под влиянием консервативного лечения возможно также частичное рас- сасывание и гипертрофических рубцов.
Келоидные рубцы практически не рассасываются, активные «узлы роста» в них могут выявляться в течение нескольких лет. В этом случае требуется по- вторное хирургическое лечение.
Рассасывание рубцовой ткани осуществляется двумя путями:
—за счет активизации фиброцитов и приобретения ими свойств фиброк- ластов, то есть клеток, способных фагоцитировать коллагеновые фибриллы;
—вследствие бесклеточного разрушения коллагеновых волокон до амор- фного материала и образования из него тонких волокон, обладающих призна- ками эластических волокон.
124
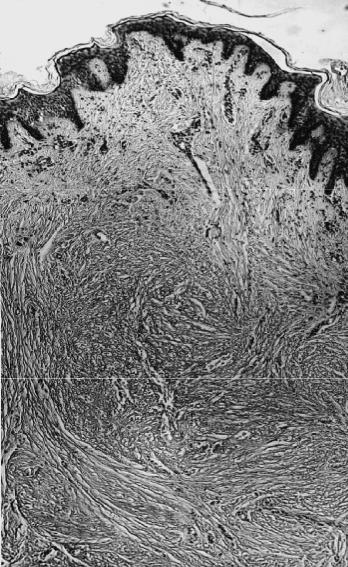
Рис. 72. В микропрепарате — ке- лоидный рубец под аутотранс- плантатом после глубокого ожога; в «узле роста» — многочисленные фибробласты; три месяца после аутопластики (окраска толуидино- вым синим, × 40)
Такие изменения происходят с коллагеновыми волокнами, не имеющими функциональных нагрузок, не подвергающимися растяжению. Поэтому в ран-
ние сроки после дерматомной аутопластики целесообразна иммобилизация оперированной области в положении максимального растяжения восстановлен- ного кожного покрова в сочетании с функциональной нагрузкой (для профи- лактики контрактур положения). Это должно способствовать формированию под трансплантатами коллагеновых пучков такой длины, при которой они в дальнейшем при выполнении движений не будут испытывать натяжения /128/.
125