Материал: Основы сестринского дела
ст е р и л и з у е м ы е изделия, что ухудшает условия их хранения, увеличивает опасность
ре к о н т а м и н а ц и и .
Воздушный метод. Стерилизующим агентом является сухой горячий воздух. От личительная особенность метода — не происходит увлажнения упаковки и изделий, и связанного с этим уменьшения срока стерильности, а также коррозии металлов.
Недостатки метода:
•медленное и неравномерное прогревание стерилизуемых изделий;
•необходимость использования более высоких температур;
•невозможность использовать для стерилизации изделий из резины, полимеров;
•невозможность использовать все и м е ю щ и е с я упаковочные материалы.
В о з д у ш н ы й м е т о д проводят в воздушных стерилизаторах п р и с л е д у ю щ и х ре жимах:
•2 0 0 ± З в С — 30 мин;
•1 8 0 ± 3 ° С — 40 мин;
•1 6 0 ± 3 ° С — 120 мин.
Эффективность воздушной стерилизации во многом зависит от равномерного проникновения горячего воздуха к стерилизуемым изделиям, что достигается прину дительной циркуляцией воздуха со скоростью 1 м/с и соблюдением норм загрузки стерилизатора .
И паровой, и воздушный методы стерилизации экологически чистые.
Газовый метод о с у щ е с т в л я е т с я п р и 18-80°С. Изделия с т е р и л и з у ю т с я в у п а ковках.
При газовой стерилизации используют этилен-оксид и его с м е с и , формальдегид. В газообразном состоянии этилен-оксид не вызывает коррозии металлов, не пор тит изделий из кожи, шерсти, бумаги, пластмасс; он является сильным бактерицидным,
спороцидным и вирулицидным средством. Пары обладают высоким проникновением. Недостаток этилен - оксида — его токсичность для персонала и взрывоопасность
при н е с о б л ю д е н и и техники безопасности . Процесс стерилизации имеет продолжи тельный цикл. Этилен-оксид редко используется в ЛПУ.
Формальдегид по своим качествам не уступает, а по некоторым показателям пре восходит этилен-оксид. Для стерилизации, как правило, используются пары 40 - про центного спиртового раствора формальдегида. Стерилизующим агентом может быть формальдегид, испаряющийся из параформа или формалина.
Стерилизация растворами — вспомогательный метод, который применяют при невозможности использования других. Стерилизация растворами имеет следующие недостатки, изделия стерилизуются без упаковки, их необходимо промывать после стерилизации, что может привести к реконтаминации.
Преимущества: повсеместная доступность, легкость в исполнении и др . Стерилизуемые растворами изделия с в о б о д н о раскладывают в емкости . При
большой длине изделие укладывают по спирали, каналы и полости заполняют раствором. После окончания стерилизации изделия трижды (при стерилизации перекисью водорода — дважды) погружают на 5 мин в стерильную воду, каждый раз меняя ее, затем стерильным корнцангом их переносят в стерильную емкость, выложенную сте
рильной простыней .
Поскольку изделия стерилизуют растворами без упаковки, этот метод может быть использован только при децентрализованной системе .
Радиационный метод необходим для стерилизации изделий из термолабильных материалов. Стерилизующим агентом являются ионизирующие у (гамма)- и β (бета)- излучения.
Для индивидуальной упаковки, помимо бумажных используют пакеты из полиэти лена. Сохраняется стерильность в такой упаковке годами, но и он ограничен. Срок годности указывается на упаковке.
36
Радиационный — основной метод промышленной стерилизации . Он использует ся предприятиями, выпускающими стерильные изделия однократного применения .
К о н т р о л ь к а ч е с т в а с т е р и л и з а ц и и
Контроль позволяет улучшить качество стерилизации в ЛПУ. Он предусматрива ет определение эффективности и параметров стерилизации .
Надежность воздушной стерилизациизависит от конструкции стерилизатора, его исправности, схемы и объема загрузки, используемой защитной упаковки, применяе мых методов оперативного и периодического контроля, подготовки персонала, обсу живающего стерилизатор.
Проблема надежности о с о б е н н о актуальна при эксплуатации аппаратов уста ревших типов, при отсутствии доступных методов контроля стерилизации .
Контроль эффективности стерилизации в воздушном стерилизаторе осуществ ляется бактериологическим методом и химическими термовременными индикаторами.
Бактериологический метод контроля проводят с помощью биотеста — объекта из определенного материала, обсемененного тест - микроорганизмами . В качестве носителей используют небольшой флакон, с о д е р ж а щ и й с п о р ы B.Licheniformis. Конт роль проводят в соответствии с утвержденной методикой. Существуют и готовые сертифицированные тесты со с п о р а м и B.Licheniformis с цветными питательными средами, позволяющими провести бактериологический контроль непосредственно в
ЦСО при наличии в нем термостата . |
|
|
|
||
Контроль |
воздушной |
стерилизации |
химическими |
термовременными |
ин |
дикаторами. Для оперативного контроля ранее рекомендовали многочисленные хи мические вещества, точка плавления которых соответствует температуре стерилиза ции. Но на сегодняшний день всем ясно, что они не могут считаться надежными инди каторами, поскольку не дают представления о времени воздействия горячего возду ха на изделие. Такой контроль носит ориентировочный характер и не гарантирует достижения стерильности в процессе стерилизации .
Надежность оперативного контроля существенно повышается при использова нии индикаторов интегрированного действия, в частности, НП фирмы «Винар» ИС-160 и ИС-180, изменяющая окраску до цвета эталона только при воздействии на них температуры стерилизации в течение всей стерилизационной выдержки. Полос ки индикатора закладываются в контрольные точки стерилизатора при каждом цикле стерилизации. Если окраска индикатора после стерилизации в какой-либо точке свет лее эталона, все изделия считаются нестерильными.
Пакеты из пергаментной бумаги, используемые для упаковки, при стерилизации в современной с т е р и л и з у ю щ е й аппаратуре имеют подобный индикатор, нанесенный в фабричных условиях.
— Надежность паровой стерилизации зависит от нескольких факторов:
•соблюдения условий эксплуатации;
•точности контрольно-измерительных приборов, установленных на стерилизаторе;
•полноты удаления воздуха из стерилизуемых изделий;
•герметичности камеры стерилизатора .
Методы периодического контроля паровых стерилизаторов изложены в системе «чистый инструмент». Они включают:
•проверку точности манометра;
•проверку точности регистрации самописцами температуры и давления;
•контроль герметичности камеры стерилизатора;
•контроль качества автоматического вакуум-теста;
•контроль эффективности сушки текстильных материалов;
•проверку полноты удаления воздуха из стерилизуемых изделий.
Определение эффективности бактериологическим методом в паровом сте
рилизаторе осуществляется тестами, с о д е р ж а щ и м и с п о р ы B.Stearothermophilus в соответствии с методикой, утвержденной МЗ РФ.
37
О п е р а т и в н ый контроль паровой стерилизации проводят х и м и ч е с к и м и и н д и к а т о р а м и интегрированного действия (термо-временными).
Индикаторы плавления (тиомочевина, бензойная кислота и др . ), которые все еще используются в некоторых ЛПУ, не являются индикаторами стерильности, поскольку регистрируют только температуру, но не учитывают стерилизационную выдержку (время стерилизации) . И н д и к а т о р ы ф и р м ы «Винар» ИС-120 и ИС-132, также, как и в воз
д у |
ш н о м |
стерилизаторе, изменяют |
окраску до |
учета |
эталона только |
при воздействии |
на |
них |
температуры стерилизации |
в течение |
всей |
стерилизационной |
выдержки. |
При каждом цикле полоски индикатора закладываются в контрольные точки сте рилизатора. Если окраска индикатора в какой-нибудь точке светлее эталона, все из
делия считаются |
нестерильными . |
|
1.3. Контроль за распространением инфекции |
||
Взятие для бактериологического |
исследования мочи, мокроты, содержимого зева, |
|
носа, носоглотки, |
и взятие кала |
—для паразитологического исследования. |
Бактериологическое и паразитологическое исследования проводятся для диаг ностики и осуществления контроля над распространением инфекции.
Емкости для проб получают накануне в бактериологической (паразитологической) лаборатории .
П о д г о т о в к а к в з я т и ю п р о б ы б и о л о г и ч е с к о г о м а т е р и а л а д л я б а к т е р и о л о г и ч е с к о г о и п а р а з и т о л о г и ч е с к о г о и с с л е д о в а н и я
•Материал для исследований нужно брать до начала антибактериальной тера пии или через 8-10 ч после введения последней дозы антибактериального препарата.
•Чтобы избежать загрязнения пробы микрофлорой окружающей среды, необхо
ди м о соблюдать строжайшую асептику.
•Использовать:
а) ватные тампоны для взятия биологического материала из раны, со слизистых оболочек (глаз, зева, носа);
б) проволочную петлю для взятия биологического материала из влагалища, аналь ного отверстия;
в) стерильную посуду для непосредственного с б о р а мочи, мокроты, кала.
•Количество материала должно быть достаточным для исследования и при не обходимости — для его повторения.
•Соблюдать требования транспортировки:
а) транспортировку полученного биологического материала в лабораторию про изводят в максимально короткие сроки;
б) если материал нельзя немедленно транспортировать в лабораторию, его сле дует хранить в холодильнике, или в специальных транспортных средах, когда транс портировка длится более 24 ч, а также когда микроорганизмы погибают почти сразу после взятия;
в) биологический материал для культивирования строгих анаэробов транспорти ровать в специальных флаконах, заполненных газом;
г) материал для бактериологического исследования транспортировать в с п е ц и альных жестких емкостях ( бикс и т.п.)
•К клиническому образцу необходимо приложить сопроводительный документ,
со д е р ж а щ и й с л е д у ю щ и е сведения:
характер |
(вид) материала; |
|
|
|
ФИО |
пациента; |
|
|
|
возраст |
пациента; |
|
|
|
название |
лечебного |
учреждения или его |
отделения; |
|
номер |
медицинской |
карты |
стационарного |
больного; |
предполагаемый |
диагноз; |
|
|
|
38
результаты |
предыдущих |
микробиологических |
исследований; |
|||
предшествующая |
антибактериальная |
терапия; |
||||
дата и время взятия материала; |
|
|
||||
цель |
исследования; |
|
|
|
||
ФИО |
врача, |
|
направляющего |
материал |
для |
исследования. |
О б у ч е н и е п а ц и е н т а ( п а ц и е н т к и ) т е х н и к е с б о р а м о ч и д л я б а к т е р и о л о г и ч е с к о г о и с с л е д о в а н и я
Оснащение: стерильная емкость, бумажное полотенце, салфетки.
I. П о д г о т о в к а к п р о ц е д у р е
1. Уточнить у пациента понимание цели предстоящего исследования и получить его согласие (информированное согласие на процедуру получает врач). В случае неинформированности пациента — уточнить у врача дальнейшую тактику.
2. Объяснить пациенту цель предстоящей подготовки к исследованию и ее пос ледовательность.
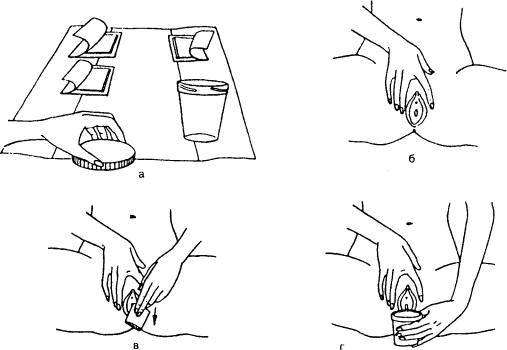
3.А. Подготовка женщины (рис.. 1.10)
Рис. 1.10. Подготовка и взятие мочи для микробиологического исследования у ж е н щ и н
•Утром накануне процедуры приготовить теплую кипяченную воду и мыло для подмывания.
•Зайти в туалетную комнату и раздеться ниже пояса.
•Вымыть руки.
•Расстелить бумажное полотенце, положить на него бумажные салфетки и по
ставить закрытый с о с у д для с б о р а мочи.
• Сесть как можно ближе к спинке унитаза и развести ноги. Пальцами раздвинуть половые губы и держать их раздвинутыми до окончания процедуры .
39
• Подмыться тщательно кипяченой водой с мылом, проводя рукой в направлении с п е р е д и назад.
•Осушить (по очереди) правую и левую половые губы и наружное отверстие мочеиспускательного канала, используя три салфетки.
•Выбросить салфетки в унитаз.
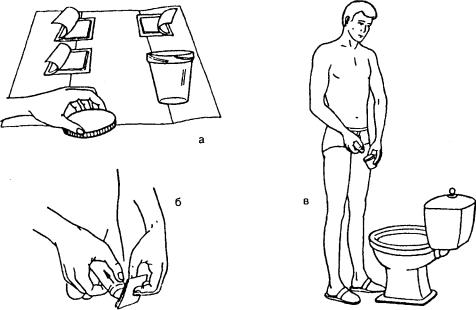
3.Б. Подготовка мужчины (рис. 1.11).
Рис. 1.11. Подготовка и взятие мочи для микробиологического исследования у мужчин
•Приготовить теплую кипяченую воду и мыло для подмывания.
•Расстелить в туалетной комнате бумажное полотенце, положить на него бумаж
ные салфетки и поставить закрытый с о с у д для с б о р а мочи.
•Вымыть руки.
•Взять половой член, как при мочеиспускании, освободить головку, отодвинуть крайнюю плоть и вымыть ее водой с мылом.
•Высушить головку полового члена, используя три салфетки; выбрасывать сал
фетки в унитаз сразу же после однократного промокания.
I I . В ы п о л н е н и е п р о ц е д у р ы
4. Взять емкость для с б о р а мочи, открыть крышку, не прикасаясь к внутренней поверхности емкости и крышки; положить крышку на бумажное полотенце внутрен ней поверхностью вверх.
5. Выпустить немного мочи в унитаз и задержать мочеиспускание.
6. Подставить с о с у д для мочи, не касаясь им гениталий и ануса (головки полового члена).
7. Собрать в с о с у д 3-5 мл мочи и задержать мочеиспускание.
Закрыть емкость с мочой крышкой, не касаясь ее внутренней поверхности, и за кончить мочеиспускание в унитаз.
8. Вымыть руки. Одеться.
III . З а в е р ш е н и е п р о ц е д у р ы
9. Отнести в контейнере с о с у д с мочой и направление в лабораторию (в амбула торных условиях. В условиях стационара — отдать медсестре) .
40