Материал: Опорні конспекти та дидактичні матеріали з органічної хімії
70 Опорні конспекти та дидактичні матеріали з органічної хімії
|
Хімічні властивості |
|
|
1. |
Повне окиснення |
|
|
|
(C6H10O5 )n + O2 → |
|
+ |
|
|
||
2. |
Гідроліз |
|
|
(C6H10O5 )n + nH2O →
3.Якісна реакція на крохмаль
|
(C6H10O5 )n + I2 → |
|
|
|
|
|
|
|
|
|
|
|
|
4. |
Нітрування глюкози |
|
|
|
||
|
(C6H10O5 )n + 3HNO3 → |
|
|
|
(нітроцелюлоза) |
|
|
|
|
|
|||
5. |
Естерифікація |
|
|
|
||
|
(C6H10O5 )n + 3CH3COOH |
|
(ацетат целюлози) |
|||
|
|
|||||
Поширення у природі
Крохмаль як резервне харчування накопичується в бульбах, плодах, насінні рослин. У бульбах картоплі міститься до 24 % крохмалю, у зернах пшениці — до 64 %, рису — 75 %, кукуру дзи — 70 %.
Целюлоза — головна складова частина клітинних оболонок усіх вищих рослин. Уміст целюлози у волокнах насіння бавовнику становить 95–98 %, луб’яних — 60–85 %, тканинах деревини — 40–44 %, нижчих рослинах — 10–25 %.
Застосування
Крохмалю
yyОдержання глюкози, патоки, етанолу; yyобробка тканин;
yyу побуті.
Целюлози
yyВиготовлення паперу й картону;
yyпереробка на штучні волокна (ацетатний шовк), пластмаси, кіно- й фотоплівки, лаки й емалі, бездимний порох, мийні засоби.
Одержання
6nCO2 + 6nH2O фотосінтез→(C6H10O5 )n + 6nO2↑
Теоретична частина |
|
|
|
|
|
71 |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Нітрогеновмісні органічні сполуки |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
Нітрогеновмісні |
|
|
|
|
|
|
||||
|
|
|
|
|
органічні сполуки |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Аміни |
|
|
|
|
|
Білки |
|
|
|||||
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
Аміно- |
|
|
||||||||||
|
|
|
|
|
|
кислоти |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Аміни |
|
|
|
|
|
|
|
|
|
|
|
||||
Загальна формула |
|
|
|
|
|
|
|
|
|
|
|
||||
|
R N |
|
H |
|
|
|
H |
|
|
|
R″ |
||||
|
|
|
|
|
N |
|
|
|
|||||||
|
|
R |
|
|
R |
|
N |
||||||||
|
|
|
|
|
|
||||||||||
|
|
|
|||||||||||||
|
H |
|
|
|
R′ |
|
|
|
R′ |
||||||
|
первинні |
|
вторинні |
|
третинні |
||||||||||
Номенклатура |
|
|
|
|
|
|
|
|
|
|
|
||||
Назва вуглеводневого радикалу + |
|
|
|
|
|
|
|
||||||||
(нумерація головного ланцюга — |
|
|
) |
||||||||||||
Ізомерія
Скласти ізомери й дати їм назви за номенклатурою ІЮПАК для формули C4H11N.
Фізичні властивості
Фізичні властивості |
Аміни |
Амінокислоти |
Білки |
|
|
|
|
Агрегатний стан |
|
|
|
|
|
|
|
Запах, смак |
|
|
|
|
|
|
|
Розчинність у воді |
|
|
|
|
|
|
|
72 |
Опорні конспекти та дидактичні матеріали з органічної хімії |
|
|
Одержання
1.R − NH3 − Cl + NaOH →
2.R − Cl + NH3 →
3.R− NO2 + H2 →
4.R− OH+ NH3 →
Застосування
yyДля виробництва барвників і лікарських речовин;
yyдля виробництва поліамідів, з яких виготовляють синтетичне волокно (капрон, найлон).
Хімічні властивості амінів
Аміни — органічні основи.
1.R− NH2 + O2 →
2.R− NH2 + H2O → R− NH+ H2O →
R
R
R− N+ H2O →
R
3.R − NH2 + HCl →
R− NH + HCl →
R
R
R − N + HCl →
R
Анілін
Молекулярна формула
C6H5NH2
Структурна формула
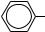 NH2
NH2
Номенклатура
Номенклатурна назва — феніламін.
|
Теоретична частина |
73 |
|
|
|
|
Фізичні властивості |
|
|
|
|
|
Агрегатний стан |
Колір |
|
Запах |
Розчинність у воді |
|
Дія на організм людини |
|
|
|
|
Взаємовплив груп атомів у аніліні
1.Бензенове кільце _____________________ основні властивості аміногрупи порівняно з аліфатичними амінами й навіть із амо ніаком.
2.Під впливом аміногрупи бензенове кільце стає ____________
активним у реакціях заміщення, ніж бензин.
δ-
 NH2
NH2
δ- |
δ- |
|
Хімічні властивості
1.За групою NH2
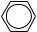 −NH2 + HCl →
−NH2 + HCl →
 −NH2 + H2O →
−NH2 + H2O →
2.За бензеновим кільцем
 −NH2 +3Br2 →
−NH2 +3Br2 →
3.Якісна реакція
C6H5NH2 + K2Cr2O7 + H2SO4 →
Застосування
У виробництві: yyполіуретанів; yyштучних каучуків; yyгербіцидів; yyбарвників; yyвибухових речовин; yyлікарських засобів.
74 |
Опорні конспекти та дидактичні матеріали з органічної хімії |
|
|
Одержання
1.Реакція Зініна (1842 р.)
C6H5NO2 + 3(NH4 )2 S → C6H5NH2 + 6NH3 + 3S + 2H2O
2.Сучасний спосіб
4C6H5NO2 +9Fe +4H2O → 4C6H5NH2 +3Fe3O4
C6H5NO2 +3H2 → C6H5NH2 +2H2O
Амінокислоти
Загальна формула
NH2 − CnH2n − COOH
(CnH2n+1O2N)
Номенклатура
1.IUPAC
а) |
Нумерація починається з |
|
; |
||
б) |
назва: локант NH2 − |
|
|
+ назва кислоти. |
|
|
|
||||
2.Систематична
а) Цифри замінюють |
|
. |
|||
|
|
|
|
|
|
б) |
Нумерація з |
|
|
. |
|
|
|
|
|
|
|
в) |
Назви кислот — систематичні. |
|
|
||
3.Історичні назви
NH2 − CH2 − COOH
Гліцин
CH3 − CH − COOH
NH2
Аланін
Скласти ізомери й дати їм назви за номенклатурою ІЮПАК для речовини, формула якої C4H9O2N.
|
Теоретична частина |
75 |
|
|
|
|
|
|
Фізичні властивості |
|
|
|
|
|
|
|
Агрегатний стан — тверді, Колір |
||
|
кристалічні |
|
|
|
Запах |
Розчинність у воді |
|
|
Смак солодкий |
Високі t°пл. |
|
|
|
|
|
Хімічні властивості
Амінокислоти — органічні амфотерні сполуки.
1.Взаємодія з основами — кислотні властивості
R − COOH + NaOH →
NH2
2.Взаємодія з кислотами — основні властивості
R − COOH + HCl →
NH2
3.Дисоціація
R− COOH
(біполярний йон)
NH2
4.Утворення пептидного зв’язку (реакція поліконденсації)
R1 − COOH + NH2 − R2 − COOH →
NH2 (____________________)
Одержання
1.Гідроліз білків: білок + H2O → амінокислоти
2.Із галогенопохідних карбонових кислот
R − CH− COOH+ NH3 →
Сl
Поширення у природі й біологічна роль
yyУчасть у обміні речовин.
yyСинтез білка (у синтезі беруть участь близько 20 різних аміно кислот у різних комбінаціях, з них 8 — незамінні).
Білки
Це |
|
|
, |
||
які складаються з |
|
, |
|||
пов’язаних |
|
|
зв’язками. |
||
76 |
Опорні конспекти та дидактичні матеріали з органічної хімії |
|
|
Класифікація білків
Протеїни — під час гідролізу дають тільки амінокислоти. (Аль буміни, глобулін)
Протеїди — під час гідролізу дають амінокислоти й неорганіч ні сполуки. (Фосфопротеїди)
Структура білка
Первинна
ланцюг, який складається з , пов’язаних пептидними зв’язками.
|
|
|
|
H R′ |
|
|
|
|
|
||||
H |
|
O |
|
|
H |
|
O |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
||
N |
C |
C |
N |
|
C |
||||||||
|
C |
|
|
N |
C |
|
|
C |
|||||
|
H R |
|
|
|
|
|
|
|
|
H R″ |
|||
|
|
|
H |
O |
|
|
|||||||
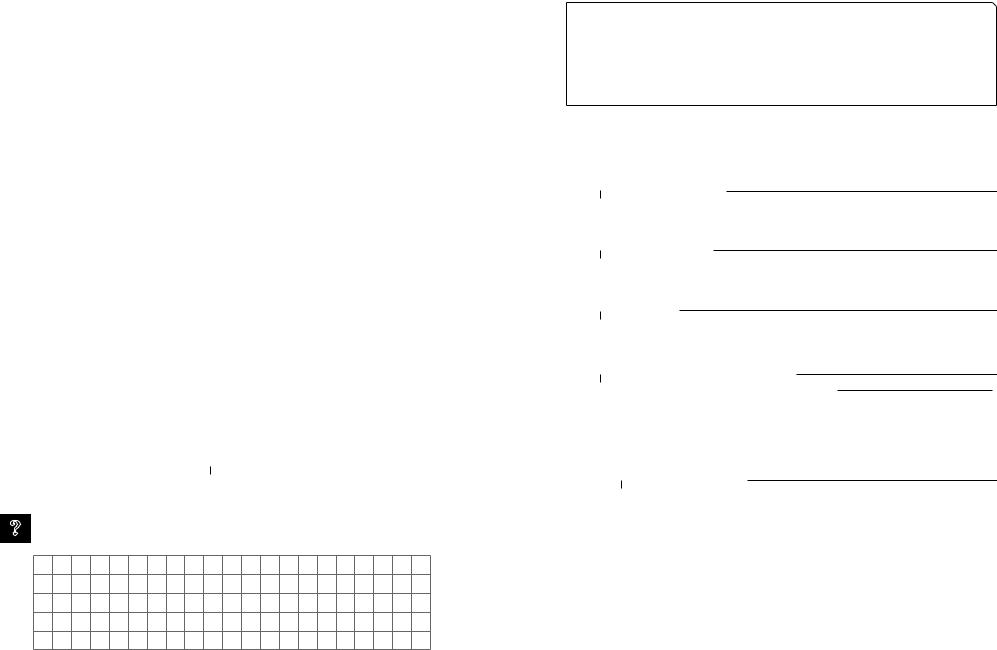
Вторинна
ланцюг, утворений із первинної структури за рахунок водневих зв’язків.
O |
|
|
|
|
R |
|
|
|
|
|
|
H |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
H |
|
|
|
|
C2 |
|
C |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
N |
|
R3 |
||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
N |
|
|
|
|
C |
|
O |
C |
|
N |
H |
|
C |
||||||
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
H |
|
H |
|
|
C |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
R R6 |
|
|
|
|
|
|
||
|
|
|
|
|
|
O |
|
N |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
1 |
|
|
|
|
H O |
||||||
|
|
C |
|
|
|
|
|
|
|
C |
C |
|
|||||||
|
|
|
H |
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
R C |
|
|
|
|
|
|
|
|
|
|
|
|
N H |
||||||
5 O |
|
|
|
|
|
|
|
O |
|
||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
N |
|
C |
|
C |
|
|
|
|
|
|
|||
|
|
H |
|
|
|
|
|
|
|
N |
|||||||||
|
|
|
|
R |
|
R4 |
H |
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
O |
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
C |
9 |
|
C |
|
|
|
|
|
|
|||
|
|
N |
|
|
|
|
|
|
N |
|
|
C R7 |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
C |
|
|
|
|
|
|
|
H |
|
O |
|
|
|
|
|||||
|
|
|
|
|
|
|
|
C |
|
|
C R10 |
||||||||
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
|
|||||
O |
|
|
|
|
|
N |
|
H |
|
|
|
|
|
|
|||||
|
|
|
|
|
R R8 |
C |
|
O |
R C |
||||||||||
|
|
|
|
|
|
|
|
||||||||||||
H |
|
|
|
C12 |
|
|
N |
|
|
||||||||||
|
|
|
|
|
|
|
13 |
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H C |
|
|
|
||
N |
|
|
|
|
|
|
|
O |
|
|
|
|
O |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
C |
|
H |
|
C |
N |
|
|
H |
||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
R11 |
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
N |
|
|
|
|
|
N |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
Теоретична частина |
77 |
|
|
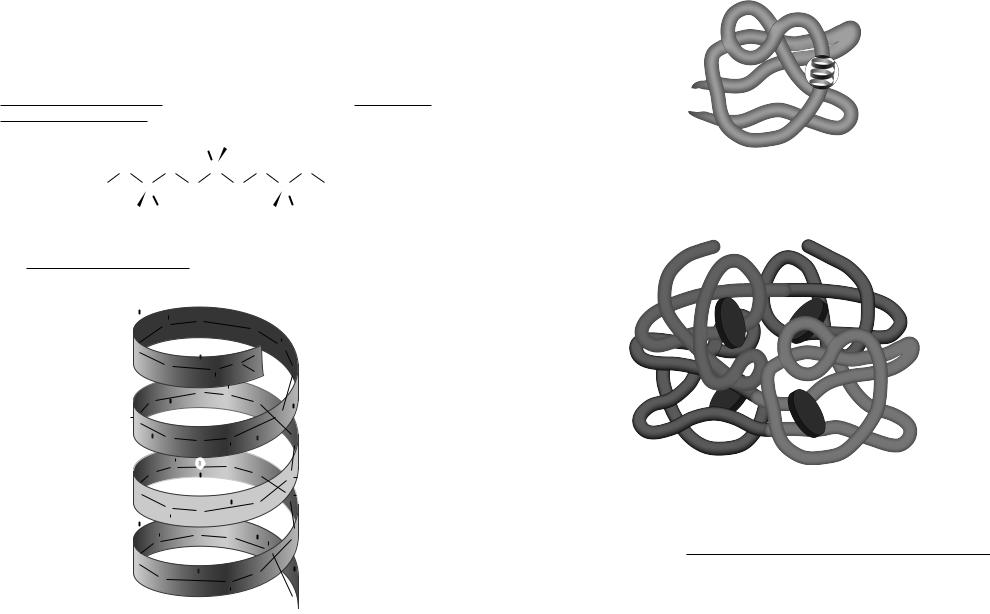
Третинна
Вторинна структура, «згорнута» у клубок (глобули, фібрили) за рахунок сульфідних зв’язків.
Четвертинна
Надмолекулярне утворення з декількох білків або з білків і ре човин небілкової природи.
Хімічні реакції білків
1.Гідроліз Білок + вода →
2.Денатурація Руйнування будь-якої структури до первинної.
Може бути оборотною й необоротною.
78 |
Опорні конспекти та дидактичні матеріали з органічної хімії |
|
|
Чинники, які зумовлюють денатурацію:
3.Якісні реакції
yyБілок + HNO3 → жовтий колір (ксантопротеїнова) yyБілок + CuSO4 + NaOH → темно-синій осад (біуретова) yyБілок + CH3 (COO)2 Pb → чорний осад
Біологічні функції
Структурна — утворення мембран клітин та інших тканин. Регуляторна — регулювання обміну речовин.
Захисна — антитіла, фібриноген.
Транспортна — приєднання й перенесення речовин у організмі. Скоротлива — здійснення всіх видів руху.
Запасальна — резерв для організму. Енергетична — 1 г білка — 17 кДж.
Ферментативна — прискорення біохімічних реакцій у клітині. У процесі біосинтезу білка в поліпептидний ланцюг включа
ються тільки α-амінокислоти:
yyті, що синтезуються в організмі; yyнезамінні.
Полімери
Полімер (з грецьк. πολύ- — багато; μέρος — частина) — речови на з великою молекулярною масою, яка складається з багаторазово
повторюваних ланок (структурна або елементарна ланка). |
|
Мономер — речовина, з якої одержують |
. |
Теоретична частина |
79 |
|
|
Класифікація
Лінійні
За формою макромолекул
Полімерні сітки
Розгалужені
По відношенню |
|
|
|
|||
|
|
Термопластичні під час нагрівання |
||||
до нагрівання |
|
|
|
|
розм’якшуються, плавляться, а під |
|
|
|
|
|
|||
|
|
|
|
|
|
час охолодження тверднуть |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Термореактивні під час нагрівання піддаються необоротному хімічному руйнуванню без плавлення
За способом одержання Природні
полімери
Штучні полімери одержують із природних полімерів
Гума
Синтетичні полімери одержують із органічних Ацетатне волокно
низькомолекулярних сполук
Полівінілхлорид
Поліметилметакрилат
«оргскло»
Полістирол