Материал: Опорні конспекти та дидактичні матеріали з органічної хімії

50 |
Опорні конспекти та дидактичні матеріали з органічної хімії |
||
|
|
|
|
|
|
|
|
Характеристики |
Гліцерин |
Етиленгліколь |
|
|
|
|
|
У воді |
|
Розчинний |
Розчинний |
|
|
|
(гігроскопічний) |
|
|
|
|
Для людини |
|
Не небезпечний |
Токсичний |
|
|
|
|
Хімічні властивості
1.Спільні з одноатомними спиртами
|
|
CH2 |
− |
CH − |
CH2 |
+3Na → |
|
|
+ |
|
|
|
|
|
|
|
|
(натрій тригліцерат) |
|
OH |
OH OH |
|
|
||||||
|
|
|
|
||||||
|
|
CH2 |
− |
CH − |
CH2 |
+3HCl → |
|
|
+ |
|
|
|
|
|
|
|
|
1,2,3-трихлорпропан |
|
OH |
OH OH |
|
|
||||||
2.Якісна реакція
|
CH2 |
− |
CH − |
CH2 + Cu(OH)2 |
→ |
|
|||
(темно-фіолетовий розчин) |
|||||||||
|
|
|
|
|
голубий осад |
|
|
||
OH |
OH OH |
|
|
||||||
|
|
|
|
||||||
3. Нітрування |
|
|
|
|
|||||
|
CH2 |
− |
CH − |
CH2 + HNO3 → |
|
|
|
||
|
|
|
|
|
|
|
|
(тринітрогліцерин) |
|
OH |
OH OH |
|
|
|
|||||
|
|
|
|
||||||
Одержання
1.CH2 = CH2 + H2O кип’ятiння з KMnO4→
2.CH2 − CH − CH2 + NaOH водний розчин→
Сl Сl Сl
3.CH2 = CH2 − CH3 + H2O кип’ятiння з KMnO4→ _
Застосування
Етиленгліколь
yyЯк компонент автомобільних антифризів і гальмових рідин; yyу виробництві полімерів;
yyяк розчинник;
yyв органічному синтезі; yyдля поглинання води.
Гліцерин
yyХарчова промисловість; yyмедицина;
Теоретична частина |
51 |
|
|
yyвиробництво мийних і косметичних засобів; yyтекстильна, паперова й шкіряна галузі промисловості; yyвиробництво пластмас;
yyлакофарбова промисловість.
Тринітрогліцерин
yyВ 1 %-му спиртовому розчині — для купірування гострих нападів спазмів коронарних судин;
yyодержання динаміту (вибухотехніка).
Феноли
Загальна формула
Ізомерія
Номенклатура
1.Назва радикала + фенол.
2.Тривіальні назви:
орто-крезол |
; |
|
|
|
|
мета-крезол |
; |
|
пара-крезол |
|
. |
Скласти ізомери й дати їм назви за номенклатурою ІЮПАК для формули C8H9OH.
52 Опорні конспекти та дидактичні матеріали з органічної хімії
Фенол
Молекулярна формула |
. |
|||||||||||||||||||||
Структурна формула |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Фізичні властивості
Агрегатний стан — рідина |
|
Колір — |
|
|
|||||||
t°пл |
|
|
|
t°кип |
|
|
|
|
|||
У холодній воді |
, Запах — різкий |
|
|
||||||||
у гарячій воді розчинний |
|
Під час зберігання рожевіє |
|||||||||
|
|
|
|
|
|||||||
Дія на організм людини |
|
|
|
|
|
|
|
|
|||
Знищує мікроорганізми (антисептик) |
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
||
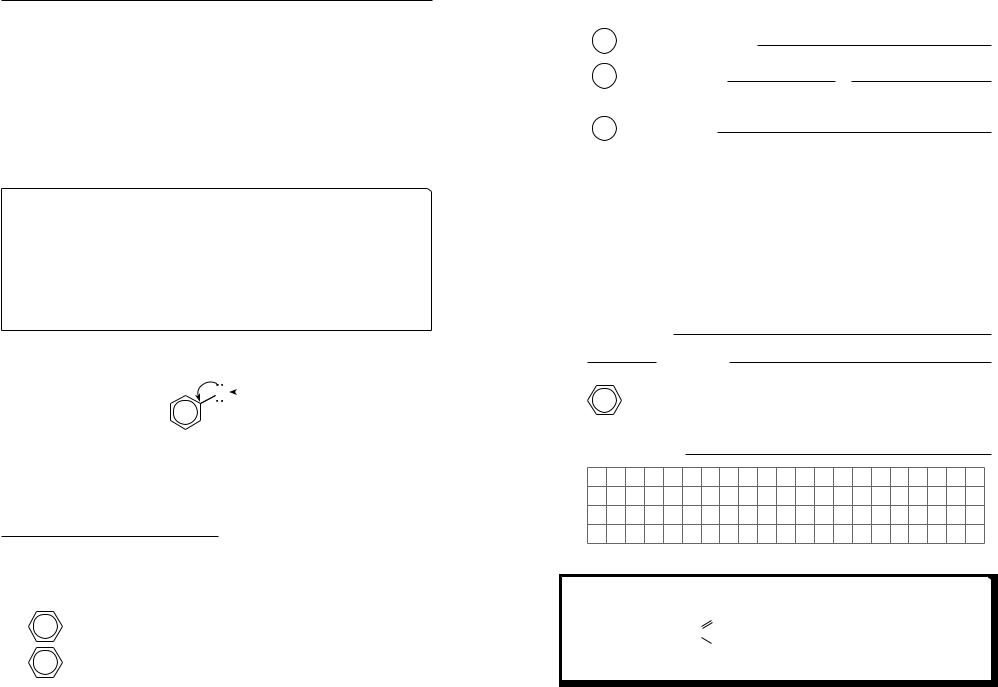
Взаємовплив груп атомів у молекулі фенолу |
|
|
|||||||||
|
|
|
|
|
|
|
|
δ+ |
|
|
|
|
|
|
δ- |
|
O |
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
δ- |
δ- |
|
|
|
|
||||
Бензенове кільце взаємодіє з електронами атома О, роблячи |
|||||||||||
зв’язок O− H більш |
|
|
|
|
|
|
|
|
. |
||
Можливість відділення атома Н від атома О |
|
|
. |
||||||||
Зростає |
|
|
|
|
|
|
|
|
. |
||
Електрони атома О, притягаючись до бензенового |
кільця, |
||||||||||
____________________________ його електронну густину, у ре
зультаті положення 2,4,6, стають |
|
. |
||||||
Хімічні властивості |
|
|||||||
1. За групою OН |
|
|||||||
−OH + Na → |
___________________ |
+ |
|
|
|
|||
|
|
(натрій фенолят) |
|
|||||
−OH + NaOH → _________________ + |
|
|||||||
|
|
|
|
|
|
|
|
|
Теоретична частина |
53 |
|
|
2. За бензеновим кільцем
 −OH +3Br2 → 3HBr +
−OH +3Br2 → 3HBr +
(2,4,6-трибромфенол, білий осад)
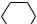 −OH+3HNO3 → ______________ +
−OH+3HNO3 → ______________ +
(тринітрофенол)
3. Якісна реакція
 −OH + FeCl3 →
−OH + FeCl3 →
(темно-фіолетове забарвлення)
Застосування
У виробництві: yyполімерів; yyлікарських препаратів; yyбарвників;
yyповерхнево-активних речовин; yyантисептиків;
yyвибухових речовин.
Одержання
1.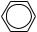 +Cl2 →
+Cl2 →
_________ +NaOH →
2.Кумольний метод
+CH2 = CH − CH3 → |
|
|
|
(кумол) |
|
|
|
||
[ ] |
|
|
||
|
|
O , H2O |
|
|
______________________ → |
|
|||
|
|
|
|
|
3. 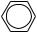 +H2O2 →
+H2O2 →
Альдегіди
Загальна |
CnH2n+1 — |
|
|
|||||
|
|
|||||||
формула |
|
|
|
|
|
|||
|
|
|
O |
|||||
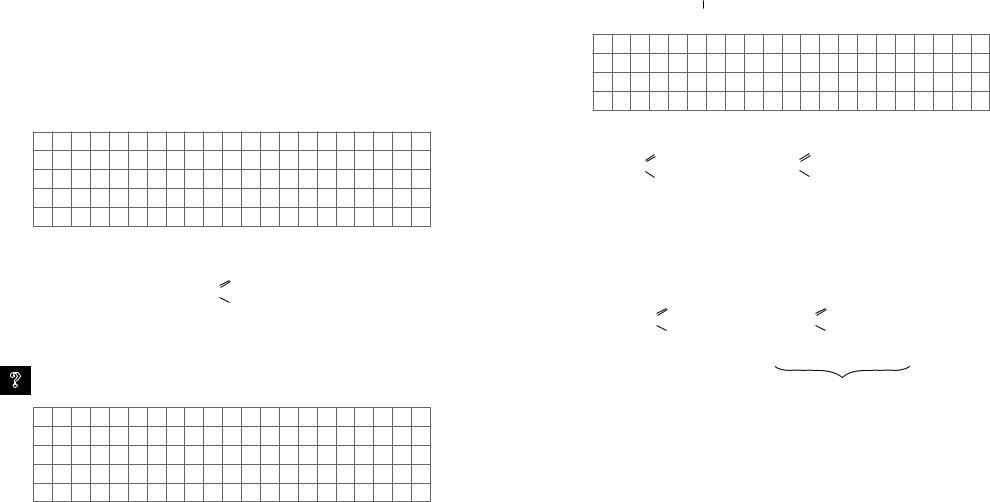
CnH2n+1CHO |
|
|
|
|
|
— карбонільна група |
||
|
C |
|||||||
|
||||||||
(CnH2nO) |
|
|
|
H |
|
|||
|
|
|
|
|
|
|
група альдегідів |
|
(натрій фенолят)
54 |
|
Опорні конспекти та дидактичні матеріали з органічної хімії |
|||||
|
|
|
|
|
|
|
|
|
Номенклатура |
|
|
|
|
||
|
Нумерація головного карбонового ланцюга — з атома C функ |
||||||
ціональної групи. |
|
|
|
|
|||
|
Назва вуглеводню + |
. |
|||||
|
Тривіальні назви |
|
|
|
|
||
|
НСОН — |
|
мурашиний альдегід, або формальдегід. |
||||
|
|
|
|
|
|
|
|
|
CH3COH — |
|
|
|
оцтовий альдегід, або ацетальдегід. |
||
|
|
|
|
||||
Ізомерія
Будова |
|
|
|
|
|
|
|
|
|
|
|
O |
|||
|
|
R |
|
C |
|||
|
|
|
|||||
|
|
|
|
OH |
|||
Гібридизація C |
. |
||||||
|
|
|
|
|
|
|
|
Види зв’язків: |
|
|
|
|
. |
||
Валентний кут: |
. |
||||||
|
|
|
|
|
|
|
|
Скласти ізомери й дати їм назви за номенклатурою ІЮПАК для формули C5H10O.
Фізичні властивості
НСНО — газ із характерним запахом, розчинний у воді, 40 %-й розчин у воді — формалін. Токсичний.
CH3CHO — рідина з характерним запахом, розчинна у воді, токсична.
Теоретична частина |
55 |
|
|
Хімічні властивості
1.Реакції відновлення (розрив зв’язку C = O)
R −C = O+ H2 t, p, k→R −CH2 −OH
H
2.Реакції окиснення (розрив зв’язку C− H)
Якісні реакції на альдегіди |
O |
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
O |
+ 2Cu(OH) t→R − C |
|
|
|
|
|
|
|
|
||||||||
a) R − C |
|
|
+ Cu2O ↓ + 2H2O |
|||||||||||||||||
|
|
|
H |
2 |
|
|
|
OH |
оранжевий |
|||||||||||
|
|
|
голубий осад |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
осад |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
б) Реакція «срібного дзеркала» |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
O |
|
|
O |
|
|
|
|
|
|
|
|||||||||
|
R −C + Ag2O →R −C |
|
+2Ag ↓ + H2O |
|||||||||||||||||||
|
|
|
|
|
|
|
t, NH4OH |
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
H |
|
|
OH |
|
|
|
|
|
|
|
|||||||||
|
|
(AgNO3 + NH4OH → Ag2O + H2O + NH4NO3 ) |
||||||||||||||||||||
2 |
Ag(NH ) |
OH |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
3 2 |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Застосування
НСНО:
yyУ виробництві феноло-формальдегідних смол; yyдля синтезу ліків і барвників;
yyдля дублення шкір;
yyяк дезінфікуючий, антисептичний засіб.
56 |
Опорні конспекти та дидактичні матеріали з органічної хімії |
|
|
CH3CHO :
yyОдержання оцтової кислоти; yyодержання етилового спирту.
Одержання
1.Лабораторний метод
|
|
|
|
|
|
O |
|
|
|
|
|
t |
+ Cu ↓ +H2O |
|
R −CH2 −OH + CuO →R −C |
|||||
|
|
|
|
|
|
H |
2. Промислові способи |
|
|||||
CH ≡ CH + H2O → |
|
|
|
|||
|
|
|
||||
|
t, p, k |
|
||||
CH4 |
+ O2 → |
|
|
|
|
|
CH2 |
= CH2 + O2 k→ |
|
|
|||
|
|
|||||
|
k |
|
||||
CH3OH + O2 → |
|
|
||||
|
|
|||||
Карбонові кислоти
Загальна |
R — |
|
|
||
формула |
O |
|
|
||
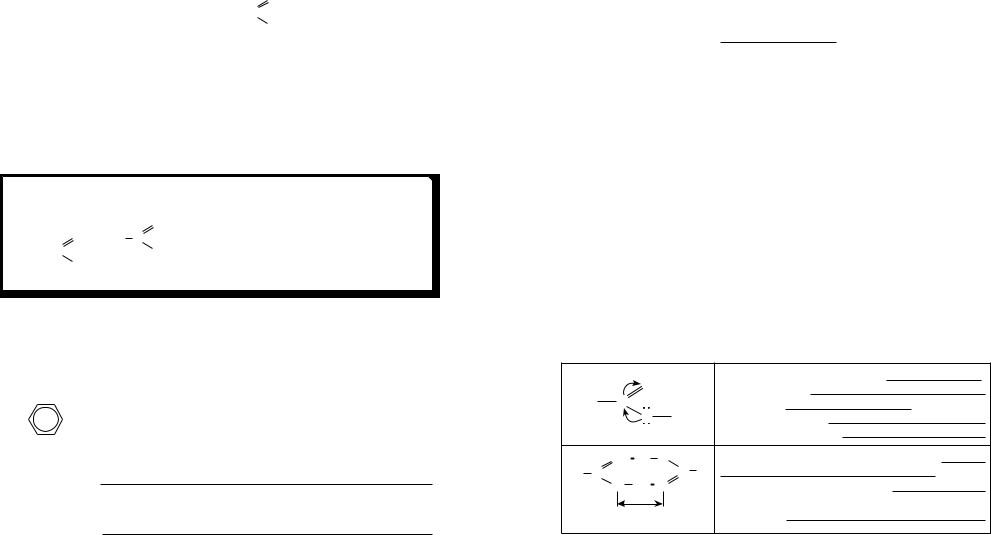
OC — карбоксильна група
R |
|
|
|
|
OH |
|
||||
C |
||||||||||
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
група кислот |
|
Класифікація |
|
|
|
|||||||
|
|
|
|
|||||||
Теоретична частина |
57 |
|
|
Насичені одноосновні карбонові кислоти
Загальна формула
CnH2n+1COOH
(CnH2nO2 )
Номенклатура
Нумераціяголовноголанцюга—затомаCфункціональноїгрупи. Назва вуглеводню + _______________ кислота.
|
Назва за |
Тривіальні |
Формула |
Назва |
|
Формула |
номенклату- |
кислотного |
кислотного |
||
назви |
|||||
|
рою ІЮПАК |
залишку |
залишку |
||
|
|
||||
|
|
|
|
|
|
НСООН |
|
Мурашина |
|
|
|
|
|
кислота |
|
|
|
|
|
|
|
|
|
CH3COOH |
|
Етанова |
|
|
|
|
|
кислота |
|
|
|
|
|
|
|
|
|
C2H5COOH |
|
Пропіонова |
|
|
|
|
|
кислота |
|
|
|
|
|
|
|
|
|
C3H7COOH |
|
Олійна |
|
|
|
|
|
кислота |
|
|
|
|
|
|
|
|
|
C4H9COOH |
|
Валеріанова |
|
|
|
|
|
кислота |
|
|
|
|
|
|
|
|
1. |
За вуглеводневим радикалом |
|
Будова |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|||
|
CnH2n+1COOH — насичені |
|
|
|
δ- |
|
|
Найбільш полярний зв’язок |
. |
|
|
CnH2n 1COOH, CnH2n 3COOH — ненасичені |
|
|
δ+ |
O |
|
|
Розрив зв’язку |
|
|
|
−COOH ароматичні |
|
R |
C |
O- |
H+ |
|
спричиняє |
властивості. |
|
|
|
|
|
|
Чим довше R, тим |
|
||||
2. За кількістю груп СООН |
|
|
|
|
|
|
кислотні властивості |
|
||
|
|
O |
H |
O |
|
Між молекулами кислот утворюється |
||||
|
R− COOH одноосновні |
|
|
R |
||||||
|
R(COOH)2 |
R |
C |
O H |
C |
|
зв’язок. |
|||
|
O |
|
Температури кипіння кислот |
|
||||||
3. |
За кількістю атомів Карбону |
|
|
|
|
|||||
|
|
|
|
|
|
температур кипіння відповідних спиртів |
||||
|
C1 − C14 |
— нижчі |
|
|
|
|
|
|
||
|
|
|
0,26 нм |
|
і альдегідів |
|
||||
|
C15 − C18 |
— |
|
|
|
|
|
|
|
|

58 |
Опорні конспекти та дидактичні матеріали з органічної хімії |
|
|
Ізомерія
Скласти ізомери й дати їм назви за номенклатурою ІЮПАК для формули C5H10O2.
Фізичні властивості
yyНСООН — рідина з характерним запахом, t°кип. = 100,8 °C, роз чинна у воді, їдка.
yyCH3COOH — рідина, із запахом, t°кип. = 118,1 °C, розчинна у воді, їдка. 80 %-й розчин — оцтова есенція, 3–9 %-й роз
чин — столовий оцет.
Хімічні властивості
1.Спільні з неорганічними кислотами
RCOOH RCOO− + H+ (змінюють колір індикаторів)
RCOOH + Me(акт.) →
RCOOH + Me2Ox →
RCOOH+ MeOH →
RCOOH + MeCO3 →
Сила кислот (за зменшенням)
HCOOH → CH3COOH → C2H5COOH →
2.Характерні для карбонових кислот Реакція етерифікації
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
O |
||||||||
|
|
R1 |
− C |
+ HO − R2 R1 − C |
|
|
+ H2O |
|||||||||||||||
|
|
|
|
|
|
OH |
|
|
|
|
складний ефiр O – R2 |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3.Галогенування
CH3 −COOH + Cl2 hν→CH2Cl −COOH + HCl
Теоретична частина |
59 |
|
|
Мурашина кислота
Альдегідокислота — біфункціональна сполука (містить дві функціональні групи)
Карбоксильна |
Карбонільна |
|
група |
||
група |
||
|
Якісна реакція
HCOOH + Ag2O →
HCOOH t, H2SO4→H2O + CO
Поширення у природі
НСООН — у хвої ялини, кропиві, фруктах, їдких виділеннях бджіл і мурах.
CH3COOH — є продуктом шумування вина.
C2H5COOH — знайдено в нафті, утворюється під час шумуван ня вуглеводів.
C3H7COOH та її етери містяться у коров’ячій олії й нафті.
Одержання
1.Лабораторні методи
CH3COONa + H2SO4 →t CH3COOH + NaHSO4
RCHO+ Cu(OH)2 →
RCHO+ Ag2O →
2.Промислові методи
RCOH [O]→RCOOH
CH4 + O2 t, p, k→
R −CH2 −OH + O2 t, k→
CO + NaOH t, p→HCOONa + H2SO4 →t HCOOH + NaHSO4
3.Оцтовокисле шумування
C2H5OH бактерiї→CH3 − COOH
Застосування
НСООН — для синтезу естерів, консервування соків. CH3COOH — у харчовій промисловості (харчова добавка E260)
і побутової кулінарії, а також у консервуванні, для одержання лі карських і запашних речовин, як розчинник.