Материал: Опорні конспекти та дидактичні матеріали з органічної хімії
60 |
Опорні конспекти та дидактичні матеріали з органічної хімії |
|
|
C2H5COOH
1.У виробництві: yyгербіцидів; yyлікарських засобів; yyзапашних речовин; yyпластмас; yyрозчинників.
2.Як консервант у продуктах.
Естери (складні ефіри)
|
|
Загальна |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
O |
||||||||||||||||||||||||
|
|
|
формула |
|
R1 |
|
|
C |
|
|
|
— залишок від карбонової кислоти |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O – |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
||||||||||||||||||
R |
|
|
|
|
|
|
|
R2 — залишок від |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
1 |
|
C |
|
O – R2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
(CnH2nO2 ) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ізомерія |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Номенклатура
1.Назва R2 + назва кислотного залишку R1COOH.
2.Назва R2 + овий ефір + назва R1COOH.
 Скласти формули естерів для молекулярної формули C5H10O2 .
Скласти формули естерів для молекулярної формули C5H10O2 .
Теоретична частина |
61 |
|
|
Фізичні властивості
yyРідини; yyіз запахом;
yyнерозчинні у воді; yyрозчинники.
Застосування
yyРозчинники; yyпластифікатори; yyароматизатори; yyвиробництво ліків.
Хімічні властивості
Гідроліз |
|
O |
|
R1 − C |
+ H2O → |
O – R2 |
|
Одержання |
|
|
реакція етерифікації |
||||||||
|
Жири |
||||||||
|
Жири — складні ефіри (естери) |
|
|||||||
і |
__________________________. |
||||||||
|
Загальна формула |
|
|||||||
|
|
|
|
|
|
||||
|
|
|
O |
||||||
|
|
CH2 – O – C |
|
|
– R1 |
|
|||
|
|
|
|
||||||
|
|
|
|
|
|
||||
|
|
|
O |
||||||
|
|
CH – O – C |
|
– R2 |
|
||||
|
|
||||||||
|
|
|
|
|
|
||||
|
|
|
O |
||||||
|
|
CH2 – O – C |
|
– R3 |
|
||||
|
|
|
|
||||||
|
C3H5 (R1COO)(R2COO)(R3COO) |
||||||||
Номенклатура
1.R1 = R2 = R3
три + назва кислотного залишку,
2.R1 = R2 = R3
гліцерид + назва кислот
62 |
Опорні конспекти та дидактичні матеріали з органічної хімії |
|
|
C17H35COOH — стеаринова кислота (C17H35COO)− — стеарат
C17H33COOH — олеїнова кислота (C17H33COO)− — олеат
C15H31COOH — пальмітинова кислота (C15H31COO)− — пальміат
Скласти формули жирів: а) триолеат;
б) тристеарат;
в) трипальміат.
Фізичні властивості жирів
1.Агрегатний стан.
yyТверді (тваринні) _______________________вищі насичені кислоти (вершкова олія, тваринні жири, сало) (виняток — риб’ячий жир);
yyрідкі (рослинні) ______________ вищі ненасичені кислоти (со
няшникова олія, маслинова олія) (виняток — кокосова олія).
Теоретична частина |
63 |
|
|
2.Гідрофобні (гідрофобія — «боязнь» води).
3.Розчинні в органічних розчинниках.
Хімічні властивості
|
O |
|
|
|
|
|
||
CH2 – O – C |
|
– R1 |
+O2 → |
|
|
|
||
|
||||||||
|
H+ |
|||||||
|
|
|
|
|
||||
|
|
|
|
|||||
|
O |
|
+ H2O → |
|
||||
|
|
|
(кислотний гідроліз) |
|||||
CH – O – C – R2 |
|
|
|
|||||
|
|
|
|
|||||
|
|
|
|
|
|
|
||
|
O |
+ NaOH → |
|
|||||
|
|
|
|
|||||
CH2 – O – C – R3 |
||||||||
|
(лужний гідроліз — омилення) |
|||||||
Гідрування (одержання твердих жирів із рідких)
C3H5 (C17H33COOH)3 + 3H2 →
Якісне визначення рослинних (ненасичених) жирів
C3H5 (C17H33COOH)3 + 3Br2 →
Застосування
yyХарчова промисловість; yyфармація;
yyвиробництво мила й косметичних виробів; yyвиробництво мастильних матеріалів.
Одержання
Гліцерин + вищі карбонові кислоти
|
O |
|
|
|
|
|
||
R1 – O – C |
|
|
– R1 |
|
|
|
HO – CH2 |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
||
|
O |
|
|
|
|
|||
R2 – O – C |
|
– R2 |
|
|
|
HO – CH |
||
|
|
|
|
|||||
|
|
|
|
|||||
|
|
|
|
|
|
|
||
|
O |
|
|
|
|
|||
R3 – O – C |
|
– R3 |
|
|
|
HO – CH2 |
||
|
|
|
|
|||||
C3H5 (OH)3 + R1COOH + R2COOH + R3COOH →
64 |
Опорні конспекти та дидактичні матеріали з органічної хімії |
|
|
Біологічна роль жирів
Жири входять до складу всіх рослинних і тваринних клітин. Запасні жири відкладаються в підшкірній клітковині й у сальни ках і є джерелом енергії. Плазматичні жири входять до складу більшості мембран. Жири мають високу енергетичну цінність (під час повного окиснення 1 г жиру виділяється 37,7 кДж). Завдяки низькій теплопровідності жири відіграють важливу роль у тепло регуляції. Завдяки своїй еластичності жири відіграють захисну роль у шкірі. Жири — необхідна складова частина їжі. Норма спо живання дорослою людиною — 80–100 г/добу.
Теоретична частина |
65 |
|
|
CH |
(CH ) COONa = CH |
(CH ) |
COO− + Na+ |
||||||
|
3 |
|
2 |
16 |
3 |
|
2 |
16 |
|
|
|
натрiй стеарат |
|
стеарат iон |
|||||
CH |
(CH ) |
COO− + H |
O = CH |
(CH ) COOH+ OH− |
|||||
3 |
|
2 |
16 |
2 |
|
3 |
|
2 |
16 |
|
стеарат iон |
|
стеаринова кислота |
||||||
Молекули кислоти, що утворилася під час гідролізу мила, дов гою гідрофобною частиною оточують краплю або частинку жиро вого забруднення, а гідрофільні групи СООН звернені у воду. Тому частинки бруду переходять у воду.
У жорсткій воді:
CH3 (CH2 )16 COO− + Ca2+ → (CH3 (CH2 )16 COO)2 Ca ↓
Мила |
|
|
|
Тверде мило — C17H35COONa, рідке — C17H35COOK. |
|
||
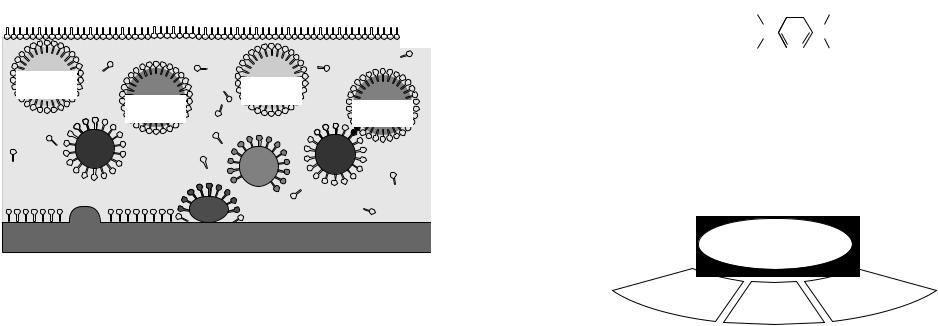
Мийна дія мила |
|
|
|
|
|
|
ж |
е |
|
д |
|
|
|
|
|
повітря |
е |
повітря |
е |
|
|||
|
|
|
|
|
повітря |
|
повітря |
|
|
|
|
г |
|
г |
|
|
|
|
|
|
|
в |
|
а |
|
б |
|
|
|
|
|
Синтетичні мийні засоби
Це сполуки, які містять насичений вуглеводний ланцюг із 10–15 атомів Карбону, так чи інакше пов’язаний із сульфатною або сульфонатною групою, наприклад:
HO
CH3 |
− (CH2 ) |
− C − |
|
|
−S − O−Na+ |
|
|
9 |
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
CH3 |
|
|
||
Переваги перед милом: однаково добре миють як у м’якій, так і в жорсткій воді. Діють не тільки в гарячій воді, але й у воді за порівняно низьких температур, що важливо для прання тканин зі штучних волокон. Зрештою, концентрація синтетичних мийних речовин навіть у м’якій воді може бути набагато нижче, ніж мила, отриманого із жирів.
Вуглеводи
|
|
|
Загальна формула |
|||
|
|
Cn (H2O)m , n, m ≥ 3 |
||||
Мийний процес |
|
|
|
|
|
|
|
|
|
|
|
|
|
а — частка бруду на поверхні матеріалу; |
|
моносахариди |
|
|
|
полісахариди |
|
|
|
|
|||
б — адсорбція мийної речовини на частці бруду; |
|
|
|
|
||
|
|
|
дисахариди |
|
|
|
в — відрив частки бруду від забрудненої поверхні; |
|
|
|
|
|
|
|
|
|
|
|
|
|
г — частка бруду в мийному розчині; |
|
|
|
|
|
|
|
|
|
|
|
|
|
д — пухирці повітря з адсорбованими молекулами мийної речовини |
|
|
|
|
|
|
(піна); |
Глюкоза (моносахарид) |
|||||
е — злиплі пухирці піни й частки бруду; |
Формула |
|
|
|
|
|
ж — адсорбційний прошарок мийного розчину на межі розподілу пові |
|
|
|
|
||
тря — вода. |
|
|
|
C6H12O6 |
||
66 |
|
|
|
Опорні конспекти та дидактичні матеріали з органічної хімії |
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Будова |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
OH |
O |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
CH2 – CH – CH – CH – CH – C |
|
— розгорнута форма. |
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
OH |
OH OH |
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
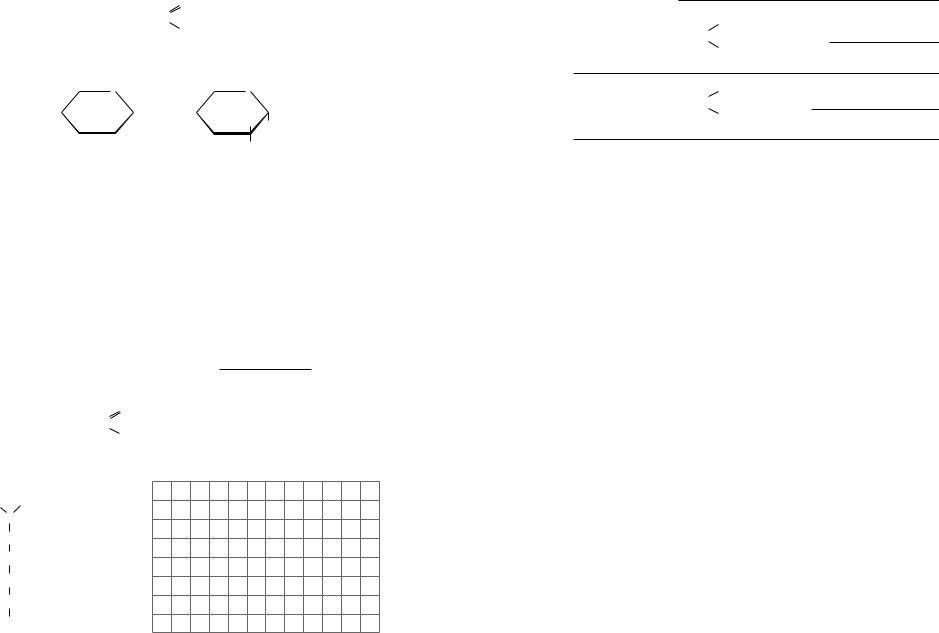
Глюкоза — альдегідоспирт |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
СH2OH |
|
|
|
СH2OH |
||||||||||||||||||
|
|
|
|
H |
|
|
|
|
|
O |
H |
|
H |
|
|
|
O |
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
||||||||||||||
|
|
|
|
H |
|
|
|
|
|
H |
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
OH |
|
H |
|
|
|
|
|
|
|
OH |
H H |
||||||||||
|
|
|
|
HO |
|
|
|
OH |
|
HO |
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
OH |
|
|
|
H |
OH |
||||||||||||||
|
|
|
|
|
|
α-глюкоза |
|
β-глюкоза |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
Циклічна форма |
|
|
|
|
|
|
||||||||||
Фізичні властивості |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
Агрегатний стан |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
. |
|||||||||||
Тверда, кристалічна речовина білого кольору, солодка на смак. У воді добре розчинна.
|
Хімічні властивості |
|
|
1. |
Повне окиснення |
|
|
|
C6H12O6 + O2 → |
|
+ |
|
|
||
2. |
Відновлення |
|
|
CH2OH − (CHOH)4 |
O |
|
|
− C + H2 → |
|
сорбіт |
|
|
H |
|
|
3.Якісні реакції 1) Як на багатоатомний спирт
HО
С H – C – OH
H – C – OH
HO – C – H +Cu(OH)2 → H – C – OH
H – C – OH CH2OH
Теоретична частина |
67 |
|
|
2) Як на альдегід
C6H12O6 + Cu(OH)2 →
O
а) CH2OH −(CHOH)4 − C + Cu(OH)2 t°→
+ Cu(OH)2 t°→
H
O
б) CH2OH −(CHOH)4 − C + Ag2O t °→
+ Ag2O t °→
H
Шумування
C6H12O6 |
→ |
|
|
|
+ |
|
|
|
||
|
|
|
спиртове шумування |
|
|
|||||
C6H12O6 |
→ |
|
|
+ |
|
|
|
+ |
|
|
|
|
|
олійнокисле шумування |
|||||||
C6H12O6 |
→ |
|
|
|
|
|
|
|
||
молочнокисле шумування |
||||||||||
|
|
|
||||||||
Поширення у природі
У соку багатьох фруктів і ягід, у тому числі й винограду, че рез що глюкозу й називають виноградним цукром. В організмі лю дини.
Біологічна роль
В організмі людини й тварин глюкоза є основним і найбільш універсальним джерелом енергії для забезпечення метаболічних процесів.
Застосування
Як продукт харчування, у медицині (антитоксичний засіб).
Одержання
Фотосинтез
6CO2 +6H2O → C6H12O6 +6O2↑
Синтез Бутлерова
6HCOH → C6H12O6
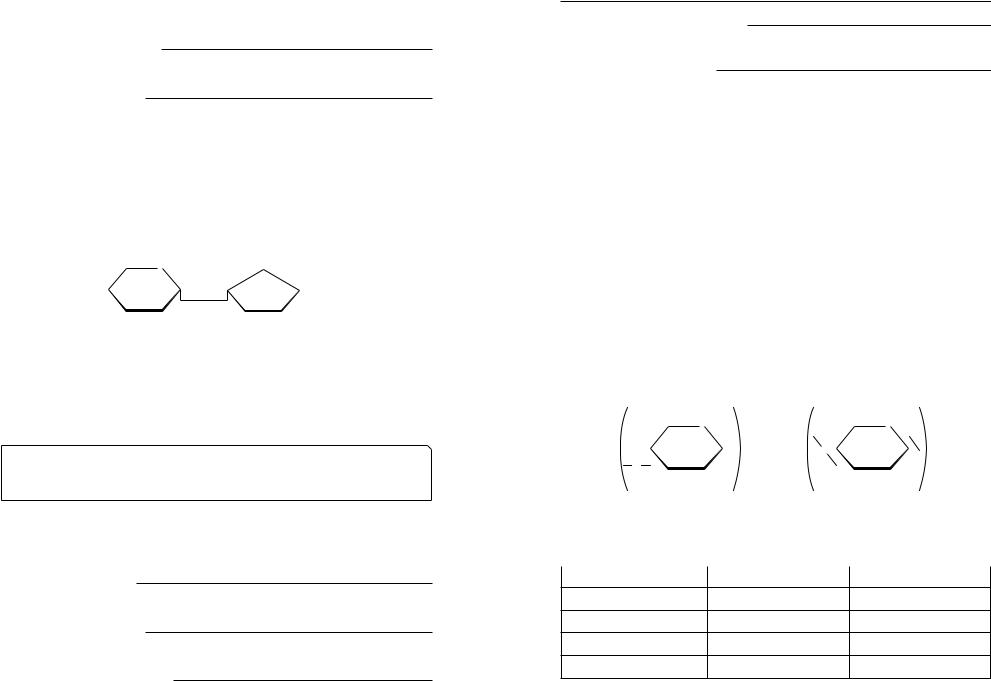
68 |
Опорні конспекти та дидактичні матеріали з органічної хімії |
|
|
Гідроліз крохмалю або целюлози
(C6H10O5 )n + nH2O →
Гідроліз сахарози
C12H22O11 + H2O →
Сахароза
Формула
|
|
|
|
|
|
|
|
|
C12H22O11 |
|
|
|
|
||||||
Будова |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
СH2OH |
|
|
|
СH2OH |
|
|
|
|
|||||||||
H |
|
|
O |
|
H |
|
|
|
|
|
|
O |
|
|
OH |
||||
H |
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
OH |
H |
|
|
H HO |
|
|
|||||||||||
HO |
|
O |
СH2OH |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
H |
OH |
|
|
|
|
|
OH |
H |
|
|
|||||||
сахароза
Молекула сахарози складається з одного залишку глюкози й одного залишку фруктози.
Фізичні властивості
Агрегатний стан |
Колір |
Смак |
Розчинність у воді |
|
|
Хімічні властивості
1.Окиснення
C12H22O11 + O2 →
2.Гідроліз
C12H22O11 + H2O →
3.Якісна реакція
C12H22O11 + Cu(OH)2 →
Теоретична частина |
69 |
C12H22O11 + Cu(OH)2 →t
4.Обвуглювання концентрованою сульфатною кислотою
C12H22O11 + H2SO4 →
Поширення у природі
Міститься в цукровій тростині, цукровому буряку (до 28 % су хої речовини), соках рослин і плодах (наприклад, берези, клена, дині й моркви).
Застосування
Харчова промисловість, виробництво етанолу.
Одержання
Фотосинтез
12CO2 +12H2O → C12H22O11 +12O2↑
Полісахариди
Формула
|
|
|
|
|
|
|
|
|
|
(C6H10O5 )n |
|
|
|
|
|
|
|
|
|
|
|
Будова |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
СH2OH |
|
|
|
СH2OH |
|||||||||||||
|
|
H |
|
|
O |
|
|
|
|
|
O |
|
|
|
|||||||
|
|
|
|
H |
|
H |
|
|
|||||||||||||
|
|
H |
|
O |
H |
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
O |
|
|
|
OH |
H |
|
|
|
|
|
OH |
H |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
H |
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
OH n |
|
|
|
H |
OH n |
|||||||||||
|
|
|
Крохмаль |
|
|
|
Целюлоза |
||||||||||||||
Фізичні властивості |
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
Фізичні властивості |
|
|
|
|
Крохмалю |
|
|
|
|
|
|
Целюлози |
|||||||||
Колір
Смак
Розчинність у воді
Агрегатний стан