Материал: Опорні конспекти та дидактичні матеріали з органічної хімії
30 Опорні конспекти та дидактичні матеріали з органічної хімії
Дегідратація (відщеплення води) |
|
|
+H2O |
||||||
R − CH2 |
− CHOH − R → |
|
|
|
|
||||
|
|
H2SO4 , t |
|
|
|
|
|
||
Відщеплення галогенів (дегалогенування) |
|
|
|
||||||
R − CHCl − CHCl − R + Zn → |
|
|
|
|
+ZnCl2 |
||||
|
|
|
|
||||||
3. Реакція приєднання |
|
|
|
|
|
||||
Гідрування алкінів |
|
|
|
|
|
||||
R −C ≡ C−R + H2 → |
|
|
|
|
|
||||
|
|
t, k |
|
|
|
|
|
|
|
Умови перебігу реакцій |
|
|
|
|
|
||||
|
|
|
|
|
|
||||
−H2 |
|
−Cl2 |
|
–НCl |
−H2O |
||||
|
|
|
|
|
|
|
|
|
|
t°, каталізатор |
Активні метали |
|
+KOH (спирто |
H2SO4 (конц.), t |
|||||
(Ni, Pt) |
|
|
вий розчин) |
||||||
|
|
|
|
|
|
|
|
|
|
Застосування
Для синтезу етиленгліколю, етанолу.
Оксид етилену застосовують для синтезу різних органічних ре човин, виробництва оцтового альдегіду, лаків, пластмас, косметич них препаратів і т. д.
Алкіни
Загальна формула
Гомологічний ряд C2H2, C3H4, |
|
, |
|
. |
|
|
Види ізомерії
Теоретична частина |
31 |
|
|
Будова
Гібридизація атома С |
|
|
|
|
|
. |
|||||||
Види зв’язків: C− C |
|
|
|
|
C− H |
|
|
|
. |
|
|
||
Валентний кут: σ − σ |
|
|
|
|
σ − π |
|
|
. |
|
||||
Номенклатура
Суфікс у головному ланцюзі — локант потрійного зв’язку. Нумерація головного ланцюга з того кінця, де ближче кратний
зв’язок.
Фізичні властивості
Число атомів С |
|
Етин (ацетилен) — газ, без ко |
||||||||
t°пл |
|
|
|
|
льору, запаху, малорозчинний |
|||||
|
|
|
|
у воді, легше за повітря |
||||||
t°кип |
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
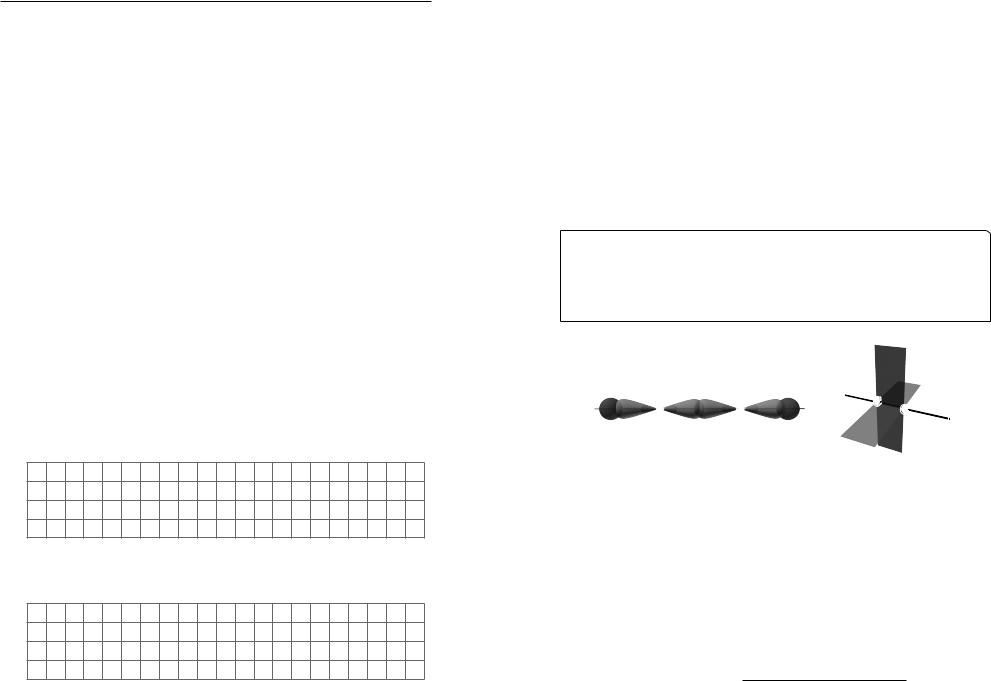
p |
|
|
H |
C |
|
|
H |
σ |
C |
C |
σ |
|
|
|
|
C |
|
||||||
|
|
|
|
|
||||||
|
|
|
|
|
H |
|
p |
|
|
H |
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
H− C ≡ C− H
Етин (ацетилен)
Хімічні властивості
1.Реакція окиснення
CnH2n2 + O2 → |
|
(горіння) |
|
2.Реакції приєднання
R − C ≡ C− R + H2 t, k→R − CH = CH − R
t, k |
(гідрування) |
R −C ≡ C−R +2H2 → |

32 |
Опорні конспекти та дидактичні матеріали з органічної хімії |
|
|
Галогенування
R − C ≡ C − R + Cl2 → R − C = C − R
Сl Сl
R − C ≡ C − R +2Cl2 →
Гідрогалогенування (за правилом Марковникова)
R − C ≡ C − R + HCl → R − CH = C − R
Сl
R − C ≡ C − R +2HCl →
Гідратація (реакція Кучерова)
2+
R −C ≡ C −R + H2O Hg →R −CH2 −C −R
O
3.Специфічні реакції ацетилену Одержання етаналю (оцтового альдегіду)
|
|
Hg2+ |
|
O |
|
|
|
|
−C |
||
HC ≡ CH + HOH →CH3 |
|||||
|
|
|
|
H |
|
Тримеризація |
|
|
|
|
|
t °C |
|
|
|
|
(бензен) |
3CH ≡ CH → |
|
|
|
|
|
Реакції заміщення атома Гідрогену біля потрійного зв’язку |
|||||
HC ≡ CH + 2 Ag(NH3 ) |
OH → Ag |
− C ≡ C − Ag+ 4NH3 + 2H2O |
|||
|
2 |
|
аргентум |
|
|
ацетиленiд
Лінійна полімеризація
HC ≡ CH + HC ≡ CH Cu2Cl2 80°С→HC ≡ C − CH = CH2
вiнiлацетилен (бут 1 ен 3 iн)
Поширення у природі
Не трапляється через активність молекули. Одержують шля хом синтезу.
Одержання
1.Крекінг метану
2СH4 →t
2.Дегідрування алкенів
R −CH = CH −R t, k→______ + ______
Теоретична частина |
33 |
|
|
3.Дегідрогалогенування
R − CH − CH − R +...→...+2KCl + H2O
Сl Сl
4.Відщеплення галогенів
R − CCl2 − CCl2 − R +...→...+...
5.Карбідний метод
CaC2 + H2O → CH ≡ CH + Ca(OH)2
кальцiй
карбiд
Одержання карбіду:
CaCO3 t→CaO +CO2; CaO +3C t→CaC2 +CO
Застосування
Ацетилен використовують для автогенного зварювання й рі зання металів. Для цього потрібні два балони з газами — з киснем і ацетиленом. Гази з балонів надходять у спеціальний пальник. Під час згоряння ацетилену в кисні виходить дуже гаряче полум’я; максимальної його температури (3200 °С) досягають за вмісту аце тилену 45 % за об’ємом.
Як джерело дуже яскравого, білого світла в автономних сві тильниках, де він утворюється під час узаємодії кальцій карбіду й води (карбідка).
Ацетилен використовують у виробництві вибухових речовин (ацетиленіди), для одержання етанової кислоти, етилового спирту, розчинників, пластичних мас, каучуку, ароматичних вуглеводнів.
Циклоалкани
Загальна формула
Гомологічний ряд _____, _______, ______.
34 |
|
Опорні конспекти та дидактичні матеріали з органічної хімії |
Теоретична частина |
35 |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
Форма запису головного ланцюга |
|
|
Скласти структурні формули ізомерів складу C6H12 |
й дати їм |
|||
|
|
|
|
|
|
|
назви. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
CH2 − CH2 =
CH2 − CH2
CH − CH3 |
= |
CH2 − CH2 |
|
Номенклатура
Положення замісників нумерують так, щоби сума локантів
була |
|
. |
|
Назва головного ланцюга |
|
. |
|
Ізомерія
Будова
Гібридизація електронних орбіталей атомів C |
|
. |
||||||
Види зв’язків: C− H |
|
C− C |
|
. |
|
|||
Валентні кути: |
|
|
|
|
|
. |
||
Найстійкіші цикли — |
|
|
|
|
|
. |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
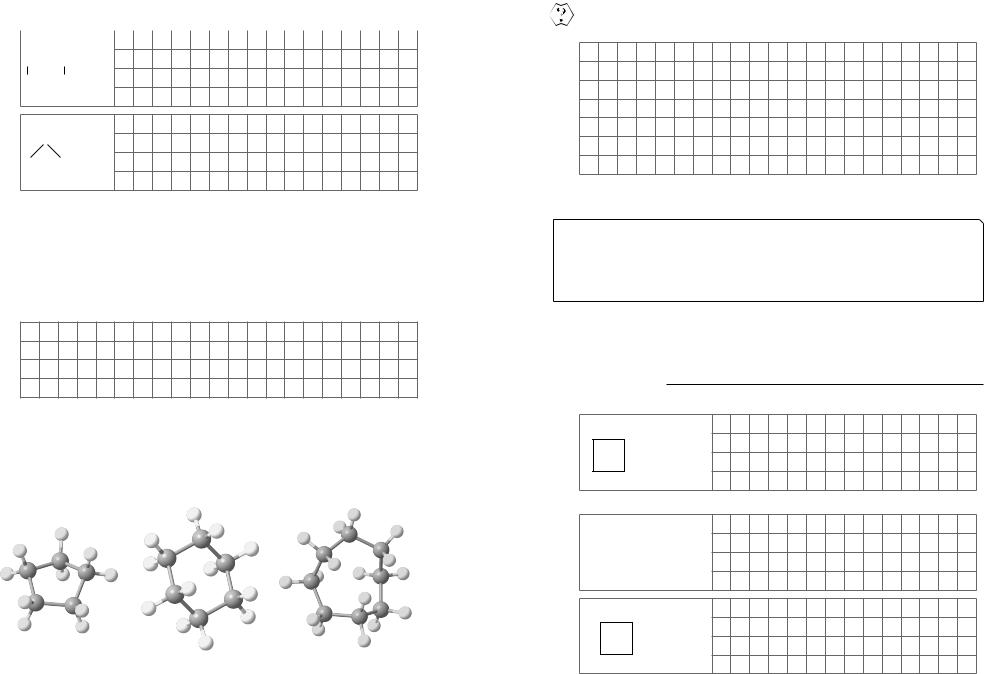
Циклопентан |
|
Циклогексан |
|
Циклооктан |
Фізичні властивості
C3H6, C4H8 — |
|
безбарвні речовини, |
|
C5H10, C6H12 — |
|
майже не розчинні |
|
|
у воді, горючі |
||
C7H14,... — |
|
|
|
|
|
|
|
|
|
|
|
Хімічні властивості
1.Горіння
CnH2n + O2 →
2.Заміщення
+ Cl2 hν→
3.Приєднання
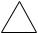 + H2 →
+ H2 →
+ HCl →
36 |
Опорні конспекти та дидактичні матеріали з органічної хімії |
|
|
 + Br2 t, hν→
+ Br2 t, hν→
4.Дегідрування
 AlCl3→ ←
AlCl3→ ←
Застосування
Найбільше практичне значення мають циклогексан, етилци клогексан. Циклогексан використовують для одержання цикло гексанолу, циклогексанону, адипінової кислоти, капролактаму, а також як розчинник.
Циклопропан використовують у медичній практиці як інгаля ційний анестезуючий засіб.
Одержання
1.Крекінг нафти
2.Гідрування ароматичних вуглеводнів
|
+ 3H2 |
→ |
|
|
|
|
|
|
Pt, t |
|
|
3. Дегалогенування |
|
|
|
||
|
|
|
|||
|
CH2 − CH2 − |
CH2 + Zn → |
|
+ZnCl2 |
|
|
|
|
|
|
|
Сl Сl
4.Дегідратація із циклізацією
CH3 −CH2 −CH2 −CH2 −CH3 → 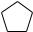 +H2
+H2
Арени (ароматичні вуглеводні)
Загальна формула
Теоретична частина |
37 |
|||||||
|
|
|
|
|
|
|
|
|
Гомологічний ряд C6H6, |
______ |
, |
______ |
. |
|
|
||
|
|
|
|
|
||||
В основі аренів |
|
. |
||||||
|
|
|
|
|
||||
Номенклатура |
|
|
||||||
Ароматичне ядро нумерують так, щоби сума локантів була |
|
|
||||||
|
|
|
|
|
|
|
|
. |
У назві аренів обов’язково є |
|
|
. |
|||||
Ізомерія
За кількістю й розташуванням радикалів у бензеновому ядрі.
Тривіальні назви
толуен — метилбензен
 CH3
CH3
стирол — вінілбензен
о-ксилен — 1,2-диметилбензен
м-ксилен — 1,3-диметилбензен
п-ксилен — 1,4-диметилбензен
38 |
Опорні конспекти та дидактичні матеріали з органічної хімії |
|
|
Бензен
Молекулярна формула
Структурна формула
Формула радикала фенілу
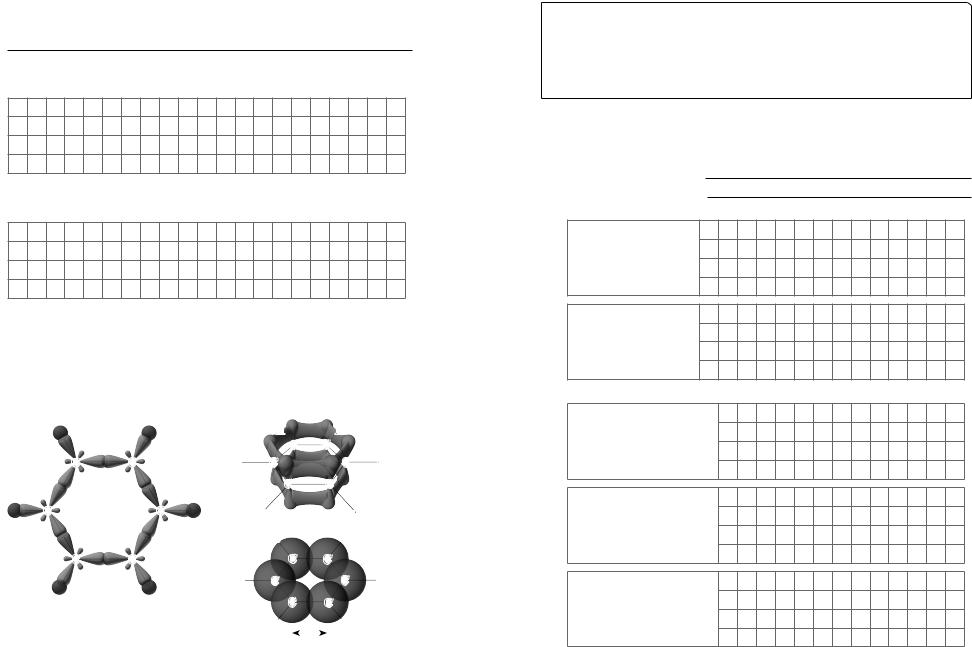
Будова
Гібридизація атомів C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
. |
||||||||
Види зв’язків: C− H |
|
|
|
|
|
C− C |
|
|
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
Валентні кути: σ − σ |
|
|
|
|
|
σ − π |
|
|
|
|
|
|
|
|
. |
|
|
|
|
|
|
||||||||||
|
H |
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
H |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
C |
C |
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
C |
C |
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
C |
|
H |
|
||||||||||
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
C |
|
C |
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
C |
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
H |
|
|
|
|
|
|
|
|
|
H |
H |
|
|
|
|
|
|
|
H |
|
H |
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
C |
C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
C |
|
|
|
||||||||
|
|
H |
|
|
|
|
H |
|
|
|
|
|
H |
|
|
|
C |
|
|
|
C |
|
H |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
C |
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,14 нм |
|
|
|
|||||||
Теоретична частина |
39 |
|
|
Фізичні властивості
Агрегатний стан |
Колір |
|||
t°пл |
|
Запах |
|
|
t°кип |
|
У воді |
|
|
|
|
|||
Дія на організм людини |
|
|
|
|
|
|
|
|
|
Хімічні властивості
1. Горіння
C6H6 + O2 (чистий) →
C6H6 + O2 (повiтря) →
2.Приєднання
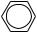 + H2 t, kat→
+ H2 t, kat→
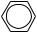 + Cl2 УФ→
+ Cl2 УФ→
3.Заміщення
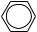 + Cl2 AlCl3→
+ Cl2 AlCl3→
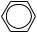 + HNO3 H2SO4→
+ HNO3 H2SO4→
 + CH3Cl AlCl3→
+ CH3Cl AlCl3→