Материал: Общая химия с физкалом

Данное равновесие можно охарактеризовать константой равновесия:
[Ag ][Cl ]
Кравн. [AgCl(к) ]
При данной температуре концентрация хлорида серебра есть величина постоянная. Если Кравн. и [AgCl(к) ] при данной температуре имеют постоянные значения, то и их произведение
К |
равн. |
[AgCl |
(к) |
] |
- тоже постоянная величина. Следовательно, |
|||||||
|
|
|
|
|||||||||
можно записать: |
|
|
|
|
|
|
|
|
||||
|
|
К |
равн. |
[AgCl |
(к) |
] [Ag |
|
][Cl |
|
] const |
||
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
||
Новая константа называется произведением растворимости (ПР). Запишем выражение ПР для хлорида серебра:
ПР = [Ag+][Cl-].
Произведением растворимости называется произведение равновесных концентраций ионов в насыщенном растворе над осадком малорастворимого электролита в степени, отвечающей числу этих ионов, возникающих при переходе данного соединения в раствор.
Например, для малорастворимого соединения фторид кальция CaF2 запишем уравнение гетерогенного равновесия:
CaF |
Ca |
2 |
2F |
|
|
|
|||
2(к) |
|
|
|
|
|
насыщ.р - р |
|||
Тогда выражение ПР имеет вид:
ПР |
|
|
[Ca |
2 |
][F |
2 |
(CaF |
) |
|
] . |
|||
|
2 |
|
|
|
|
|
Из справочников по химии можно узнать, что ПР при данной температуре величина постоянная (см. табл. 5).
7.2. Насыщенные, ненасыщенные, пересыщенные растворы с точки зрения теории произведения растворимости
Введем понятие произведения концентраций (ПК).
Произведение концентраций (ПК) ионов – это произведение
101
неравновесных концентраций ионов (зависит от условий задачи), отвечающих числу ионов, которые образуются при диссоциации соединения в растворе.
Например, уравнение гетерогенного равновесия для фосфата кальция Са3(РО4)2:
Са |
3 |
(РО |
4 |
) |
2(к) |
3Са |
2 |
2РО |
3 |
|
4 |
||||||||
|
|
|
|
|
|
Выражение ПР для этого соединения:
ПР [Ca2 ]3 [PO34 ]2.
Выражение ПК:
ПК С |
3 |
|
Са |
||
|
2 С |
2 |
3 . |
|
|
РО |
|
4 |
С |
Са |
2 или С |
3- |
|
|
РО |
|
|
|
|
4 |
- молярные неравновесные
концентрации ионов, которые зависят от условий задачи.
С точки зрения теории ПР все растворы делятся на насыщенные, ненасыщенные и пересыщенные.
Раствор, в котором произведение концентраций ионов равно ПР, называется насыщенным (ПК = ПР). В данном случае наблюдается равновесие: осадок ↔ насыщенный раствор.
Раствор, в котором произведение концентраций ионов меньше величины ПР, называется ненасыщенным (ПК < ПР). В этом случае осадка не будет.
Раствор, в котором произведение концентраций ионов больше величины ПР, называется пересыщенным (ПК > ПР). В растворе будет образовываться осадок этого соединения, т.к. пересыщенный раствор неустойчив, быстро переходит в насыщенный, что и приводит к образованию осадка. Образованию осадков способствует понижение температуры, т.к. снижается величина ПР и раствор оказывается пересыщенным.
Условием образования осадка является превышение произведения концентрации ионов ПК малорастворимого сильного электролита над величиной ПР. Зная концентрации ионов в растворе, можно прогнозировать направление гетерогенного процесса. Если ПК> ПР (раствор пересыщенный), то произойдет образование твердой фазы, т.е. осадка. Выпадение осадка продолжается до тех пор, пока
102
раствор |
не |
станет |
насыщенным. |
Впроцессе образования осадка можно выделить три стадии:
1)возникновение зародышей(центров) кристаллизации;
2)рост кристаллов из зародышей;
3)агрегация кристаллов с образованием поликристаллического осадка. Эти стадии протекают с разной скоростью. Стадией лимитирующей скорость гетерогенного процесса является самая медленная реакция - образования центров кристаллизации. Поэтому при достижении условия: ПК> ПР не всегда сразу же образуется осадок. Эта стадия может требовать для своего завершения нескольких часов, а то и суток.
Внекоторых случаях кристаллизация малорастворимого электролита, ограничивается только возникновением его микрокристаллов, которые стабилизируются, и при этом образуется лиофобный коллоидный ультрамикрогетерогенный раствор (см. раздел 9.2).
7.3. Практическое применение ПР. Растворимость веществ
Если известно произведение растворимости, его можно использовать для вычисления растворимости вещества при заданной температуре. Чем меньше величина ПР, тем труднее растворим электролит.
Введем понятие растворимости. Обозначим ее через S (моль/л).
Растворимость – S – это молярная концентрация в насыщенном растворе, она показывает, сколько моль данного вещества растворяется в 1 л воды.
Растворимость также принято выражать в г/л: S (г/л) = S (моль/л) ∙ М,
где М – молярная масса вещества в г/моль. Произведение растворимости плохо растворимого
соединения можно вычислить по данным его растворимости в моль/л.
7.4. Условия растворения осадков
103
Осадок растворяется, если гетерогенное равновесие смещается вправо, при этом насыщенный раствор переходит в ненасыщенный путем связывания одного из ионов труднорастворимого электролита в более прочные частицы:
слабый электролит;
менее растворимое вещество, ПР которого меньше;
газ;
комплексный ион.
Кроме того, на растворение осадков влияет температура. С ростом температуры возрастает и величина ПР. Раствор оказывается ненасыщенным (при высокой температуре), т.е. выполняется неравенство ПР > ПК.
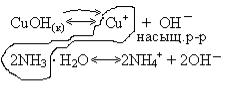
Пример 1. Объяснить с точки зрения теории ПР, почему гидроксид меди (I) растворяется при добавлении аммиака?
Ионы
Ag |
|
,Cu |
2 |
,Cu |
|
|
|
|
образуют
аммиачные
комплексы общей формулы
[Me |
n |
(NH |
) |
|
n |
|
2n |
] |
|||
|
|
3 |
|
|
, где n – заряд
иона.
Схема поведения осадка:
ион:
Ионы |
Cu |
|
и молекулы |
NH3 |
||
|
|
|||||
[Cu(NH3 )2 ] |
|
. |
|
|
||
|
|
|
|
|||
Запишем уравнение реакции:
образуют комплексный
Cu(OH) |
(к) |
2NH |
3 |
H |
O [Cu(NH |
) |
2 |
]OH 2H |
2 |
O |
|
|
2 |
3 |
|
|
|
Ионы насыщенного раствора связываются в прочные комплексные соединения, гетерогенное равновесие смещается вправо. Осадок CuOH растворяется в аммиаке.
Пример 2. Будет ли гидроксид алюминия растворяться в минеральных кислотах и щелочах?
104

Амфотерные гидроксиды металлов, такие как
Zn(OH) |
2 |
, |
Be(OH) |
2 |
, Pb(OH) |
2 |
, |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Sn(OH )2 , |
Al(OH)3 , Fe(OH)3 , Cr(OH)3 |
и др., растворяются в |
||||||||||||||||||
щелочах |
|
(ЭОН) с |
образованием |
гидрокомплексов |
общей |
|||||||||||||||
формулы |
|
Э |
|
[Me |
n |
(OH) |
|
n |
, где n |
– заряд иона металла, |
||||||||||
|
n |
|
|
2n |
] |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
соединения |
|
которого |
амфотерны; |
|
Э |
|
- |
ион металла |
||||||||||||
|
|
|
||||||||||||||||||
образующего |
щелочь (например, |
Na |
|
, K |
|
). |
А1(ОН)3 |
будет |
||||||||||||
|
|
|
||||||||||||||||||
растворяться в щелочах, например, в NaOH. Схема поведения осадка:
Ионы |
3 |
и |
ОН |
|
|
|
|
|
|
А1 |
|
|
|
|
|
||||
|
|
|
|
|
|
3 |
. |
|
|
образуют комплексный ион [Al(OH)6 ] |
|
|
|||||||
|
Запишем уравнение реакции: |
|
|
|
|||||
|
Al(OH) |
3 |
3NaOH Na |
[Al(OH) |
6 |
] |
|||
|
|
|
|
3 |
|
|
|
||
.
Ионы насыщенного раствора связываются в прочное комплексное соединение, гетерогенное равновесие смещается
вправо. Осадок
А1(ОН)3
растворяется в щелочи.
А1(ОН)3 |
будет |
растворяться |
в |
минеральных |
(неорганических) кислотах, например, в НС1. Схема поведения осадка:
Уравнение реакции: А1(ОН)3 + 3НС1 → А1С13 + 3Н2О. Ионы насыщенного раствора связываются с образованием слабого электролита – воды, гетерогенное
105