Материал: Неорганическая химия - курс лекций-презентаций

Общая характеристика галогенов
В подгруппу галогенов входят фтор, хлор, бром, иод и астат (астат – радиоактивный элемент, мало изучен).
Атомы галогенов имеют на внешнем энергетическом уровне по 7 электронов в состоянии …s2р5.
Этим объясняется общность их свойств.
Стремясь завершить внешний уровень, они присоединяют по одному электрону, проявляя степень окисления, равную –1. Такую степень окисления галогены имеют в соединениях с водородом и металлами.
Однако атомы галогенов, кроме фтора, могут проявлять и положительную степень окисления: +1, +3, +5, +7.
Такое значение степеней окисления объясняется электронным строением внешних энергетических уровней атомов галогенов.
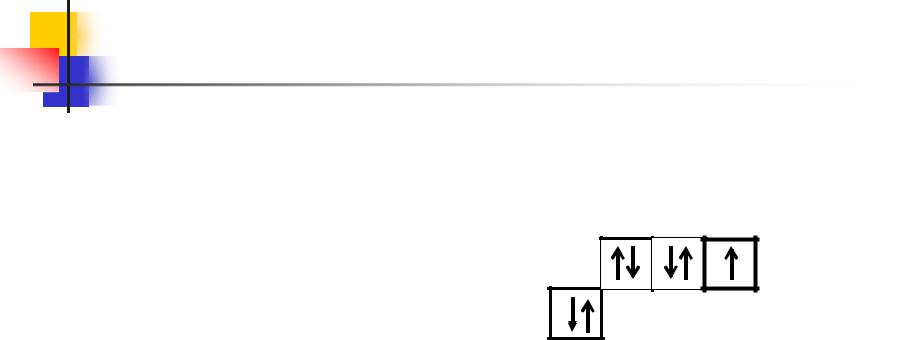
Общая характеристика галогенов
Будучи наиболее электроотрицательным элементом, фтор может только принимать один электрон на 2р-подуровень.
9 F |
1s |
2 |
2s |
2 |
2 p |
5 |
В’=1 |
|
|
|
2p |
||||
|
|
|
|
|
|
|
2s |
У него один неспаренный электрон, поэтому фтор бывает только одновалентным, а его степень окисления всегда –1.
Необходимо учитывать особенности фтора и его соединений.
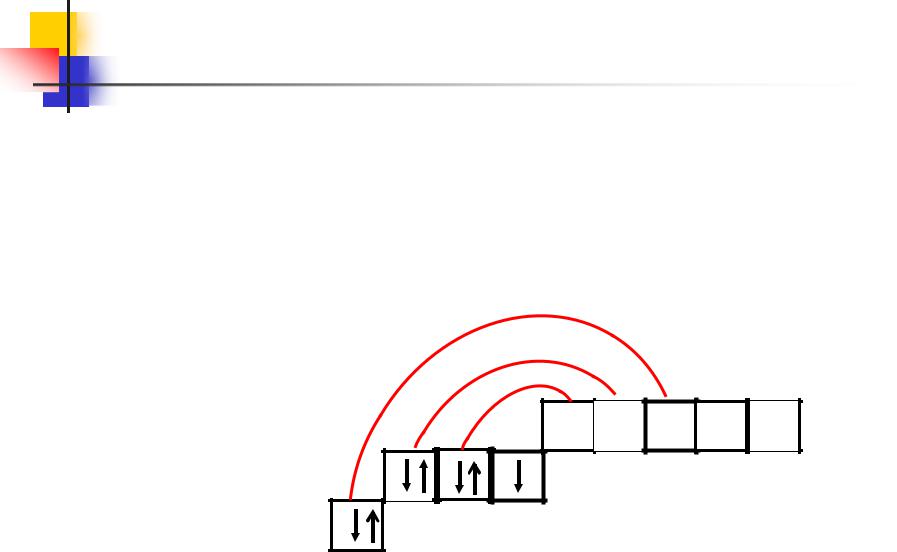
Общая характеристика галогенов
У атома хлора один неспаренный электрон на Зр-подуровне и он в обычном (невозбужденном) состоянии одновалентен.
Но поскольку хлор находится в III периоде, то у него имеется еще пять орбиталей (ячеек) Зd-подуровня:
17 Cl 1s2 2s2 2 p6 3s2 3p5
3p |
3s |
В’=1
3d
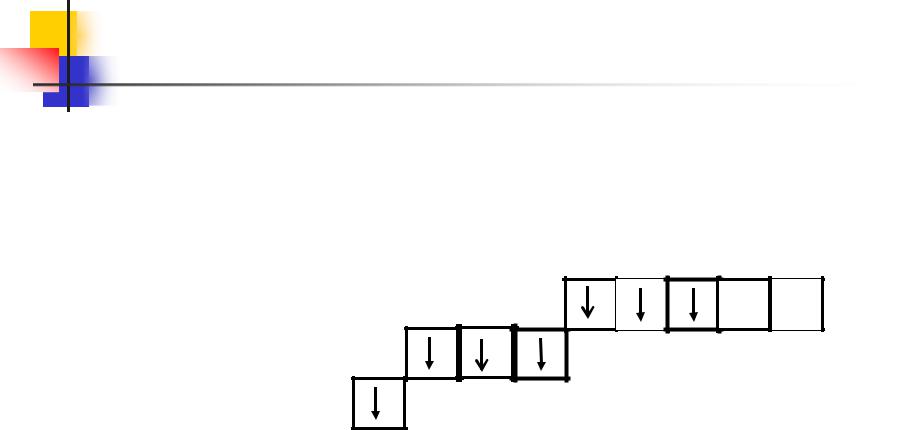
Общая характеристика галогенов
У атома хлора в возбужденном состоянии электроны с Зр- и 3s- подуровней переходят на Зd-подуровень (на схеме показано стрелками).
Разъединение электронов, находящихся в одной ячейке, увеличивает валентность на две единицы.
***Cl 1s2 2s2 2 p6 3s13p3 3d 3
17
3p |
3s |
В’=7 |
3d |
Хлор и его аналоги, кроме фтора, могут проявлять лишь
нечетную переменную валентность 1, 3, 5, 7 и
соответствующие положительные степени окисления.

Общая характеристика галогенов
Водные растворы водородных соединений галогенов являются кислотами: НF – фтороводородная (плавиковая), НСl – соляная, НВг – бромоводородная, НI– иодоводородная.
Следует иметь в виду, что галогены помимо общих свойств имеют и различия.
Это особенно характерно для фтора и его соединений.
Так, плавиковая кислота НF – слабая кислота; НСl, НВг, HI –
сильные кислоты.
Причем сила их возрастает с ростом заряда ядра атома.
Растворимость малорастворимых солей уменьшается в ряду
АgСl, АgВг, АgI.
В отличие от них АgF хорошо растворим в воде.
Фтор проявляет степень окисления только –1 (он прочнее всех удерживает электроны).