Материал: Нанотехнологии для всех (Рыбалкина), 2005, c.444
НАНОТЕХНОЛОГИИ ДЛЯ ВСЕХ
Теперь ясно видно, что | |2 определяет вероятность нахож дения частицы в некоторый момент времени t в некотором объ еме dV, то есть фактически место ее нахождения в точке с коор динатами x,y,z (объем имеет три измерения)
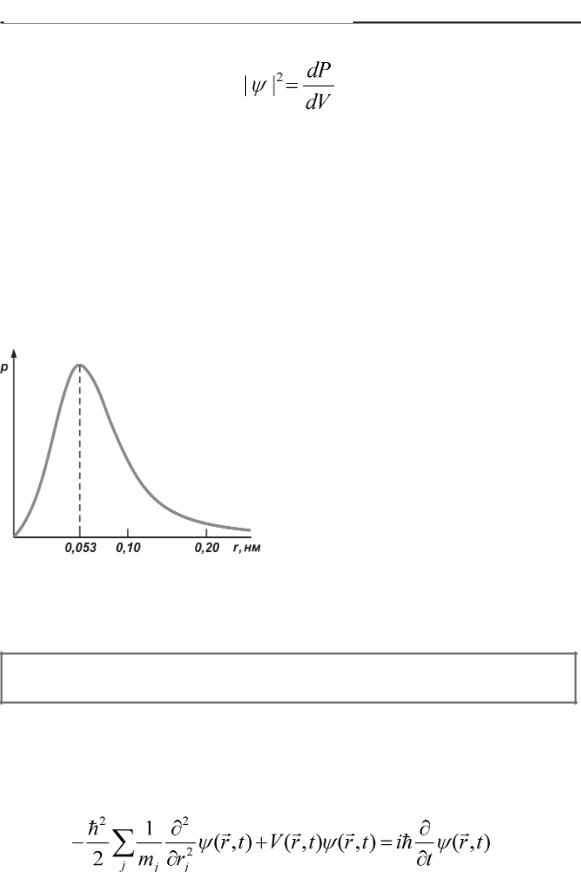
В атоме водорода единственный электрон как бы образует вокруг ядра электронное облако – облако отрицательного заряда, плотность которого в некоторой точке характеризует вероятность нахождения там электрона. На рисунке показана вероятность об наружить электрон на расстоянии r от ядра атома водорода.
Максимальная вероятность найти электрон соответствует рас стоянию r=0,053нм. Вполне воз можно, что в некоторый момент электрон находится или ближе к ядру, или дальше, но вероятность его обнаружения при этом убывает.
Область пространства, для ко торой вероятность обнаружения электрона составляет 95%, назы вается атомной орбиталью.
Итак, мы усвоили еще одну важную особенность квантовой механики:
Поведение элементарных частиц носит вероятностный характер, описываемый волновой функцией
Чтобы определить волновую функцию частицы для конкретной задачи, физики решают уравнение Шредингера, которое учитывает влияние электромагнитных сил на ее движение. Это дифференци альное уравнение в частных производных второго порядка.
Страшно? Для решения этого уравнения потребутся зна ния, которые не может обеспечить школьная программа по ма тематике, поэтому мы не будем обсуждать его в нашем курсе. За метим лишь то, что для квантового мира уравнение Шредингера играет ту же роль, что законы Ньютона для мира классического.
98

ГЛАВА 2. Законы квантового мира
Уравнение Шредингера и Периодическая сис тема элементов Менделеева
Многообразие нашего мира объясняется огромным разно образием элементов, существующих во Вселенной. В настоя щее время науке известно более 110 элементов с уникальными физико химическими свойствами.
Мы знаем, что атом любого вещества состоит из положи тельно заряженного ядра, окруженного облаком электронов. Ядро, в свою очередь, состоит из некоторого количества прото нов, заряженных положительно, и нейтронов, не имеющих ни какого заряда. Атомы стабильны потому, что в своем основном состоянии они энергетически нейтральны, то есть положитель ный заряд ядра полностью скомпенсирован суммарным заря дом электронов (число протонов в ядре атома равно числу электронов на его орбиталях).
Ученые всегда стремились упорядочить все разнообразные элементы в некую единую логическую схему. Самой удачной попыткой сделать это оказался принцип, предложенный в 1869 году русским ученым Д.И. Менделеевым, который лег в основу современной Периодической системы элементов.
В таблице Менделеева элементы расположены в порядке возрастания их атомных номеров (числа протонов в ядре). Нап ример, атомный номер водорода равен единице. Это говорит о том, что ядро атома водорода состоит из одного протона, вокруг которого вращается единственный электрон.
Элементы распределены по горизонтальным рядам, назы ваемым периодами, и вертикальным столбцам, называемым группами. Такое распределение основывается на некоторой общности физико химических свойств элементов, которые пе риодически изменяются в соответствии с их атомным номером. Например, все элементы первой группы (кроме водорода) яв ляются щелочными металлами, а все элементы восьмой группы представляют собой благородные газы.
Все это здорово, но при чем же здесь уравнение Шрединге ра? Мы помним, что согласно принципу Паули, электронная оболочка атома не может одновременно содержать два электро на в одном и том же состоянии. А поскольку число электронов в некоторых атомах достигает десятков и даже сотен, то возни кает естественный вопрос: как же они все там расположены?
www.nanonewsnet.ru |
99 |

НАНОТЕХНОЛОГИИ ДЛЯ ВСЕХ
Решение волнового уравнения Шредингера позволило вы числить четыре параметра, которых достаточно, чтобы пол ностью охарактеризовать состояние любого отдельно взятого электрона. Эти параметры получили название “четыре квантовых числа”. Полученная квантовая четверка – своего рода “паспорт”, однозначно идентифицирующий каждый электрон в атоме.
Главное квантовое число (число n) характеризует оболочку, в которой находится электрон. Оно соответствует повыша ющимся энергетическим уровням оболочек.
Чем больше число n, тем дальше элект рон отстоит от ядра и тем выше его энергия. Выделяют четыре энергетических оболочки:
K(n=1), L(n=2), M(n=3) и N(n=4).
Но одного деления на оболочки для пол ного описания состояния электрона недоста точно. Дело в том, что каждая энергетическая оболочка атома может “вмещать в себя” раз ное количество электронов. Понятно, что для
того, чтобы обеспечить их уникальность (согласно принципу Паули), каждая оболочка должна разбиваться еще на несколько подоболочек, получивших название орбиталей.
Орбитальное квантовое число (число l) определяет форму электронных орбиталей.
Решение уравнения Шредингера позволило вычислить формы всех существующих видов электронных орбиталей. Их всего четыре: s*, p*, d* и f орбитали. На рисунке изображен вид s , p и d орбиталей. S орбиталь имеет сферическую форму, p орбиталь – форму гантелей, d орбиталь похожа на трехмерный четырехлепестковый цветок.
Рис 42. Форма s*, p* и d* орбиталей
100
ГЛАВА 2. Законы квантового мира
Каждому типу орбитали соответствует определенная энер гия электрона. При переходе с одной орбитали на другую элект рон испускает излучение, характерное для соответствующего типа линий в атомном спектре, откуда, собственно, и произош ло их название:
s орбиталь соответствует “резкой” (sharp) s линии атомно го спектра;
p орбиталь соответствует “главной” (principal) p линии; d орбиталь соответствует “диффузной” (diffuse) d линии; f орбиталь соответствует “фундаментальной” (fundamental)
f*линии;
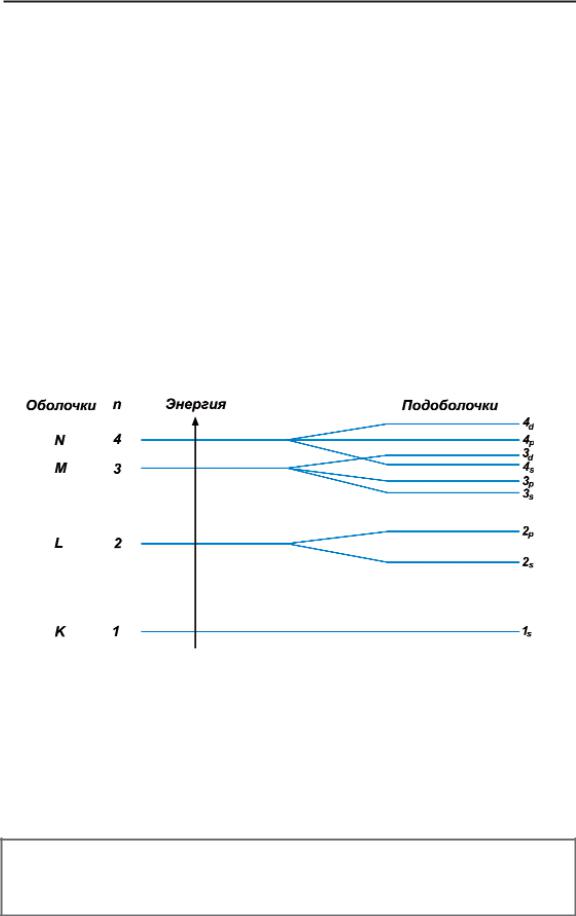
Энергетические уровни оболочек содержат в себе разное количество орбиталей. На рисунке показано относительное расположение энергетических уровней орбиталей, принадле жащих первым четырем электронным оболочкам:
Рис 43. Порядок расположения атомных орбиталей и оболочек
Так, первая К оболочка содержит только одну s*орбиталь. Следовательно, на первом энергетическом уровне может “жить” либо один, либо два электрона. Вторая оболочка вклю чает не только s*, но и 3 p*орбитали. Здесь обитают уже 2+6=8 электронов и т.д. Обратите внимание на особенность 4s подобо лочки: ее энергетический уровень расположен чуть ниже 3d по доболочки.
Магнитное квантовое число (число m) отражает влияние внешнего магнитного поля на состояние электрона и определяет ориентацию орбиталей в пространстве
Электрон – это не только отрицательно заряженная части ца, но еще и миниатюрный магнит, подобный стрелке компаса
www.nanonewsnet.ru |
101 |
НАНОТЕХНОЛОГИИ ДЛЯ ВСЕХ
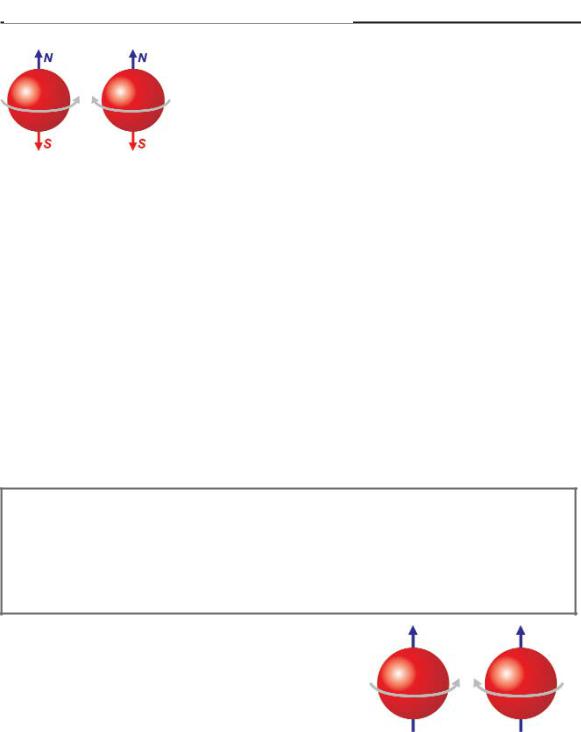
Рис 44. Магнитные полюсы электрона
с северным и южным полюсами. Электрон нельзя размагнитить, но зато можно повора чивать в пространстве, воздействуя на него внешним электромагнитным полем.
Число m также показывает максимально возможное число орбиталей для каждой
оболочки l.
Всего на оболочке может быть:одна s–орбиталь;
три p–орбитали;пять d– орбиталей;семь f– орбиталей.
Давайте теперь пристальнее посмотрим на один отдельно взятый электрон. Он, подобно планете Солнечной системы, вращается не только вокруг положительно заряженного ядра, но и вокруг собственной оси. Поэтому одной из важнейших ха рактеристик при описании электрона является его спиновое квантовое число.
Спиновое квантовое число (число s), показывает направление собственного момента вращения, который называется спином (от англ. “spin” – вращаться). Вращаться электрон может только в двух состояниях: по часовой стрелке, “спин вверх” (s=+1/2), и против часовой стрелки, “спин вниз” (s=–1/2).
Итак, принимая во внимание при веденные выше сведения, принцип запрета Паули можно переписать сле дующим образом:
Никакие два электрона в атоме не могут иметь одинаковые наборы четы* рех квантовых чисел.
Рис 50. Спин электрона. Пару электронов с противоположными спинами изображают cтрелками 
Электронная конфигурация элемента это запись распреде ления электронов в атоме по оболочкам и орбиталям. Она обычно записывается для атомов в основном состоянии соглас но следующим правилам:
1. Электроны заполняют орбитали последовательно, от меньшего энергетического уровня к большему. Низшие по энергии орбитали всегда заполняются первыми.
102