Материал: Нанотехнологии для всех (Рыбалкина), 2005, c.444
ГЛАВА 2. Законы квантового мира
Например:
Водород, атомный номер =1, число электронов = 1 Этот единственный в атоме водорода электрон должен за
нимать s орбиталь К оболочки, поскольку из всех возможных орбиталей она имеет самую низкую энергию. Электрон на этой орбитали называется 1s электрон.
Следовательно, электронная конфигурация водорода в ос новном состоянии: 1s1.
2. На любой орбитали может находиться не более двух электронов, и то лишь в том случае, если они имеют противо положные спины.
Например:
Литий, атомный номер =3, число электронов = 3 Орбиталь с самой низкой энергией – это 1s орбиталь. Она
может принять на себя только два электрона с неодинаковыми спинами. Схематически это записывается так: 

– запрещенное расположение спинов.
Третий электрон в атоме лития должен занимать орбиталь, следующую по энергии за самой низкой орбиталью, т.е. 2s ор биталь. Таким образом, литий имеет электронную конфигура цию: 1s22s1.
3. Заполнение орбиталей одной подоболочки начинается одиночными электронами с параллельными (одинаковыми по знаку) спинами, и лишь после того, как одиночные электроны займут все орбитали, может происходить окончательное запол нение орбиталей парами электронов с противоположными спинами.
Например:
Азот, атомный номер =7, число электронов = 7
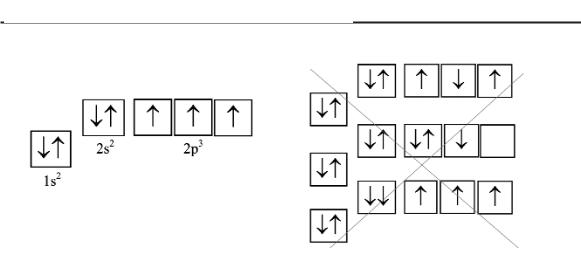
Азот имеет электронную конфигурацию 1s22s22p3. Три электрона, находящиеся на 2p подоболочке, должны распола гаться поодиночке на каждой из трех 2p орбиталей. При этом все три электрона должны иметь параллельные спины.
www.nanonewsnet.ru |
103 |
НАНОТЕХНОЛОГИИ ДЛЯ ВСЕХ
Разрешенная конфигурация электронов
Три неразрешенные конфигурации электронов
Современная наука считает все электроны стандартными, поэтому если поменять два любых электрона местами, конфигу рация системы не изменится. В таблице представлены электрон ные конфигурации элементов с атомными номерами от 1 до 20:
Атомный |
Элемент |
Электронная |
Атомный |
Элемент |
Электронная |
номер |
|
конфигурация |
номер |
|
конфигурация |
|
|
|
|
|
|
1 |
Водород |
1s1 |
11 |
Натрий |
1s22s22p63s1 |
2 |
Гелий |
1s2 |
12 |
Магний |
1s22s22p63s2 |
3 |
Литий |
1s22s1 |
13 |
Аллюминий |
1s22s22p63s23p1 |
4 |
Бериллий |
1s22s2 |
14 |
Кремний |
1s22s22p63s23p2 |
5 |
Бор |
1s22s22p1 |
15 |
Фосфор |
1s22s22p63s23p3 |
6 |
Углерод |
1s22s22p2 |
16 |
Сера |
1s22s22p63s23p4 |
7 |
Азот |
1s22s22p3 |
17 |
Хлор |
1s22s22p63s23p5 |
8 |
Кислород |
1s22s22p4 |
18 |
Аргон |
1s22s22p63s23p6 |
9 |
Фтор |
1s22s22p5 |
19 |
Калий |
1s22s22p63s23p64s1 |
10 |
Неон |
1s22s22p6 |
20 |
Кальций |
1s22s22p63s23p64s2 |
Табл 4. Электронные конфигурации первых 20 ти элементов Периодической системы
Из таблицы видно, что электронные конфигурации эле ментов отличаются периодичностью, что и отображено в табли це Менделеева. Например, все элементы одного периода имеют одинаковый электронный остов (внутренние электронные обо лочки) и отличаются лишь количеством электронов, находя щихся на подоболочках с самой высокой энергией.
А все элементы, принадлежащие какой либо группе, имеют характерную для нее электронную конфигурацию высшей по энергии оболочки. Например, для I группы характерна конфи гурация Ns1, где N – номер периода; для II группы – конфигу рация Ns2, для III группы – Ns2p1 и так далее, до группы 0(VIII), все элементы которой имеют конфигурацию Ns2p6.
104

ГЛАВА 2. Законы квантового мира
|
|
|
|
|
Группы |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
I |
II |
III |
IV |
|
V |
VI |
VII |
VIII(0) |
|
|
|
|
|
|
|
|
|
|
Характерная |
s1 |
s2 |
s2p1 |
s2p2 |
|
s2p3 |
s2p4 |
s2p5 |
s2p6 |
конфигурация |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 й период |
2s1 |
2s2 |
2s22p1 |
2s22p2 |
|
2s22p3 |
2s22p4 |
2s22p5 |
2s22p6 |
3 й период |
3s1 |
3s2 |
3s23p1 |
3s23p2 |
|
3s23p3 |
3s23p4 |
3s23p5 |
3s23p6 |
|
|
|
|
|
|
|
|
|
|
4 й период |
4s1 |
4s2 |
4s24p1 |
4s24p2 |
|
4s24p3 |
4s24p4 |
4s24p5 |
4s24p6 |
Табл 5. Электронная конфигурация высшей по энергии подооболочки у элементов различных групп
Электронная конфигурация элементов VIII группы назы вается устойчивой, поскольку при этом внешняя оболочка их атомов заполнена полностью. Элементы этой группы получили название “инертных” или “благородных” газов, поскольку из за своей устойчивой электронной конфигурации при обычных условиях они практически не образуют химических соедине ний. Подробнее о механизме образования химических связей можно прочесть в главе, посвященной нанохимии.
Квантовые размерные эффекты
Внашей вводной лекции мы познакомились с понятием ультрадисперсности и убедились, что с уменьшением размера частиц какого либо вещества его физические и химические свойства могут существенно меняться. Это происходит из за того, что ход физических процессов зависит не только от свойств самого вещества, но и от геометрии той области прост ранства, в которой они протекают – грубо говоря, от “разме ров” этой области. Для наглядной иллюстрации этой идеи при ведем следующую аналогию: представим, что в узком переулке нужно развернуться какому то транспортному средству. Оче видно, что мотоциклисту это будет сделать легче, чем водителю тяжелого КАМАЗа.
Размерные эффекты в твердых телах – это явление, наблю дающееся в условиях, когда геометрические размеры объекта сравнимы с той или иной из длин, определяющих протекание физических процессов (например, длиной свободного пробега носителя заряда, длиной волны де Бройля и т.д.).
Взависимости от размеров исследуемого образца различа ют классические и квантовые размерные эффекты, которые могут влиять практически на любые свойства вещества. Понят но, что для нанометровых объектов, где размеры частиц срав
www.nanonewsnet.ru |
105 |
НАНОТЕХНОЛОГИИ ДЛЯ ВСЕХ
нимы с де Бройлевской длиной волны электрона, характерны именно квантовые размерные эффекты, определяющие такие свойства вещества, как теплоемкость, электропроводность не которые оптические свойства и т.п.
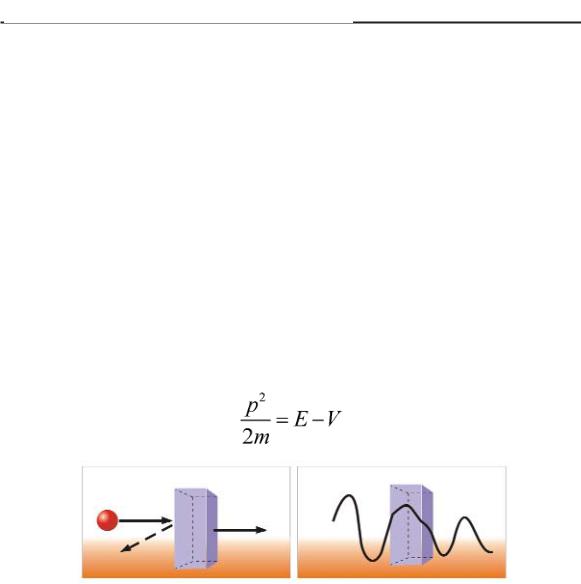
Самым ярким представителем квантовых размерных эф фектов является туннельный эффект — явление, играющее важную роль в нанотехнологии. Сущность туннельного эффек та заключается в преодолении микрочастицей потенциального барьера в случае, когда ее полная энергия меньше высоты барь ера. Это явление чисто квантовое, ведь классическая частица не может находиться внутри потенциального барьера высоты V, если ее энергия E<V, так как кинетическая энергия частицы становится при этом отрицательной, а ее импульс — мнимой величиной.
Рис 21. Условная схема туннельного перехода
Однако для микрочастицы этот вывод не справедлив: всле дствие соотношения неопределенностей фиксация частицы внутри барьера делает неопределенным ее импульс.
Поскольку потенциальная энергия частицы однозначно определяется ее координатой, кинетическая энергия импуль сом, а в силу соотношения неопределенностей одновременно и точно координату и импульс частицы определить невозможно, то разделение энергии на кинетическую и потенциальную в квантовой физике бессмысленно. Соответственно, появляется вероятность прохождения частицы сквозь потенциальный барьер.
Феномен туннелирования открыл в 1928 году наш соотече ственник Г. А. Гамов, впервые получив решения уравнения Шредингера, описывающие возможность преодоления части цей энергетического барьера, даже если ее энергия меньше вы
106

ГЛАВА 2. Законы квантового мира
соты барьера. Найденное решение объясняло многие экспери ментально наблюдавшиеся процессы и позволило понять боль шой круг явлений, происходящих при вылете частицы из ядра
– основы атомной науки и техники. Многие считают, что за грандиозность результатов его работ, ставших основополагаю щими для многих наук, Г. А. Гамов должен был быть удостоен нескольких Нобелевских премий.
И лишь спустя тридцать лет после открытия Гамова появи лись первые приборы на основе туннельного эффекта: туннель ные диоды, транзисторы, датчики, термометры для измерения сверхнизких температур, и, наконец, сканирующие туннель ные микроскопы, положившие начало современной нанотех нологии.
Почему нельзя смешивать законы классичес кой и квантовой физики
В квантовой механике широко используется принцип супер* позиции. Это означает, что результат действия двух или более волн может быть получен суммированием действий каждой из волн в отдельности. Согласно этому допущению, если кванто механическая система может находиться в нескольких состоя ниях, описываемых, соответственно, волновыми функциями
, …, n, то физически допустимой будет и суперпози
ция (суммирование, наложение) этих состояний, то есть состо яние, изображаемое волновой функцией
где c1,c2,c3,…,cn – вероятность нахождения системы в сос тояниях , …, n соответственно. Операция суммирова ния в теории вероятности соответствует логическому “или”, а операция умножения – логическому “и”. Поэтому для просто ты восприятия суперпозицию вида c1 c2 можно читать так: система N находится в состоянии если она находится ли* бо в состоянии , либо в состоянии .
Таким образом, любая сложная волновая функция может быть представлена в виде совокупности нескольких более простых функций
www.nanonewsnet.ru |
107 |