Материал: Национальная+программа+Недостаточность+витамина+Д+2018

Более эффективными дозами, способными устранить дефицит витамина, являются дозы, превышающие норму физиологической потребности в 2–3 раза. Высокие дозы витаминов необходимы для быстрой ликвидации дефицита
иполного насыщения организма этими микронутриентами.
6.2.Обогащенные витаминами пищевые продукты
ВВеликобритании для профилактики рахита проводится обогащение маргаринов и кулинарных жиров витамином D, до 40% которого поступает именно с этими продуктами. Во многих странах практикуется обогащение витамином D молока (примерно 400 МЕ на 1 литр).
Как показали исследования, проведенные во Франции, Ирландии и Великобритании, у детей, подростков и взрослых, регулярно использовавших в питании обогащенные микронутриентами готовые завтраки на зерновой основе, потребление витаминов В1, В2, В6, В12, D, фолиевой кислоты
ижелеза было выше, чем у людей, не употреблявших эти продукты, и более соответствовало рекомендуемым нормам потребления (RDA).
ВГермании потребление витамина D за счет обычных продуктов колебалось от 22% РНП в младшей возрастной группе до 45% у подростков, причем вклад обогащенных
70продуктов в потребление этого витамина был незначительным (2–3%). Лишь прием витаминно-минеральных комплексов позволил увеличить суммарное поступление витамина D до 60–75% рекомендуемого уровня его потребления.
ВСША обогащение сухих зерновых завтраков витаминами и минеральными веществами в количестве от 15 до 25% рекомендуемого суточного потребления на порцию осуществляется с 1970-х годов, а начиная с 1980-х годов производится обогащение кальцием (в дозе 30% от РНП на стакан) апельсинового сока. Регулярное включение в рацион этих продуктов внесло существенный вклад в потребление вносимых микронутриентов у разных слоев населения. Более чем у половины населения потребление этих микронутриентов приблизилось или достигло рекомендуемого уровня.
К сожалению, в торговой сети присутствует лишь ограниченное количество обогащенных продуктов. В 2008– 2010 годах в нашей стране подвергалось обогащению витаминами и минеральными веществами около 2% хлебобулочных изделий (Письмо Главного государственного санитарного врача РФ Г. Г. Онищенко № 01/1867-0-32 от 11.02.2010 «Об обогащении микронутриентами пищевых продуктов,
втом числе массовых сортов хлеба») и молочных продуктов, а также безалкогольных напитков от общего количества их производства (Письмо Главного санитарного врача РФ Г. Г. Онищенко № 01/12925-8-32 от 12.11.2008 «О состоянии заболеваемости, обусловленной дефицитом микронутриентов»).
25 октября 2010 г. Распоряжением Правительства Рос-
сийской Федерации № 1873-р были утверждены «Основы государственной политики Российской Федерации в области здорового питания населения на период до 2020 года»5. Одной из основных задач государственной политики в области здорового питания является развитие производства пищевых продуктов, обогащенных незаменимыми компонентами, специализированных продуктов детского питания, продуктов функционального назначения, диетических (лечебных и профилактических) пищевых продуктов и биологически активных добавок к пище, в том числе
для питания в организованных коллективах (трудовые, образовательные и др.) с целью сохранения и укрепления здоровья населения, профилактики заболеваний, обусловленных неполноценным и несбалансированным питанием. Оптимизация витаминного статуса каждого человека принадлежит к технологиям снижения потерь от социально значимых алиментарнозависимых заболеваний.
6.3. Применение витамина D во время беременности
При компенсации дефицита витамина D во время беременности дозы витамина D в 2000 и 4000 МЕ/сут демонстрируют схожие эффекты. Беременные (12–16 недель беременности) сначала получали по 2000 МЕ/сут в течение 30 суток, затем были рандомизированы для получения 2000 или 4000 МЕ/сут до начала родов. В начале исследования содержание 25(OH)D в плазме крови у беременных составило 22,7 ± 9,7 нг/мл, в конце исследования — 36,2 ± 15,0 нг/мл в группе 2000 МЕ/сут и 37,9 ± 13,5 нг/мл в группе 4000 МЕ/сут. Влияние различных доз витамина было более выраженным при исследовании пуповинной крови: уровень 25(OH)D составил 22,1 ± 10,3 нг/мл в группе принимавших 2000 МЕ/сут и 27,0 ± 13,3 нг/мл у получавших 4000 МЕ/сут (р = 0,024). Риск преждевременных родов был обратно пропорционален концентрации 25(OH)D
всыворотке крови беременных перед родами. У беременных, принимавших как 2000 МЕ, так и 4000 МЕ витамина D
всутки, не зарегистрировано каких-либо нежелательных явлений, связанных с его приемом [14].
Интересные результаты были получены при осуществлении программ по комплексной нутритивной поддержке витамином D беременной / ребенка в период внутриутробного развития, в которых витамин D назначали сначала беременной, а затем новорожденному. Такой комплексный подход обеспечивал весьма эффективную компенсацию дефицита витамина D и у матери, и у ребенка. Например, в одном рандомизированном исследовании показали, что прием более высоких доз витамина D беременными (2000 МЕ/сут), а затем новорожденными до возраста 6 месяцев (800 МЕ/сут) является более эффективным для поддержания уровня 25(OH)D > 20 нг/мл, чем более низкие его дозы (1000 МЕ/сут — беременные, 400 МЕ/сут — новорожденные). Беременные были рандомизированы на полу-
чение плацебо, 1000 МЕ/сут витамина D3 или 2000 МЕ/сут витамина D3, начиная с 27-й недели беременности и до родоразрешения. Затем новорожденные получали плацебо,
400 или 800 МЕ/сут витамина D3 от рождения до возраста 6 месяцев. На момент начала исследования концентрация 25(OH)D > 20 нг/мл была зафиксирована у 54% пациенток
вгруппе плацебо, у 64% в группе 1000 МЕ/сут, у 55% в группе 2000 МЕ/сут. На 36-й неделе беременности концентрация 25(OH)D > 20 нг/мл отмечалась существенно чаще у беременных, получавших витамин D (91 и 89% соответственно), чем в группе плацебо (50%; p < 0,001). Концентрация
25(OH)D 20 нг/мл в пуповинной крови также отмечалась чаще в группах детей, получавших витамин D (72 и 71%), чем в группе плацебо (22%; p < 0,001). Важно отметить, что в возрасте 6 месяцев уровень 25(OH)D 20 нг/мл был зафиксирован у 74% детей в группе плацебо, у 82% детей, получавших 400 МЕ/сут (в сравнении с плацебо р = 0,21), у 89%
вгруппе 800 МЕ/сут (в сравнении с плацебо р = 0,03) [15].
Вдругом рандомизированном контролируемом исследовании прием витамина D в дозе 5000 МЕ/сут кормящими матерями оказался эффективным и безопасным для ком-
5Доступно на: https://zakonbase.ru/content/part/700988 Ссылка активна на 17.01.2018.
пенсации дефицита витамина D у детей. Матери, осущест- |
|
( 2 = 8,37; р = 0,004), дыхательной системы ( 2 = 4,95; |
|
|
вляющие исключительно грудное вскармливание, были |
|
р = 0,026); |
|
|
рандомизированы на получение холекальциферола в дозе |
• выраженный токсикоз и угрозу прерывания в 1-м и |
|
||
5000 МЕ/сут в течение 28 суток или на получение одно- |
|
3-м триместрах беременности ( 2 = 4,81; р = 0,028); |
|
|
кратной дозы 150 000 МЕ. У принимавших однократную |
• гестоз ( 2 = 3,97; р = 0,046); |
|
|
|
дозу содержание 25(OH)D достигало пика в плазме кро- |
• острые респираторные инфекции с повышением тем- |
|
||
ви (в среднем 160 нг/мл) и в грудном молоке (в среднем |
|
пературы тела и катаральными явлениями ( 2 = 5,10; |
|
|
40 нг/мл) уже в первые сутки, после чего быстро сни- |
|
р = 0,024); |
|
|
жалось. Напротив, при ежедневном приеме витамина D |
• |
курение во время или до беременности ( 2 = 9,54; |
|
|
(5000 МЕ/сут) достигалась стабильная концентрация |
|
р = 0,002) [17]. |
|
|
25(OH)D как в плазме крови (18 нг/мл), так и в грудном |
|
|
|
|
молоке (8 нг/мл). У грудных детей концентрация 25(OH)D |
|
|
|
|
увеличилась с 16 ± 12 до 39 ± 12 нг/мл именно при условии |
|
6.4. Коррекция низкого статуса |
|
|
ежедневного приема витамина кормящей матерью. При |
|
витамина D его повышенными |
|
|
этом у всех младенцев данной группы были достигнуты |
|
|
|
|
|
дозами |
|
|
|
уровни 25(OH)D > 20 нг/мл [16]. |
|
|
|
|
Более высокое потребление витамина D во время бере- |
|
Данные современных фундаментальных и клинических |
|
|
менности снижает риск так называемого свистящего дыха- |
|
|
||
исследований свидетельствуют о том, что дозы витамина D |
|
|||
ния у ребенка, т. е. бронхообструкции. Так, анализ когорты |
недостаточны для компенсации его дефицита в организме |
|
||
пар мать–ребенок в одном из исследований показал, что |
|
|||
ребенка и профилактики связанной с ним коморбидной |
|
|||
среднее потребление витамина D во время беременности |
|
|||
патологии [19–22]. |
|
|
||
составило 548 ± 167 МЕ/сут. К возрасту 3 лет у 186 (16%) |
|
|
||
|
Результаты анализа данных клинических исследований, |
|
||
детей отмечалось наличие свистящего дыхания. По сравне- |
|
|
||
в которых была зафиксирована положительная связь при- |
|
|||
нию с подгруппой беременных в нижней четверти суточного |
менения витамина D в группах детей и подростков в возрас- |
|
||
потребления витамина D (в среднем 350 МЕ/сут) беремен- |
|
|||
те от 0 до 18 лет с содержанием 25(ОН)D в плазме крови, |
|
|||
ные с самым высоким потреблением витамина D (в среднем |
представлены в табл. 6.4. |
|
|
|
720 МЕ/сут) характеризовались более низким риском рож- |
|
|
||
|
Отобранные релевантные публикации были проанали- |
71 |
||
дения ребенка со свистящим дыханием (ОР 0,39; 95% ДИ |
зированы двумя экспертами на соответствие следующим |
|
||
0,25–0,62). Увеличение потребления беременной витами- |
|
|||
критериям: |
|
|
||
на D на каждые 100 МЕ/сут было достоверно ассоцииро- |
• участие в исследовании детей и/или подростков в воз- |
|
||
вано со снижением риска свистящего дыхания на 19% [17]. |
|
расте 0–18 лет; |
|
|
Еще в одном рандомизированном исследовании устано- |
|
|
|
|
• назначение прегормона холекальциферола (витамин D |
) |
|
||
вили, что достаточная обеспеченность витамином D матери |
|
3 |
|
|
|
в форме монопрепарата витамина D; |
|
|
|
в период беременности (при условии приема холекаль- |
|
|
|
|
• |
в исследовании был получен клинически значимый |
|
||
циферола 2000 МЕ/сут) и ребенка в первые 6 месяцев |
|
результат (компенсация дефицита витамина D, зафик- |
|
|
жизни (800 МЕ/сут) достоверно снижает риск развития |
|
|
||
|
сированная по уровню 25(ОН)D, и/или снижение риска |
|
||
острой респираторной инфекции в последующие годы |
|
|
||
|
развития той или иной патологии), подтвержденный |
|
||
жизни. Здоровые беременные получали плацебо или вита- |
|
|
||
|
статистически [40]. |
|
|
|
мин D, начиная с 27-й недели беременности и до родов, |
|
В обзор не включали исследования, в которых изучалась |
|
|
а дети получали плацебо или дотации витамина D от рож- |
эффективность медленно метаболизируемого эргокальци- |
|
||
дения до возраста 6 месяцев. Беременные и рожденные |
ферола (витамин D2) и высокоактивных форм витамина D |
|
||
от них дети были рандомизированы на прием плацебо, |
(25-гидроксивитамин D, 1,25-дигидроксивитамин D и др.). |
|
||
меньшей дозы витамина D (1000 МЕ/сут — беременным, |
Также не рассматривались результаты исследований, в кото- |
|
||
400 МЕ/сут — новорожденным) или большей дозы витами- |
рых витамин D назначали короткими курсами (< 4 месяцев) |
|
||
на (2000 МЕ/сут — беременным, 800 МЕ/сут — новорож- |
в дозировках 30–180 МЕ/сут. Концентрацию 25(ОН)D |
|
||
денным). Доля детей, посещавших врача в связи с острой |
в плазме крови 21–29 нг/мл рассматривали как признак |
|
||
респираторной инфекцией, была наиболее высока в группе |
недостаточности витамина D, а уровни > 30 нг/мл при- |
|
||
плацебо (99%) и в группе с более низкой дозой витамина D |
нимали за нормальное его содержание [20]. Концентрацию |
|
||
(95%; при сравнении с группой плацебо р = 0,17). В то же |
25(ОН)D в диапазоне 10–20 нг/мл считали дефицитом, |
|
||
время прием витамина D беременной в дозе 2000 МЕ/сут |
а < 10 нг/мл — тяжелым гиповитаминозом/авитаминозом D. |
|
||
и новорожденным в дозе 800 МЕ/сут в течение 6 меся- |
|
Проанализированы результаты 21 клинического иссле- |
|
|
цев приводил к достоверному уменьшению числа детей |
дования по оценке эффективности: |
|
|
|
(на 12%), нуждавшихся в медицинской помощи по пово- |
1) компенсации дефицита витамина D при различных |
|
||
ду острой респираторной инфекции (87%; р = 0,004). При |
|
состояниях; |
|
|
этом среднее число посещений врача ребенком в возрасте |
2) профилактики/лечения витамин D-зависимой патоло- |
|
||
6–18 месяцев было статистически значимо ниже только при |
|
гии у детей (см. табл. 6.4). |
|
|
использовании дозы 2000 МЕ/сут (для беременной) и дозы |
|
Большинство исследований первой группы было наце- |
|
|
800 МЕ/сут (для ребенка): в группе плацебо — в среднем |
лено на частичную компенсацию дефицита витамина D |
|
||
4 визита, в группе низкой дозы витамина — 3 визита, более |
[25(OH)D > 20 нг/мл] [23, 27, 35–39] и только одно |
|
||
высокой дозы витамина — 2,5 визита (р = 0,048) [18]. |
исследование — на компенсацию дефицита витамина D |
|
||
Следует отметить, что, согласно проведенному исследодо нижней границы нормы [25(OH)D > 30 нг/мл] [28]. |
|
|||
ванию, к факторам риска низкой обеспеченности беремен- |
Ориентированность большинства исследователей на дости- |
|
||
ных женщин витамином D следует относить: |
жение относительно низкого значения 25(OH)D — 20 нг/мл, |
|
||
• возраст старше 25 лет ( 2 = 15,37; p < 0,001); |
вероятно, связана с тем, что достижение этой концентрации |
|
||
•профилактику гиповитаминоза недостаточной дозипозволяет эффективно предупреждать изменения костной
ровкой 25(OH)D3 или отсутствие приема витамина D |
ткани, наблюдаемые при дефиците витамина D [23, 24, 34]. |
( 2 = 22,27; p < 0,001); |
Однако развитие внекостной симптоматики дефицита вита- |
• наличие патологии костно-суставной системы |
мина D (ожирение, сниженная резистентность к инфекции, |
( 2 = 10,15; p < 0,001), желудочно-кишечного тракта |
бронхолегочные заболевания и др.) наиболее эффективно |

Таблица 6.4. Результаты исследований, в которых подтверждено влияние дотации витамина D на содержание 25(ОН)D в плазме крови
|
|
Исследования (целевая группа) |
Возраст |
Средняя доза, МЕ/сут |
Курс, мес |
|
|
|
|
|
|
|
|
Цель — частичная компенсация дефицита витамина D: 25(OH)D > 20 нг/мл |
|
||
|
|
|
|
|
|
|
|
Дети с ожирением (нагрузочная доза 25 000 МЕ/нед, 2 мес, |
11 ± 3 лет |
3570 |
2 |
|
|
затем поддерживающая доза) [23] |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Подростки с ожирением [24] |
12–18 лет |
2000 |
3 |
|
|
|
|
|
|
|
|
Дети раннего возраста [25] |
1–2 мес |
600–800 |
9 |
|
|
|
|
|
|
|
|
Недоношенные дети (28–34 нед гестации) [26] |
1–10 мес |
800 |
10 |
|
|
|
|
|
|
|
|
Дети и подростки с болезнью Крона [27] |
8–18 лет |
2000 |
6 |
|
|
|
|
|
|
|
|
Дети раннего возраста [28], при этом их матери получали |
1 мес |
800* |
6 |
|
|
по 2000 МЕ/сут во время беременности |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Дети и подростки [29] |
13 ± 2 лет |
2000 |
12 |
|
|
|
|
|
|
|
|
Дети и подростки [30] |
10–14 лет |
1000 |
3 |
|
|
|
|
|
|
|
|
Дети с аномально высоким уровнем паратгормона [31] |
4–8 лет |
1000 |
2 |
|
|
|
|
|
|
|
|
Дети и подростки [32] |
10–17 лет |
2000 |
12 |
|
|
|
|
|
|
|
|
Цель — полная компенсация дефицита витамина D: 25(OH)D > 30 нг/мл |
|
||
|
|
|
|
|
|
|
|
Дети и подростки [33] (метаанализ) |
5–14 лет |
1000–4000 |
1–3 |
|
|
|
|
|
|
|
|
Цель — профилактика/лечение различных заболеваний |
|
||
|
|
|
|
|
|
|
|
Снижение риска обострения бронхиальной астмы [34] |
5–18 лет |
500–2000 |
1–12 |
|
|
(систематический обзор) |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Снижение риска развития атопического дерматита в зимний |
9 ± 5 лет |
1000 |
1 |
72 |
|
период [35] |
|||
|
|
|
|
||
|
|
Снижение риска заболеваемости острым средним отитом |
5–14 лет |
1000 |
4 |
|
|
и его осложнений [36] |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Профилактика гриппа и приступов бронхиальной астмы [37] |
7–14 лет |
1200 |
6 |
|
|
|
|
|
|
|
|
Повышение минеральной плотности кости при приеме |
10–18 лет |
2000 |
12 |
|
|
противоэпилептических препаратов [38] |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Повышение содержания адипонектина у детей с ожирением [39] |
5–18 лет |
3000 |
12 |
|
|
|
|
|
|
Примечание. Исходный уровень 25(OH)D у детей, включенных в исследования, варьировал от 4 до 19,5 нг/мл. * — группа сравнения получала плацебо; после 6 месяцев применения статистически значимых различий в концентрации витамина D в сравниваемых группах не обнаружено.
предупреждается при достижении уровня 25(OH)D |
ного приема необходимо рекомендовать витамин D в дозе |
30 нг/мл [35–37]. |
500 МЕ/сут (для недоношенных — 800–1000 МЕ/сут), |
В большинстве клинических исследований профилак- |
детям в возрасте от 4 месяцев до 4 лет — 1000 МЕ/сут; |
тический прием витамина D был долговременным и непре- |
4–10 лет — 1500 МЕ/сут, 10–16 лет — 2000 МЕ/сут. |
рывным: длительность курса варьировала от 1 до 12 (в сред- |
Следует подчеркнуть, что эти дозировки, сформу- |
нем 6) месяцев. При этом прием препаратов витамина D |
лированные на основе данных анализа результативных |
осуществлялся в дозах от 800 до 4000 (в среднем 1200; |
исследований, относятся только к препаратам, которые |
95% ДИ 800–3000) МЕ/сут. |
представлены моноформами витамина D, поэтому предла- |
Сопоставление данных по дозированию витамина D |
гаемые диапазоны, ориентированные на долговременный |
в разных возрастных группах показало, что усреднен- |
и непрерывный прием, заведомо не могут быть исполь- |
ной эффективной дозой витамина D для детей в возрасте |
зованы для препаратов, которые помимо витамина D |
0–1 месяца является доза 740 МЕ/сут (рис. 6.4) [41]. С каж- |
содержат, например, кальций. Избыток кальция, особенно |
дым годом жизни результативная профилактическая доза |
в форме карбоната, оказывает многочисленные небла- |
в среднем повышается на 93 МЕ/сут (r = 0,57). |
гоприятные воздействия на здоровье ребенка, включая |
Полученная в результате регрессионного анализа фор- |
замедление роста, нарушения функции желудочно-кишеч- |
мула (740 + Возраст [годы] 93 [МЕ/сут]) отражает |
ного тракта и др. [38]. |
усредненную результативную дозу витамина D в форме |
Для нормального роста и развития костной ткани необхо- |
холекальциферола для детей разного возраста, достаточную |
дим постоянный баланс между потреблением, всасыванием |
для достижения концентрации 25(OH)D > 20 нг/мл. Вместе |
и экскрецией. В соответствии с американскими и европей- |
с тем применение формулы может быть затруднительно |
скими рекомендациями, ежедневное потребление кальция |
с практической точки зрения: в частности, осуществить |
должно составлять 15 мг/кг массы тела в сутки (табл. 6.5). |
дозирование витамина D 740 МЕ/сут детям в возрасте |
Костной системе необходимо 4 мг/кг в сутки, такое же |
до 1 года, 833 МЕ/сут — детям в возрасте 1–2 лет и т. д. пред- |
количество кальция расходуется в результате резорбции. |
ставляется технически сложным (большинство препаратов |
Экскреция кальция через желудочно-кишечный тракт |
витамина D дозируются каплями по ~500 МЕ/кап). Именно |
составляет 11 мг/кг в сутки, через почки — 4 мк/кг в сутки. |
поэтому для практического применения этой формулы |
Влияние на организм недостатка кальция хорошо известно, |
предлагается «ступенеобразная» схема дозирования вита- |
но не менее опасен его избыток, который нарушает данное |
мина D для детей разного возраста. В соответствии с этой |
равновесие, способствует замедлению роста, повышению |
схемой, детям в возрасте до 4 месяцев жизни для ежеднев- |
хрупкости костей, появлению микролитов в почках [38]. |
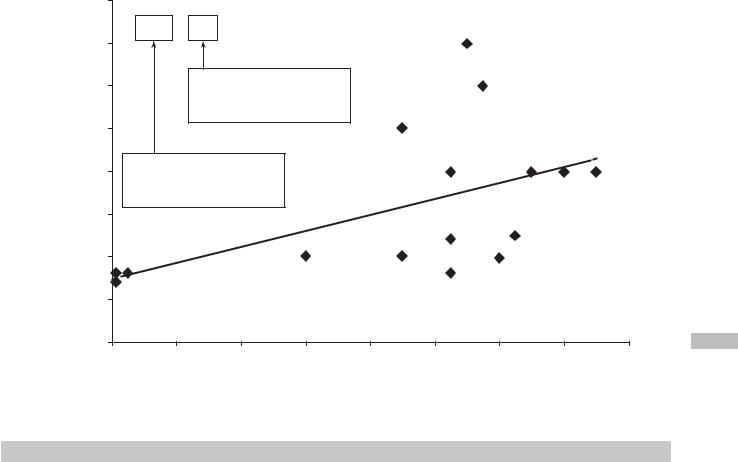
Рис. 6.4. Корреляция между изученными профилактическими дозами витамина D и возрастом детей-участников клинических |
|||||||||||
исследований [41] |
|
|
|
|
|
|
|
|
|
|
|
|
4000 |
Доза витамина D (МЕ/сут) = |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
740 |
+ |
93 |
возраст (лет) |
|
|
|
|
|
|
|
3500 |
|
|
|
|
|
|
|
|
|
|
|
3000 |
|
|
Средний ежегодный |
|
|
|
|
|
||
МЕ/сут |
|
|
прирост результативной |
|
|
|
|
||||
|
|
|
|
|
|
|
|||||
|
|
|
|
дозы витамина D |
|
|
|
|
|
||
2500 |
|
|
|
|
|
|
|
|
|
(r = 0,57) |
|
D, |
|
|
|
|
|
|
|
|
|
|
|
витамина |
2000 |
Средняя результативная |
|
|
|
|
|
|
|||
доза витамина D |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|||||
|
для новорожденных |
|
|
|
|
|
|
||||
1500 |
|
|
|
|
|
|
|
|
|
|
|
Доза |
|
|
|
|
|
|
|
|
|
|
|
1000 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
500 |
|
|
|
|
|
|
|
|
|
|
|
0 |
|
|
|
|
|
|
|
|
|
73 |
|
0 |
2 |
|
4 |
6 |
8 |
10 |
12 |
14 |
16 |
|
|
|
|
|||||||||
|
|
|
|
|
|
|
Возраст, лет |
|
|
|
|
Таблица 6.5. Рекомендуемые нормы потребления кальция (мг/сут) в Российской Федерации, странах Евросоюза и США [31]
Возраст |
РФ |
Страны ЕС |
США |
|
|
|
|
0–3 мес |
400 |
250–600 |
400 |
|
|
|
|
4–6 мес |
500 |
250–600 |
400 |
|
|
|
|
7–9 мес |
600 |
400–650 |
600 |
|
|
|
|
10–12 мес |
600 |
400–650 |
600 |
|
|
|
|
1–3 года |
800 |
400–800 |
800 |
|
|
|
|
4–6 лет |
900–1000 |
400–800 |
800 |
|
|
|
|
7–10 лет |
1100 |
600–1200 |
800 |
|
|
|
|
11–17 лет |
1200 |
700–1200 |
1200 |
|
|
|
|
25–50 лет |
1000 |
500–1200 |
800 |
|
|
|
|
Беременные |
1100–1500 |
800–1450 |
1200 |
|
|
|
|
Кормящие женщины |
1200 |
900–1550 |
1200 |
|
|
|
|
6.5. Компенсация дефицита |
мина D в дозе 200 МЕ/сут (низкая доза) или 2000 МЕ/сут |
||
витамина D у детей и подростков |
(высокая доза) в течение 12 месяцев (рис. 6.5). В начале |
||
исследования концентрация 25(OH)D |
20 нг/мл была |
||
при различных состояниях |
|||
установлена у 18%, а 30 нг/мл — у 5% участников. В тече- |
|||
Результаты клинических исследований и метаанализа |
ние первого года концентрация 25(OH)D увеличилась |
||
до 20 нг/мл и выше только у 34% детей при приеме 200 МЕ |
|||
демонстрируют, что увеличение потребления витамина D |
|||
витамина в сутки и у 96% при приеме 2000 МЕ/сут. Уровни |
|||
на каждые 100 МЕ/сут коррелирует с повышением содер- |
|||
жания 25(OH)D в плазме крови на 1 нг/мл. Таким образом, |
30 нг/мл установлены только у 4% детей, принимавших |
||
по 200 МЕ/сут, и у 64% употреблявших по 2000 МЕ/сут |
|||
для достижения оптимального уровня 25(OH)D в крови |
|||
(см. рис. 6.5) [42]. |
|
||
у детей (> 30 нг/мл) требуется прием 1000–3000 МЕ вита- |
|
||
мина D в сутки [41]. |
В другом исследовании сравнивали содержание 25(OH)D |
||
в плазме крови в начале исследования и через 12 меся- |
|||
Так, в рандомизированном контролируемом исследова- |
|||
нии с участием подростков (средний возраст 13 ± 2 года) |
цев приема очень низкой (200 МЕ/сут) и более высокой |
||
(2000 МЕ/сут) дозы витамина D у подростков в возрасте |
|||
доза витамина D в 2000 МЕ/сут была необходима для |
|||
11–15 лет (средний возраст 13 лет). В начале исследования |
|||
повышения 25(OH)D не менее чем до 20 нг/мл и выше. |
|||
Подростки были рандомизированы в группы на прием вита- |
и через 12 месяцев приема очень низкой и более высокой |
||
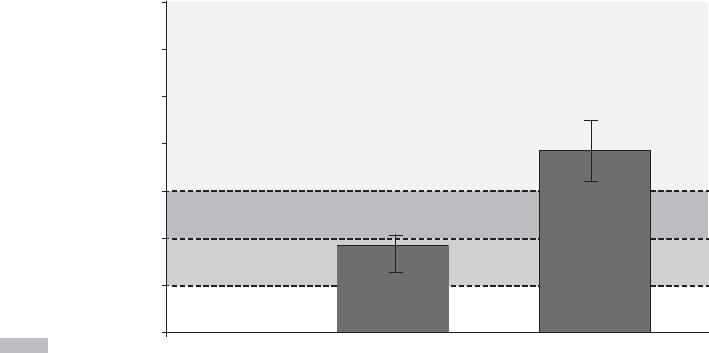
Рис. 6.5. Содержание 25(ОН)D в крови подростков (возраст 13,0 ± 2,0 года) после приема низкой (200 МЕ/сут) и высокой (2000 МЕ/сут) дозы витамина D в течение 12 месяцев [42]
Концентрация 25(OH)D в плазме крови в течение 12 мес, нг/мл
74
70
60
50
36 ± 22,3 нг/мл
40
Норма
30
Недостаточность |
19 ± 6,6 нг/мл |
20
Дефицит
10
Авитаминоз
0
Низкая доза |
Высокая доза |
(200 МЕ/сут, n = 112) |
(2000 МЕ/сут, n = 113) |
Примечание. Концентрация 25(ОН)D в плазме крови < 10 нг/мл расценивается как признак глубокого дефицита и авитаминоза, 10–20 нг/мл — как дефицита витамина D. Данные представлены в виде средних арифметических и стандартных отклонений.
дозы витамина в обеих группах оценивали преодоление |
У детей и подростков в возрасте 8–18 лет с болезнью |
концентрацией 25(ОН)D порога 20 нг/мл и более 30 нг/мл. |
Крона доза витамина D 2000 МЕ/сут оказалась более |
Из группы получавших по 200 МЕ/сут, только четверо детей |
эффективной для компенсации его дефицита по сравне- |
через 1 год преодолели концентрацию 25(ОН)D в 30 нг/мл, |
нию с дозой 400 МЕ/сут. Участники исследования были |
тогда как в группе получавших по 2000 МЕ/сут в норму |
рандомизированы на получение препарата витамина в тече- |
вошли 64 подростка [42]. |
ние 6 месяцев. Исходно в обеих группах средние уровни |
Известно, что с дефицитом витамина D ассоциировано |
25(OH)D составили 24 ± 8 нг/мл, у 79% уровень 25(OH)D |
детское и подростковое ожирение. В рандомизированном |
был менее 30 нг/мл. После 6 месяцев приема витамина толь- |
плацебоконтролируемом исследовании было установлено, |
ко у 35% детей в группе 400 МЕ/сут отмечена концентрация |
что витамин D в дозе 2000 МЕ/сут способствовал эффек- |
25(OH)D > 30 нг/мл по сравнению с 74% детей в группе |
тивной компенсации дефицита витамина D у подростков |
принимавших по 2000 МЕ/сут (p < 0,001). Средние значе- |
в возрасте 12–18 лет с ожирением. Участники получали вита- |
ния 25(OH)D были на 9,6 нг/мл выше в группе 2000 МЕ/сут, |
мин D или плацебо в течение 12 недель. В конце 12-й неде- |
чем в группе 400 МЕ/сут (95% ДИ 6,0–13,2; p < 0,001). |
ли содержание 25(OH)D в плазме в среднем увеличилось |
Процент пациентов, у которых 25(OH)D был выше верхней |
на 6 нг/мл в группе подростков, получавших по 2000 МЕ/сут |
границы нормы, в сравниваемых группах не различался [45]. |
витамина D. Меньшие дозы витамина D не имели статисти- |
Прием витамина D в дозе 1000 МЕ/сут является более |
чески значимого эффекта у подростков с ожирением [42]. |
эффективной мерой в компенсации дефицита витамина D у |
В другом исследовании оценивали эффективность и пере- |
здоровых детей в возрасте 10–14 лет, чем использование дозы |
носимость нагрузочной дозы витамина D (25 000 МЕ/нед, |
600 МЕ/сут. Участники исследования были рандомизированы |
что соответствует 3570 МЕ/сут) для компенсации его дефи- |
для получения в течение 3 месяцев плацебо (200 мл/сут моло- |
цита у детей с ожирением (средний возраст 11,1 ± 3,0 года). |
ка) или витамина D в дозах 600 или 1000 МЕ/сут. Исходно |
Прием витамина D в течение 9 недель привел к повы- |
дефицит витамина D [25(OH)D < 20 нг/мл] был зафиксиро- |
шению уровня 25(OH)D > 20 нг/мл у 84% наблюдае- |
ван у 92% детей. Через 3 месяца средний процентный прирост |
мых с недостаточностью витамина (исходная концентрация |
содержания 25(ОН)D в плазме крови был значительно выше |
25(OH)D < 20 нг/мл). У большинства детей, которые |
в группе получавших 600 МЕ/сут (+138%) и 1000 МЕ/сут |
не достигли рекомендованного уровня 25(OH)D, установ- |
(+177%) витамина D по сравнению с контрольной группой, |
лены грубые нарушения режима приема витамина D (про- |
где концентрация 25(OH)D снизилась (-5%). Процент детей |
пущено 80% назначенных доз витамина D) [43]. |
с 25(OH)D > 20 нг/мл составил 5,9% в контрольной группе, |
Протеомный анализ позволил установить, что адипо- |
70% — в группе принимавших 600 и 81% — 1000 МЕ витамина |
нектин является связующим звеном между ожирением и |
в сутки [46]. |
дефицитом витамина D в группе детей и подростков в воз- |
Другое рандомизированное контролируемое исследо- |
расте 5–18 лет. У пациентов с дефицитом витамина зафик- |
вание показало, что прием витамина D в дозе 1000 МЕ/сут |
сировано пониженное содержание адипонектина. Прием |
приводит к снижению аномально высоких уровней парат- |
витамина D (3000 МЕ/нед) в течение 12 месяцев приводил |
гормона у детей 4–8 лет. Дети были рандомизированы |
к статистически значимому повышению концентрации ади- |
на прием 1000 МЕ/сут витамина D (группа 1) или пла- |
понектина [44]. |
цебо (группа 2) в течение 2 месяцев. Спустя назначен- |