Материал: Методичка 4400 с ответами
3.2. Каталитический процесс
3.2.1. В чём сущность ускоряющего действия катализатора?
-
повышает значение свободной энергии;
-
снижает энергию активации реакции;
-
повышает энергию активации реакции;
-
смещает равновесие в обратимой реакции;
-
открывает новый реакционный путь.
3.2.2. Выбрать порядок соотношения между внутренней и наружной поверхностью пористого зерна катализатора Sвн/Sнар:
1) 100; 2) 0,01; 3) 104; 4) 108; 5)1; 6) 106.
3.2.3. Выбрать уравнение для расчета параметра Зельдовича-Тиле при проведении процесса на пористом зерне катализатора с реакцией первого порядка:
1)
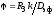 ;
2)
;
2)
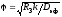 ;
3)
;
3)
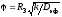 ;
;
4)
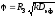 ;
5)
;
5)
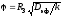 .
.
3.2.4. Указать способы увеличения степени использования внутренней поверхности зерна катализатора:
-
увеличение размера зерна катализатора;
-
уменьшение размера зерна катализатора;
-
увеличение размеров пор;
-
уменьшение коэффициента диффузии;
-
увеличение температуры;
-
уменьшение температуры.
3.2.5. Для процесса на пористом зерне катализатора правильно выбрать графическую зависимость степени использования внутренней поверхности от параметра Зельдовича-Тиле и области протекания процесса (I – кинетическая область; II – переходная область; III – внутридиффузионная область):
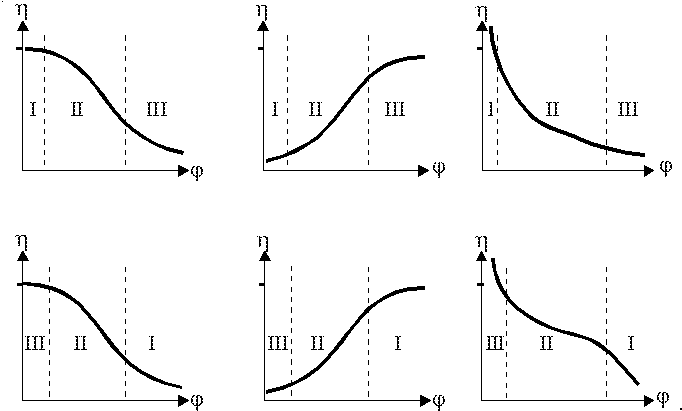
1 2 3
4 5 6
3.2.5. Зависит ли скорость химического процесса от размера зерна катализатора?
-
зависит, если процесс протекает в кинетической области;
-
не зависит, если процесс протекает во внутридиффузионной области;
-
не зависит, если режим в реакторе изотермический;
-
зависит, если внутренняя диффузия является лимитирующей стадией процесса;
-
не зависит, если лимитирующей стадией процесса является эндотермическая реакция.
3.2.6. Какое распределение концентрации внутри пористого зерна катализатора характерно для кинетической области?
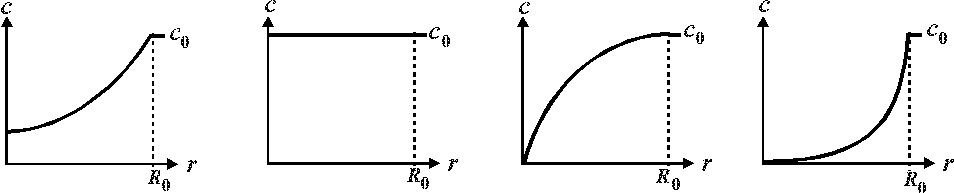
1 2 3 4
3.2.7. Какое распределение концентрации внутри пористого зерна катализатора характерно для внутридиффузионной области?
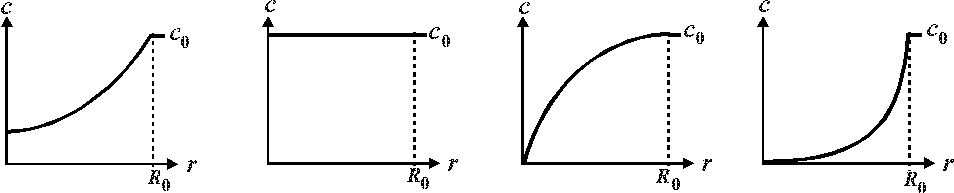
4. Химический реактор
4.1. Общие положения
4.1.1.
Чему равен
порядок n
реакции, протекающей в реакторах
идеального смешения непрерывного и
идеального вытеснения, включенных
параллельно, если
при одинаковых их объёмах нагрузки
соотносятся как
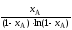 ?
?
-
n = 1;
-
n = 0;
-
данных недостаточно;
-
n = 0,5;
-
n = 2
4.1.2. В каких случаях оправдано проведение реакции при избытке одного из компонентов?
-
если реакция обратимая, один из компонентов (более дешёвый или более доступный) берется в избытке для повышения степени превращения другого (более ценного) компонента;
-
избыток одного из компонентов не оправдан, так как для наилучшего протекания реакции необходимо брать компоненты в стехиометрических количествах;
-
избыток одного из компонентов уместен в случае, когда другой компонент ядовит или когда продукты реакции повышенно токсичны;
-
когда один из компонентов токсичен или когда продукты реакции ядовиты, реагенты следует брать строго в стехиометрических количествах.
4.1.3. Чему равен порядок n реакции, протекающей в реакторах идеального смешения непрерывного и идеального вытеснения, соединенных параллельно, если одинаковы объемы реакторов, объемные скорости потока в них и достигаемые степени превращения?
-
n = 1;
-
n = 0;
-
данных недостаточно;
-
n = 0,5;
-
n = 2
4.1.4. Экзотермическая реакция осуществлена в адиабатическом режиме в в двух реакторах – с неподвижным и с псевдоожиженным слоем катализатора, – до достижения одинаковой степени превращения. Температура на входе в слой катализатора – одинаковая. Каковы температуры на выходе из слоя в обоих случаях?
-
в неподвижном слое выше;
-
в неподвижном слое ниже;
-
температуры одинаковы;
-
в псевдоожиженном слое выше.
4.1.5. С какой целью осуществляют теоретическую оптимизацию процесса:
-
для выбора наилучшего ввода реагента в реактор;
-
для эффективного отвода тепла из зоны реакции;
-
для организации процесса в реакторе, чтобы максимально приблизиться к оптимальному температурному режиму;
-
чтобы сместить равновесие реакции;
-
чтобы определить необходимый избыток реагента.
4.2. Математическая модель процесса в реакторе
4.2.1. Какие из приведенных уравнений можно использовать для расчета времени пребывания реагентов в реакторе идеального вытеснения при проведении реакции первого порядка A→R?
|
|
|
1 2 3 4
3.2.8. При каком режиме в центре пористого зерна будет достигнута максимальная степень превращения?
-
кинетическом;
-
внутридиффузионном;
-
внешнедиффузионном.
3.2.8. Зависит ли скорость превращения вещества в пористом зерне ката-лизатора от температуры при протекании процесса во внутридиффузионной области?
-
зависит;
-
не зависит;
-
слабо зависит.
3.2.9. Зависит ли скорость превращения вещества в пористом зерне катализатора от температуры катализатора при протекании процесса во внешнедиффузионной области?
-
зависит;
-
не зависит;
-
слабо зависит.
3.2.10. Активность катализатора – это характеристика:
-
замедляющего действия на данную реакцию;
-
ускоряющего действия на данную реакцию;
-
избирательности в процессе органического синтеза;
-
термостойкости при проведении сильно экзотермических процессов;
-
стойкости к действию контактных ядов.
3.2.11. Какие способы интенсификации каталитического процесса, протекающего в кинетической или во внутридиффузионной области, можно использовать?
-
измельчение катализатора;
-
повышение температуры;
-
понижение температуры;
-
увеличение концентрации исходных веществ в объеме потока;
-
повышение давления в аппарате;
-
понижение давления;
-
организация псевдоожижения.
3.2.13. Укажите причину увеличения скорости реакции в присутствии катализатора:
-
изменяется энергия активации реакции;
-
увеличивается движущая сила процесса;
-
изменяется константа равновесия;
-
изменяется фазовый состав реагентов;
-
изменяется температурный режим.
3.2.14. Экзотермический каталитический процесс протекает стационарно в области внешней диффузии. Будут ли различаться температура потока и катализатора, почему и насколько?
-
нет. Теплопроводность твердого катализатора большая, что выравнивает температуры потока и катализатора.
-
нет. Вследствие интенсивного теплообмена выравнивается температура между катализатором и потоком.
-
да. Теплообмен между катализатором и потоком не достаточен для полного выравнивания их температур, которые будут различаться на несколько градусов.
-
да. Тепло- и массообмен между катализатором и окружающим потоком имеют одинаковый механизм переноса (молекулярный перенос через пограничный слой), т.е. процесс протекает адиабатически и температура катализатора отличается от температуры потока на величину адиабатического разогрева Tад.
-
да. Но часть тепла реакции расходуется на нагрев катализатора, и его температура меньше величины адиабатического разогрева Tад.
4.2.2. Какими уравнениями можно пользоваться для расчета времени пребывания реагентов в реакторе идеального сиешения непрерывном при проведении необратимой реакции второго порядка A + B = R + S?
|
|
|
4.2.3. Изменение концентрации исходного реагента с во времени t и по объему в реакторе идеального вытеснения имеет вид:
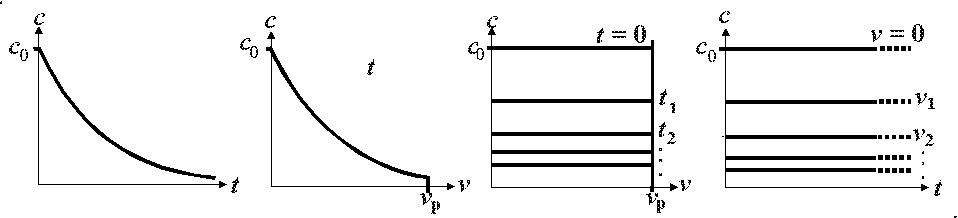
1 2 3 4
4.2.4. В изотермическом реакторе идеального смешения непрерывном проводится реакция первого порядка A → R. Какие из приведенных уравнений пригодны в этом случае для расчета времени пребывания реагентов?
|
6)
|
7)
8)
9)
|
4.2.5. Какие из приведенных уравнений пригодны для расчета времени пребывания в изотермическом реакторе идеального вытеснения при проведении необратимой реакции второго порядка A + B = R + S (реагенты A и B взяты в стехиометрическом соотношении).
|
|
|
4.2.6. Какую зависимость надо построить для нахождения времени реакции в реакторе идеального вытеснения и реакторе идеального смешения непрерывном графическим способом?
|
|
|
4.2.7. Какие из представленных уравнений используются в различных случаях как математическая модель процесса в изотермическом реакторе идеального вытеснения?
при τ=0 сА = сА0;
|
при τ=0 хА=0; при l = 0 сА = сА0; |
|
4.2.8. Какие из приведенных уравнений пригодны для расчета времени пребывания в изотермическом реакторе идеального вытеснения при проведении простой необратимой реакции второго порядка A + B = R + S?
|
|
|
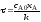 ;
;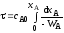 ;
;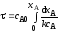 ;
;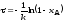 ;
;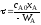 ;
;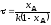 ;
;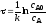 ;
;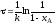 ;
;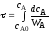 .
.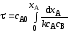 ;
;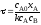 ;
;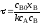 ;
;
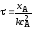 ;
;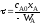 ;
;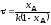 ;
;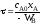 ;
;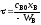 .
.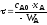 ;
;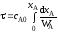 ;
;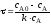 ;
;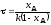 ;
;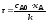 ;
;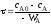 ;
;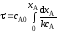 ;
;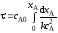 ;
;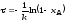 .
.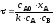 ;
;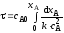 ;
;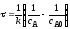 ;
;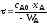 ;
;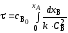 ;
;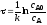 ;
;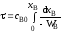 ;
;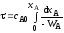 ;
;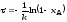 .
.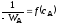 ;
;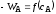 ;
;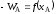 ;
;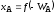 ;
;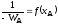 ;
;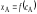 .
.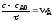 ;
;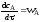
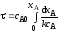 ;
;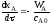
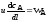
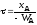 ;
;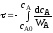 .
.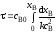 ;
;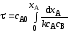 ;
;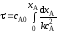 ;
;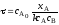 ;
;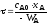 ;
;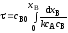 .
.