Материал: Методичка 4400 с ответами
6.2. Производство аммиака
6.2.1. Установите правильную последовательность превращений в химической схеме синтеза аммиака:
-
(3)3Н2 + N2 = 2NН3
-
(2)СО + Н2О = СО2 + Н2
-
(1)СН4 + Н2О = СО + 3Н2
6.2.2. Как изменяется равновесное содержание аммиака при понижении температуры и повышении давления в реакции N2 + 3H2 2NH3 + Q?
-
увеличивается;
-
не изменяется;
-
снижается;
-
проходит через максимум.
6.2.3. Для полноты использования азотоводородной смеси в технологической схеме синтеза аммиака применяют:
-
систему последовательности реакторов;
-
рецикл;
-
интенсивный отвод тепла реакции;
-
добавку инертных газов.
6.2.4. В каком направлении следует изменять давление P, температуру T, концентрацию реагирующих веществ в синтезе аммиака, чтобы равновесие реакции сдвинуть в сторону образования целевого продукта?
1) T увеличить, P уменьшить, процесс вести при избытке Н2;
2) T увеличить, P уменьшить, процесс вести при избытке N2;
3) T уменьшить, P уменьшить, соотношение Н2: N2 – стехиометрическое;
4) T уменьшить, P увеличить, процесс вести при избытке Н2;
5) T уменьшить, P увеличить, соотношение Н2: N2 – стехиометрическое;
6) T уменьшить, P атмосферное, применить катализатор.
6.2.5. Какие мероприятия могут способствовать реализации концепции минимизации отходов в производстве аммиака?
-
применение активных катализаторов;
-
использование полного рецикла;
-
использование фракционного рецикла;
-
уменьшение объёма продувочных газов.
6.2.6. Какие мероприятия могут способствовать реализации концепции оптимального использования оборудования в производстве аммиака?
-
увеличение температуры топочных газов в трубчатой печи конверсии метана, тем самым увеличение скорости превращения и, соответственно, уменьшение размеров этого реактора;
-
замена некоторых реакторов с горизонтальным расположением катализатора на радиальные аппараты;
-
уменьшение диаметра и толщины стенки контактного аппарата;
-
замена аммиачного конденсатора на воздушный теплообменник;
-
совмещение процессов конверсии природного газа и оксида углерода в одном аппарате;
-
исключение из технологической схемы отделения выделения диоксида углерода из конвертированного газа.
6.2.7. Какие мероприятия могут способствовать реализации концепции эффективного использования энергетических ресурсов в производстве аммиака?
-
переход на энерготехнологическую схему;
-
использование в качестве теплоносителя водяного пара вместо природного газа в отделении конверсии СН4;
-
снижение давления во всех отделениях;
-
уменьшение производительности ХТС;
-
использование радиальных реакторов вместо аксиальных.
6.2.8. Какие мероприятия могут способствовать снижению себестоимости аммиака?
-
снижение давления во всех отделениях;
-
увеличение производительности ХТС;
-
использование радиальных реакторов вместо аксиальных;
-
отказ от отделения очистки природного газа;
-
исключение из ХТС отделения выделения диоксида углерода из конвертированного газа;
-
снижение газовой нагрузки на колонну синтеза аммиака путем отказа от рецикла.
6.2.9. В функциональной схеме производства аммиака
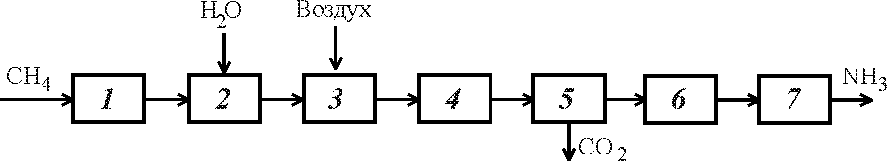
установите соответствие порядкового номера на схеме стадиям процесса, поименованным ниже:
-
(7)синтез аммиака;
-
(3)паровоздушная конверсия метана;
-
(2)паровая конверсия метана;
-
(4)конверсия диоксида углерода;
-
(6)очистка конвертированного газа от оксида углерода;
-
(5)очистка конвертированного газа от диоксида углерода;
-
(1)сероочистка природного газа.
6.2.10. Система очистки природного газа от серы включает процессы гидрирования и абсорбции. Что происходит в процессе очистки?
-
сначала гидрируются непредельные углеводороды природного газа, чтобы предотвратить закоксование поглотителя серы;
-
сначала адсорбируются соединения серы, затем проводится доочистка газа от серы в реакторе гидрирования;
-
сначала гидрируются все соединения серы до сероводорода, который затем поглощается в абсорбере;
-
сначала восстанавливается сера природного газа до элементарной серы, затем она отделяется в адсорбере;
-
гидрирование и адсорбция протекают в одном аппарате, что обеспечивает полноту выделения серы.
6.2.11. Выберите обоснование выбора способа конверсии метана в две стадии – паровая конверсия в трубчатом реакторе и паровоздушная конверсия в шахтном реакторе:
-
снижение энергетических расходов, поскольку гидравлическое сопротивление трубок меньше шахтного аппарата;
-
обеспечение "зажигания" катализатора (интенсивного начала процесса) путем подвода тепла дымовых газов в трубчатом реакторе;
-
увеличение температуры конверсии в шахтном реакторе путем ввода в него воздуха для сжигания части метана;
-
увеличение степени превращения метана, так как объем трубчатого реактора не достаточен для этого;
-
конверсия метана в две стадии плохо обоснован – процесс можно осуществить в одном реакторе при выборе соответствующего режима.
6.2.12. Как влияет температура Т и давление Р на степень превращения метана в процессе паровой конверсии природного газа?
-
Т увеличивает, Р увеличивает;
-
Т увеличивает, Р уменьшает;
-
Т уменьшает, Р уменьшает;
-
Т уменьшает, Р увеличивает.
6.2.13. Почему в конверсии природного газа одновременно протекают реакции СН4 + Н2O = СО + 3Н2 и СО + Н2O = СО2 + Н2, а на стадии конверсии оксида углерода только вторая из них?
-
конверсия СО идет при более низкой температуре, когда катализатор не влияет на скорость взаимодействия СН4 с Н20;
-
конверсию СО ведут при небольшом избытке воды, меньшем, чем в конверсии природного газа;
-
используется избирательный катализатор;
-
при температуре процесса конверсии СО равновесие реакции взаимодействия СН4 с Н2O сдвинуто в сторону полного превращения метана.
6.2.14. В современных схемах производства аммиака для извлечения СО2 из конвертированного газа используют методы:
-
адсорбция оксидом цинка;
-
абсорбция моноэтаноламином;
-
абсорбция азотной кислотой;
-
абсорбция поташом;
-
низкотемпературная ректификация конвертированного газа.
6.2.15. Какие концепции построения ХТС реализуются в узле очистки конвертированного газа от диоксида углерода?
-
регенерация теплоты;
-
утилизация отходов;
-
регенерация вспомогательных материалов с рециклом;
-
совмещение процессов.
6.2.16. Тепловой режим в реакторе синтеза аммиака в целом:
-
изотермический;
-
адиабатический;
-
политропический с отводом тепла.
6.2.17. Что определяет примерно одинаковую организацию процесса в реакторах синтеза аммиака, конверсии СО в производстве аммиака и окисления SO2 в производстве серной кислоты?
-
реакции каталитические;
-
реакции экзотермические;
-
реакции обратимые;
-
реакции обратимые экзотермические;
-
все вещества в газовой фазе;
-
использование наиболее простой схемы реактора – полочного.
6.2.18. Стехиометрическое соотношение H2:N2 = 3:1 в производстве аммиака необходимо соблюдать в первую очередь для:
-
достижения максимального выхода NH3;
-
предотвращения неполноты использования избыточного компонента;
-
предотвращения накопления избыточного компонента в рецикле;
-
обеспечения максимальной скорости процесса.
6.2.19. Энерготехнологическая схема в производстве аммиака обеспечивает:
-
уменьшение расхода теплоты и энергии в химико-технологических процессах;
-
увеличение количества вторичных энергетических ресурсов;
-
автономную работу по обеспечению энергией технологического процесса;
-
поддержание оптимального режима технологических процессов.
6.2.20. Какой теоретический расход природного газа (метана) на производство 1 т аммиака?
1) 242,5 м3; 2) 485 м3; 3) 910 м3; 4) 1250 м3.
6.2.21. Целесообразно ли заменить в производстве аммиака некоторые реакторы с аксиальным ходом газа на радиальные аппараты и почему?
-
нет, так как это увеличит материалоёмкость;
-
да, так как это уменьшит материалоёмкость;
-
нет, так как при этом возрастет гидравлическое сопротивление аппарата;
-
да, так как при этом уменьшится гидравлическое сопротивление аппарата;
-
нет, так как при этом увеличатся габариты аппарата;
-
да, так как при этом улучшится газораспределение;
-
да, так как при этом уменьшится диаметр аппарата.
6.3. Производство азотной кислоты
6.3.1.
В
функциональной
схеме производства разбавленной азотной
кислоты из аммиака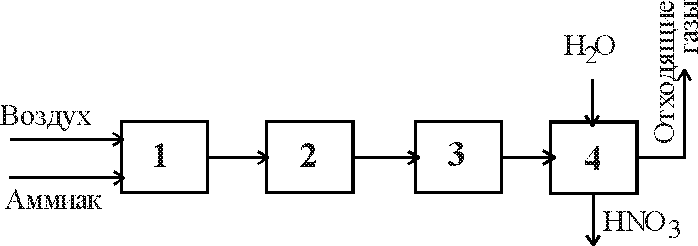
установите соответствие порядкового номера на схеме стадиям процесса, поименованным ниже:
-
очистка нитрозных газов;
-
экстракция оксида азота;
-
(1)окисление аммиака;
-
(3)окисление оксида азота до диоксида;
-
(2)охлаждение нитрозного газа;
-
(4)адсорбция диоксида азота;
6.3.2. Как влияет понижение температуры на процесс абсорбции оксидов азота водой?
-
не оказывает влияния;
-
увеличивает степень абсорбции;
-
снижает степень абсорбции.
6.3.3. Окисление аммиака на катализаторе протекает в области:
-
кинетической;
-
внутренней диффузии;
-
внешней диффузии.
6.3.4. Почему концентрация аммиака в исходной смеси в производстве азотной кислоты не превышает 11 об.%?
-
будет превышен предел взрывобезопасности;
-
уменьшится максимальная (равновесная) степень превращения;
-
катализатор дезактивируется при высокой концентрации NH3;
-
слой катализатора перегреется;
-
будет недостаточно кислорода для полного окисления NH3.
6.3.5. Рассчитайте максимальную (теоретическую) концентрацию азотной кислоты при ее получении из аммиака:
-
56%; 2) 74%; 3) 100%; 4) 83%.
6.3.6. Какой массовой концентрации соответствует 10 об.% NH3 в воздухе?
1) 6,2; 2) 10,0; 3) 8,7; 4) 12,0.
6.3.7. Какой температурный режим реализуется в процессе окисления аммиака на платиновом катализаторе в контактном аппарате?
-
изотермический;
-
адиабатический с последовательным повышением температуры реакционной смеси по мере увеличения степени превращения;
-
политермический с отводом тепла;
-
политермический с подводом тепла;
-
адиабатический с изотермией в слое сеток.
6.3.8. Как изменится степень окисления оксида азота NO в реакции
NO + 0,5O2 NO2 – H при повышении температуры?
-
увеличится;
-
уменьшится;
-
не изменится.
6.3.9. При абсорбции диоксида азота водой 3NO2 + H2O = 2HNO3 + NO образуется оксид азота NO. Как происходит его переработка в производстве азотной кислоты?
-
выбрасывается с отходящими газами;
-
возвращается на повторное окисление (рецикл);
-
окисляется в окислительном реакторе до NO2 и направляется на следующую ступень адсорбции;
-
окисляется между ступенями (тарелками) в абсорбере; ??????
-
утилизируется с получением дополнительного продукта.
6.3.10. Какой график правильно отображает влияние температуры Т на выход оксида азота ЕNO в реакторе окисления аммиака?
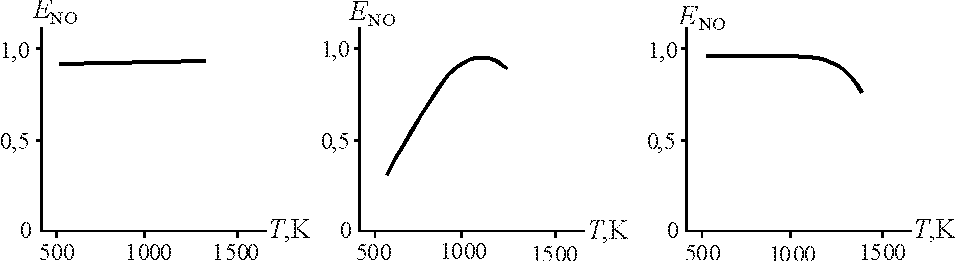
1 2 3
6.3.11. Из каких соображений выбирают давление выше атмосферного в производстве азотной кислоты?
-
для увеличения общей скорости окисления аммиака;
-
для достижения максимальной скорости окисления аммиака в оксид азота;
-
для увеличения скорости абсорбции диоксида азота;
-
для получения максимальной селективности по оксиду азота;
-
для снижения потерь платиноидов, уносимых газовой реакционной смесью с катализатора при высокой температуре.
-
для создания энерготехнологической схемы
-
для уменьшения габаритов технологических аппаратов
6.3.12. Выбрать правильный рисунок, изображающий влияние времени контакта аммиачно-воздушной смеси с катализатором на выход оксида азота ЕNO.
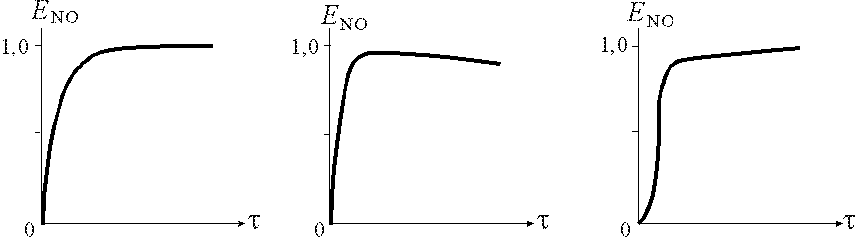
1 2 3
6.3.13. Как влияет соотношение О2 : NH3 в аммиачновоздушной смеси на выход оксида азота?
-
не влияет на выход;
-
с увеличением содержания кислорода против стехиометрии выход оксида азота увеличивается;
-
отклонение соотношения О2 : NH3 от стехиометрического всегда уменьша-ет выход оксида азота;
-
повышение содержания NH3 против стехиометрии увеличивает выход оксида азота;
-
уменьшение содержания NH3 на входе против стехиометрии повышает выход оксида азота.
6.3.14. Какие данные необходимо иметь для расчета выхода оксида азота?
-
концентрацию аммиака на входе и выходе;
-
концентрацию аммиака на входе и оксида азота на выходе;
-
концентрацию оксида азота и аммиака на выходе;
-
степень превращения аммиака, концентрацию аммиака и оксида азота на выходе;
5) концентрацию аммиака и кислорода на входе и на выходе.
6.3.15. Какие реакции из приведенной ниже химической схемы окисления аммиака следует взять для проведения балансовых расчетов процесса?


 1
NO
1
NO
 NH3
4 2
NH3
4 2
3 N2
1) 1 и 2; 2) 1 и 3; 3) 1, 2 и 3; 4) 4; 5) 1, 2, 3, 4
6.3.16. Как происходит санитарная очистка отходящих газов от оксидов азота в производстве азотной кислоты?
-
адсорбцией на твердых поглотителях;
-
фильтрованием на специальных фильтрах-мембранах;
-
абсорбцией щелочным раствором;
-
каталитическим восстановлением до азота;
-
промывкой газа в скруббере.
Тесты с защиты лабораторной работы
1. Укажите способы увеличения равновесного превращения SO2 в SO3 :