Материал: Методичка 4400 с ответами
6. Химические производства
6.1. Производство серной кислоты
6.1.1. В какой области протекает каталитический процесс окисления SO2 в промышленном реакторе?
-
в кинетической;
-
во внутридиффузионной;
-
во внешнедиффузионной;
-
в переходной.
6.1.2. Укажите способы увеличения равновесного превращения SO2 в SO3:
1) увеличение концентрации SO2 при постоянной концентрации О2;
2) уменьшение концентрации SO2 при постоянной концентрации О2;
3) увеличение давления;
4) увеличение температуры;
5) уменьшение температуры;
6) вывод SO3 из газовой смеси.
Выбрать сочетание правильных ответов:
1) 1, 2, 7; 2) 1, 3, 4, 6; 3) 1, 3, 5, 6; 4) 3, 5; 5) 3, 4, 6; 6) 2, 3, 5, 6.
6.1.3. Как влияет увеличение исходной концентрации SO2 на равновесную степень превращения SO2 в SO3 при постоянном соотношении О2:SO2?
-
проходит через максимум;
-
уменьшается;
-
не влияет;
-
увеличивается;
-
проходит через минимум.
6.1.4. Как изменяется константа равновесия реакции окисления SO2 с увеличением температуры?
-
увеличивается;
-
зависит от теплового режима в реакторе;
-
проходит через максимум;
-
проходит через минимум;
-
уменьшается.
6.1.5. Как изменяется фактическая степень превращения SO2 с увеличением температуры при постоянном времени контакта ?
-
снижается;
-
возрастает;
-
проходит через минимум;
-
проходит через максимум;
-
характер изменения определяется моделью реактора.
6.1.6. Экспериментально получено, что при температуре Т1 степень превращения равна х1. Какое значение х2 при температуре Т2 можно ожидать, если Т2 > Т1 и остальные условия эксперимента сохранены?
1) х2 = х1; 2) х2 < х1; 3) х2 ≥ х1; 4) х2 ≤ хI; 5) х2 > хI.
6.1.7. Укажите способы увеличения скорости контактного окисления SO2:
-
увеличение давления;
-
снижение давления;
-
увеличение температуры.
-
снижение температуры;
-
поддержание температуры на определенном уровне;
-
увеличение концентрации SO2;
-
увеличение концентрации О2;
-
увеличение концентрации SO3.
6.1.8. Какие данные необходимы для определения необходимого объема катализатора в контактном аппарате?
1) производительность аппарата;
2) сопротивление слоя катализатора;
3) скорость химической реакции;
4) активность катализатора;
5) концентрация реагентов;
6) заданная степень превращения;
7) степень приближения режима к линии оптимальных температур.
Выбрать сочетание правильных ответов:
1) 1, 3, 4, 5, 6; 2) 1, 2, 4; 3) 2, 3, 6; 4) 1, 2, 4, 5, 6; 5) 2, 4, 6, 7; 6) 1, 2, 4, 5, 6, 7.
6.1.9. Какие показатели процесса окисления SO2 могут быть улучшены, если процесс будет протекать в оптимальном температурном режиме при заданном времени реакции τ ?
1) степень превращения SO2 в SO3;
2) скорость процесса окисления SO2;
3) тепловые потери в окружающую среду;
4) продолжительность срока службы катализатора;
5) качество получаемого продукта.
Выбрать сочетание правильных ответов:
1) 1, 3, 4; 2) 4, 5; 3) 1, 2; 4) 2, 4, 5; 5) 1, 4, 5; 6) 1.
6.1.10. Как влияет увеличение концентрации SO2 в исходном газе на изменение температуры в слое катализатора в адиабатическом процессе?
-
температура уменьшается;
-
температура остается постоянной;
-
зависимость температуры от концентрации проходит через максимум;
-
температура увеличивается;
-
зависимость температуры от концентрации проходит через минимум.
6.1.11. Какой режим реализуется в реакционной зоне полочного контактного аппарата с неподвижным слоем катализатора для окисления SO2 в SO3?
-
идеального вытеснения, изотермический;
-
идеального смешения, адиабатический;
-
идеального смешения, политропический;
-
идеального смешения, изотермический;
-
идеального вытеснения, адиабатический.
6.1.12. Чем обусловлена необходимость секционирования реакционной зоны (слоя катализатора) в контактном аппарате?
-
для уменьшения механической нагрузки на опору слоя катализатора;
-
для улучшения условий теплообмена;
-
для снижения гидравлического сопротивления аппарата;
-
для приближения температурного режима процесса к оптимальному;
-
для сдвига равновесия реакции.
6.1.13. Можно ли получить степень превращения SO2, равную 98,5%, в контактном аппарате с одним слоем катализатора?
-
нет, потому что линейная скорость потока мала;
-
да, в трубчатом реакторе с использованием хладагента;
-
да, но только в адиабатическом режиме;
-
да, в схеме с рециклом;
-
да, если слой катализатора функционирует в режиме псевдоожижения.
6.1.14. Почему в промышленности для окисления SO2 в SO3 используют многослойные полочные реакторы с неподвижным слоем катализатора:
-
в адиабатическом режиме в одном слое реактора невозможно достигнуть степени превращения SO2, близкой к 100%;
-
в трубчатом реакторе из-за ограниченного количества трубок практически невозможно расположить необходимый объем катализатора для обеспечения производительности 300 т/сутки и выше;
-
несколько слоев нужны для удобства размещения теплообменников;
-
из-за низкой активности катализатора и его высокой температуры зажигания;
-
из-за низкой коррозионной стойкости конструкционных сталей.
6.1.15. Какой критерий оптимальности используется при построении линии оптимальных температур?
-
минимальная степень превращения SO2;
-
минимальная концентрация сернистого ангидрида;
-
максимальная скорость реакции при заданном составе реакционной смеси;
-
минимальная степень превращения по кислороду;
-
максимальный выход SO3.
6.1.16. Почему процесс окисления SO2 в промышленных условиях начинают при 4200С?
-
при этом достигается максимальная степень превращения в первом слое катализатора;
-
это минимальная температура, обеспечивающая необходимую скорость процесса;
-
эта температура соответствуют оптимальному режиму работы предшествующих стадий процесса – отделение обжига и очистки газа;
-
при этом достигается автотермичность работы контактного аппарата;
-
это оптимальная температура, обеспечивающая максимальный коэффициент теплопередачи в теплообменнике после первого слоя контактного аппарата.
6.1.17. Почему в многослойном контактном аппарате объём катализатора увеличивается в каждом слое по ходу газа?
-
это определяется конструктивными соображениями;
-
это определяется условиями теплообмена;
-
это связано с уменьшением скорости реакции по слоям из-за снижения концентраций;
-
это определяется гидродинамическим расчетом;
-
это зависит от активности катализатора.
6.1.18. Какое максимальное содержание SO2 в газовой смеси может быть получено при сжигании серы в кислороде воздуха?
1) 100%; 2) 21%; 3) 16%; 4) 79%; 5) 8,2%.
6.1.19. Какие конструкции реакторов для проведения процесса окисления SO2 в присутствии катализатора можно использовать?
-
реактор идеального смешения изотермический;
-
реактор идеального вытеснения с отводом тепла;
-
многослойный реактор с подводом тепла;
-
многослойный реактор с промежуточным отводом тепла;
-
реактор с псевдоожиженным слоя катализатора и отводом тепла;
-
адсорбер с кольцевыми насадками.
6.1.20. Чем определяется минимальное время контакта реакционного потока в слое катализатора для процесса окисления SO2 при заданной степени превращения SO2?
-
условиями оптимального температурного режима;
-
гидравлическим сопротивлением слоя катализатора;
-
адиабатическим разогревом;
-
равновесной степенью превращения;
-
размером зерна катализатора;
-
объемной скоростью подачи реагентов;
-
температурным интервалом работы катализатора.
6.1.21. Как определяется оптимальное количество катализатора в реакторе и его секционирование по слоям для процесса окисления SO2 в SO3?
-
по значению равновесной степени превращения SO2;
-
из условий оптимизации режима;
-
типом катализатора;
-
по начальным концентрациям SO2 и О2;
-
по количеству катализатора, загруженного в аппарат;
-
по температуре хладагента в теплообменниках.
6.1.22. Зачем в процессе окисления SO2 используют катализатор?
-
для смещения равновесия в сторону образования конечного продукта SO3;
-
для снижения температуры процесса;
-
для повышения степени превращения SO2;
-
для повышения скорости процесса окисления SO2;
-
для повышения избирательности процесса;
-
для снижения константы скорости обратной реакции;
-
для увеличения константы скорости прямой реакции окисления SO2.
6.1.23. Какие данные необходимы для расчета величины адиабатического разогрева окисления SO2?
-
концентрация SO3;
-
теплоемкость реакционной смеси;
-
концентрации всех исходных веществ;
-
заданная степень превращения SO2;
-
температура зажигания катализатора;
-
равновесная степень превращения SO2 ;
-
тепловой эффект реакции;
-
температурный режим работы катализатора;
-
количество катализатора в слое;
-
концентрация SO2 на входе в реактор.
6.1.24. Может ли быть достигнута заданная степень превращения SO2 в присутствии катализатора, если процесс вести не по линии оптимальных температур (ЛОТ), а в интервале температур работы катализатора?
-
да, но необходимо обеспечить дополнительный теплоотвод;
-
нет, так как линия оптимальных температур определяет достигаемую степень превращения;
-
да, но время контакта для достижения заданной степени превращения при этом возрастет;
-
нет, поскольку катализатор работает не в оптимальном режиме.
6.1.25. В функциональной схеме производства серной кислоты из серосодержащего сырья
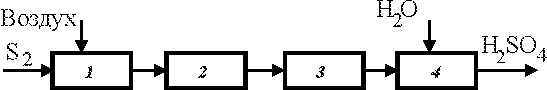
установите соответствие порядкового номера на схеме стадиям процесса, поименованным ниже:
-
(2)очистка и промывка обжигового газа;
-
(3)окисление SO2;
-
(1)обжиг серосодержащего сырья;
-
десорбция SO2;
-
(4)абсорбция SO3;
-
десорбция SO3.
6.1.26. В функциональной схеме производства серной кислоты из серного колчедана
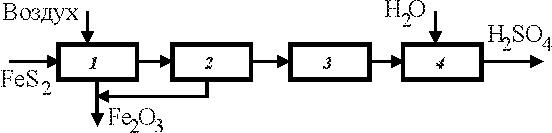
установите соответствие порядкового номера на схеме стадиям процесса, поименованным ниже:
-
десорбция SO2;
-
десорбция SO3;
-
(1)обжиг серосодержащего сырья;
-
(3)окисление SO2;
-
(2)очистка и промывка обжигового газа;
-
(4)абсорбция SO3.
6.1.27. В схеме реактора окисления SO2 в SO3 в производстве серной кислоты
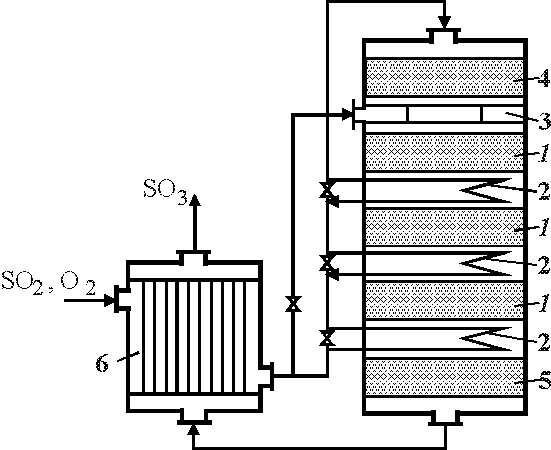
установите соответствие номера элемента реактора его наименованию:
-
слой колец Рашига;
-
(3)смеситель;
-
(1,4,5)слой катализатора;
-
(2)промежуточные теплообменники;
-
слой активированного угля;
-
(6)внешний теплообменник.
6.1.28. Чем определяется выбор концентрации 98,3% серной кислоты в качестве орошающей жидкости при абсорбции SO3?
-
минимальным разогревом;
-
максимальной движущей силой;
-
минимальной коррозионной активностью жидкости в абсорбере;
-
минимальной коррозионной активностью отходящих газов.
-
экономическими соображениями;
6.1.29. Если SO3 на стадии получения серной кислоты абсорбировать олеумом, то поглощение будет:
-
полным;
-
неполным;
-
отсутствовать.
6.1.30. В функциональной схеме производства серной кислоты по методу «двойное контактирование – двойная абсорбция» на основе серы
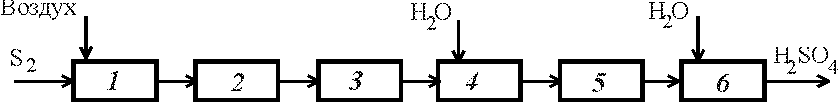
установите соответствие порядкового номера на схеме стадиям процесса, поименованным ниже:
-
(3)первая стадия окисления SO2;
-
(5)вторая стадия окисления SO2;
-
(6)вторая стадия абсорбции SO3;
-
(4)первая стадия абсорбции SO3;
-
(2)промывка обжигового газа;
-
(1)обжиг серосодержащего сырья.
6.1.31. Почему концентрация SO2 в исходной смеси в промышленных условиях не превышает 10 об. %?
-
будет превышен предел взрывобезопасности;
-
уменьшится максимальная (равновесная) степень превращения;
-
катализатор дезактивируется при высокой концентрации SO2;
-
слой катализатора перегреется;
-
экономически невыгодно;
-
будет недостаточно кислорода для полного окисления SO2.
6.1.32. За счет чего достигается более полное окисление диоксида серы в производстве серной кислоты по схеме "двойное контактирование двойная абсорбция"?
-
увеличивается объём катализатора;
-
улучшаются условия отвода тепла;
-
увеличивается скорость процесса;
-
сдвигается равновесие реакции;
-
осуществляется вывод продукта из зоны реакции.
6.1.33. Предложите мероприятия, способствующие реализации концепции минимизации отходов в производстве серной кислоты:
-
уменьшение концентрации диоксида серы;
-
выбор оптимальной концентрации орошающей кислоты;
-
внедрение схемы ДК-ДА;
-
использование контактного аппарата с кипящими слоями катализатора.