Материал: mass_spectr
имеют сходную картину распада молекулярного иона. Например, в спектрах моноалкилбензолов присутствует осколочный ион с m/z = 91, соответствующий образованию катиона тропилия в результате бензильного разрыва, что может быть использовано при установлении структуры. Масс-спектр органического соединения, записанный в условиях электронной ионизации, обладает высокой индивидуальностью. Получается своего рода отпечаток пальца молекулы, с помощью которого проводят идентификацию. Для этого масс-спектр анализируемого образца сравнивают с масс-спектрами известных соединений, сопоставляя величины m/z и интенсивности всех сигналов. В настоящее время эту работу выполняет компьютер масс-спектрометра, сразу выдавая совпавшие структуры.
Как и любой другой метод ионизации, описанный здесь, электронная ионизация имеет свои преимущества и недостатки.
Преимущества:
Наиболее изученный метод ионизации;
Может использоваться для ионизации практически любых летучих соединений;
Высокая воспроизводимость спектров;
Фрагментация позволяет получить информацию о строении соединения;
Возможность идентификации соединений сравнением полученного массспектра со спектрами из базы данных.
Недостатки:
Анализируемое вещество должно обладать достаточной летучестью и термической стабильностью;
Отсутствие или низкая интенсивность в спектрах многих соединений сиг-
нала молекулярного иона затрудняет идентификацию.
Диапазон масс: до 1000 Да.
11
1.2 Химическая ионизация (chemical ionization, CI)
Несмотря на ряд достоинств, метод электронной ионизации во многих случаях не позволяет установить молекулярную массу соединения из-за отсутствия молекулярного пика в спектре и установить реальную структуру становится крайне затруднительно. Поиск альтернативных методов, которые позволили бы решить эту проблему, привел к разработке в 1966 г. Мансоном и Филдом новой техники получения масс-спектров, названной химической ионизацией. Это намного более «мягкий» метод ионизации, в ходе которого молекулярный ион получает небольшую порцию избыточной энергии и степень фрагментации оказывается весьма незначительной. Иногда спектр содержит только пик молекулярного иона. Как же это достигается?
Если проводить взаимодействие пучка электронов с молекулами вещества в условиях высокого вакуума, как при ионизации электронным ударом, основным направлением реакции будет образование катион-радикалов. Если проводить аналогичное облучение вещества при более высоком давлении (до 1 мм рт. ст.), образующиеся ионы будут взаимодействовать с нейтральными молекулами, давая различные типы новых ионов. Например, при облучении метана электронами протекают следующие превращения:
CH4 +e → CH4+• +2e CH4+• → CH3+ + H •
CH4+• +CH4 → CH5+ +CH3•
CH3+ +CH4 → C2 H5+ + H2 и т.д.
Если теперь полученные ионы ввести в ионизационную камеру с молекулами исследуемого вещества, предварительно переведенными в газообразное состояние, между ними могут протекать различные реакции:
а) протонирование:
M + BH + → MH + + B
12
в случае метана: M +CH5 + → MH + +CH4
б) перезарядка:
M+ X +• → M +• + X
вслучае метана: M +CH 4 +• → M +• +CH 4
в) электрофильное присоединение:
M + X + → MX +
в случае метана: M +C2 H5 + →[M +C2 H5 ]+
Как видно, все эти реакции приводят к генерированию из нейтральной молекулы заряженных ионов, преимущественно катионов, которые стабильнее катионрадикалов и имеют больше шансов достичь детектора. Данный процесс и называется химической ионизацией, а метан выступает в роли газа-реагента. На рисунке 6 приведены масс-спектры три-н-бутиламина, полученные в условиях электронной и химической ионизации и показывающие преимущества последнего метода для определения молекулярной массы.
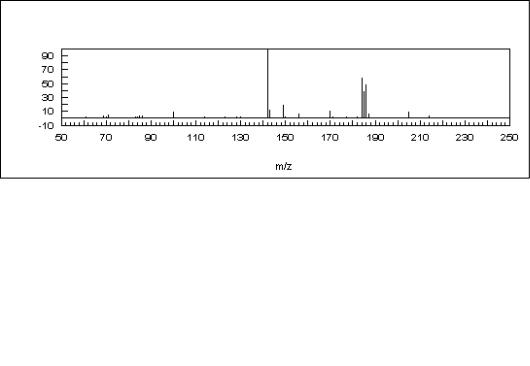
Электронная ионизация, 70 эВ
Химическая ионизация, газ-реагент – метан
Рисунок 6 – Масс-спектры три-н-бутиламина (Mr = 185), записанные в условиях электронной (вверху) и химической (внизу) ионизации
13
В качестве газа-реагента может быть использовано практически любое летучее вещество. Помимо метана часто применяют изобутан, аммиак и аргон. В случае аргона возможен только один путь взаимодействия с веществом – перезарядка, поэтому в таком масс-спектре отсутствуют протонированные ионы и продукты электрофильного присоединения. При использовании изобутана помимо молекулярного иона в спектре присутствуют интенсивные сигналы ионов [M + H]+ и [M + C4H9]+, а если газ-реагент – аммиак, то наблюдаются ионы [M + H]+ и [M + NH4]+.
Информация, получаемая в условиях химической ионизации, дополняет данные электронной ионизации, и их комбинация является мощным инструментом в установлении структуры.
Преимущества:
Позволяет получить информацию о молекулярной массе соединения;
Масс-спектр намного проще, чем при ионизации электронами.
Недостатки:
Как и в случае электронной ионизации, анализируемое вещество должно обладать достаточной летучестью и термической стабильностью;
Поскольку осколочных ионов практически не образуется, метод в большинстве случаев не позволяет получить информацию о строении вещества;
Результат сильно зависит от типа газа-реагента, его давления, времени взаимодействия с веществом, поэтому очень трудно добиться воспроизводимых результатов.
Диапазон масс: как и в случае электронной ионизации до 1000 Да.
14

1.3 Ионизация электрическим полем (field ionization, FI) и
полевая десорбция (field desorption, FD)
|
Оба метода относятся к «мягким» способам ио- |
|
низации и имеют практически одинаковое ап- |
|
паратное оформление и механизм воздействия |
|
на вещество. Ключевую роль играет проволоч- |
|
ный эмиттер, поверхность которого покрыта |
|
микроиглами (рисунок 7). Между эмиттером и |
Рисунок 7 – Вид эмиттера под |
ускоряющим катодом поддерживается разность |
микроскопом |
потенциалов 8–10 кВ. Благодаря малому радиу- |
су кривизны на концах игл создается высокая напряженность электрического поля. Молекулярные орбитали вещества под действием поля искривляются, и происходит туннелирование электронов из молекулы на эмиттер. Энергия, переносимая в результате этого процесса, составляет доли электрон-вольт, причем избыточная энергия молекулярного иона оказывается даже ниже, чем в условиях химической ионизации, поэтому в большинстве случаев пик молекулярного иона является единственным сигналом в спектре (рисунок 8). Высокий положительный потенциал эмиттера выталкивает образовавшийся молекулярный ион по направлению к детектору.
CH3
Mr = 92.14
Рисунок 8 – Масс-спектр толуола, полученный при ионизации электрическим полем
15