Материал: mass_spectr
1 Основные способы ионизации
1.1 Электронная ионизация (electron ionization, EI)
Является одним из наиболее известных способов ионизации. Несмотря на то, что это исторически первый метод ионизации органических соединений, предложенный еще в 1934 г., он не потерял актуальности до наших дней.
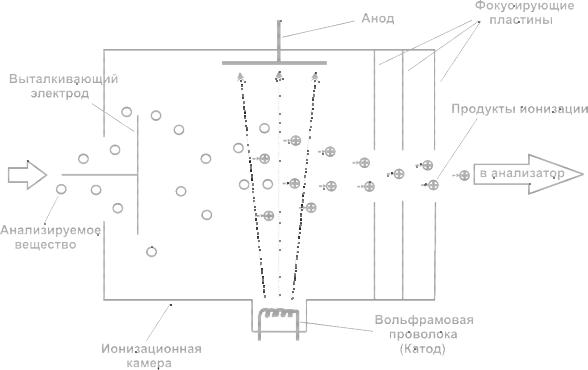
Для ионизации вещества используется поток электронов с высокой энергией. На рисунке 2 приведена схема типичной установки, применяемой для этих целей.
Рисунок 2 – Устройство прибора для электронной ионизации
Источником электронов является нагретая металлическая проволока (катод). Электроны, покидающие поверхность катода, разгоняются электрическим полем по направлению к аноду. Путь электронов проходит через объем, занятый анализируемым веществом, предварительно переведенным в газообразное состояние (в ионизационной камере поддерживается разряжение 10–5 – 10–6 мм рт. ст.), с молекулами которого происходит взаимодействие, заключающееся в передаче энергии. Однако следует понимать, что реального соударения молекул и электронов не происходит. Электрон, пролетая вблизи молекулы, вызывает лишь воз-
6
возбуждение ее электронной оболочки, поэтому термин «электронный удар» (electron impact), который часто используется как альтернативное название для этого метода, не соответствует действительности. Результатом такого возбуждения является перемещение собственных электронов молекулы на более высоколежащие орбитали. Начиная с определенных значений энергии (энергия ионизации), возбуждение заканчивается потерей электрона и превращением молекулы в соответствующий катион-радикал, называемый молекулярным ионом.
M +e → M +• + 2e
Образующиеся катион-радикалы выталкиваются специальным электродом из ионизационной камеры и после фокусировки в узкий пучок направляются в анализатор. Для достижения ионного детектора каждому иону требуется в среднем не более 2×10–5 с.
Важным параметром является энергия ионизирующих электронов. Стандартные масс-спектры EI принято снимать, используя электроны с энергией 70 эВ, что соответствует ускоряющему потенциалу между катодом и анодом в 70 В. Выбор такой энергии не случаен. Во-первых, при этом достигается максимальная эффективность ионизации и, во-вторых, только в этом случае получается воспроизводимый масс-спектр.
Энергии ионизации большинства органических соединений лежат в диапазоне 6– 12 эВ. Это, в свою очередь, означает, что образующийся после взаимодействия молекулы с пучком электронов катион-радикал получает избыточную энергию, которая усиливает колебания связей и может стать причиной разрыва наиболее слабых из них (фрагментация). В результате фрагментации происходит распад молекулярного иона на две частицы, одна из которых – ион с меньшей массой (осколочный ион), вторая – радикал или нейтральный фрагмент. Незаряженные радикалы (X•) и нейтральные частицы (N) прибором не записываются.
M +• →[M − N]+• + N
M +• →[M − X ]+ + X •
7
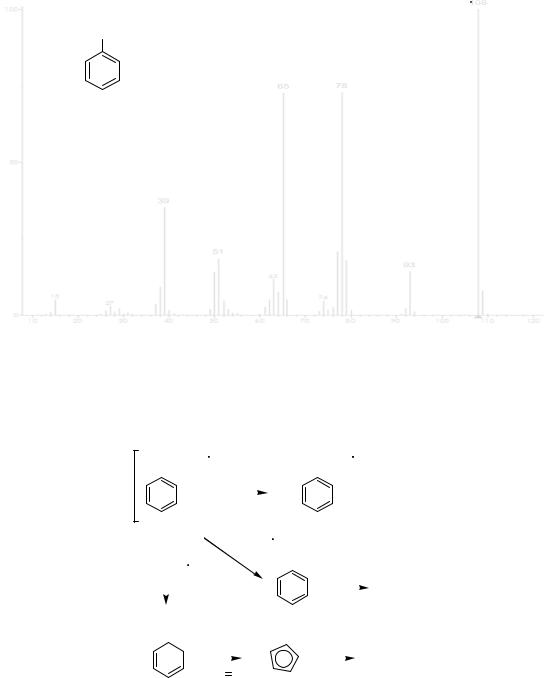
Если избыточная энергия осколочного иона остается высокой, он может распадаться дальше на еще более мелкие фрагменты. Типичный масс-спектр, получаемый в условиях электронной ионизации, представлен на рисунке 3. По оси абсцисс откладывается масса ионов (величина m/z), а по оси ординат – их интенсивность (относительное количество).
OCH3
Mr = 108
Рисунок 3 – Масс-спектр анизола
В выбранном примере основные направления фрагментации молекулы анизола выглядят так:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OCH3 |
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- H2C |
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
m/z 108 |
|
- CH3O |
m/z 78 |
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
- CH3 |
|
|
|
|
|
|
|
|
|
|
|
C H |
+ |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4 |
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- C2H2 |
m/z 51 |
|||||||||
|
|
O |
|
|
|
|
m/z 77 |
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C H |
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
- C O |
|
- C2H2 |
3 |
3 |
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
m/z 39 |
|
||||||||||||||||||||||
m/z 93 |
|
|
|
|
m/z 65 |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
В данном случае пик молекулярного иона – молекулярный пик – является в спек-
8
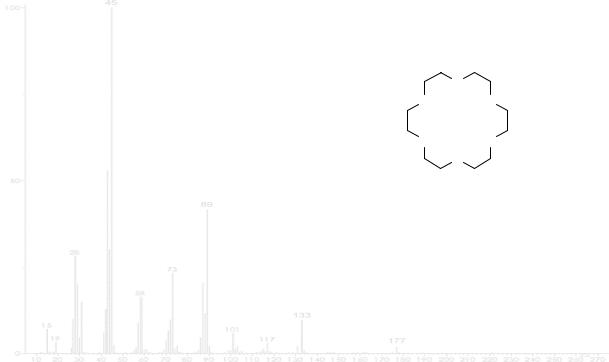
тре самым интенсивным, что свидетельствует о высокой устойчивости образующегося катион-радикала. По мере увеличения склонности молекулярного иона к фрагментации, его интенсивность в масс-спектре относительно осколочных ионов будет падать. Крайним случаем является полное отсутствие молекулярного пика в спектре, что существенно затрудняет идентификацию соединения. Примером является циклический эфир 18-краун-6 (рисунок 4), в спектре которого самым тяжелым ионом является частица с массой 177 [(C2H4)4O4H]+. Это может ввести в заблуждение относительно реальной молекулярной массы исследуемого соединения. Поэтому интерпретация спектров, полученных ионизацией электронным ударом, должна проводиться с большой осторожностью.
O
O O
O O
O
Mr = 264
Рисунок 4 – Масс-спектр 18-краун-6
Наиболее очевидным путем решения проблемы низкой интенсивности сигнала молекулярного иона является понижение энергии электронного пучка, используемого для ионизации. В этом случае молекулярный ион получает меньшую избыточную энергию и, соответственно, в меньшей степени претерпевает фрагментацию. На рисунке 5 приведены масс-спектры пропанола-1, записанные с изменением энергии ионизирующих электро-9электронов. Однако использование
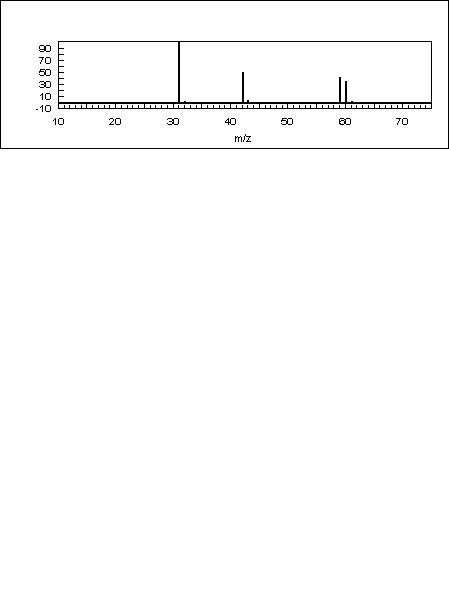
данного подхода имеет и обратную сторону: электроны с низкой энергией ионизируют намного меньше молекул образца и для регистрации спектра необходимы более чувствительные детекторы.
70 эВ
20 эВ
14 эВ
11 эВ
Рисунок 5 – Масс-спектры пропанола-1 (Mr = 60), записанные при различных энергиях ионизирующих электронов
Не стоит думать, что ценность электронной ионизации заключается лишь в возможности определения молекулярной массы анализируемого соединения, тем более что это не всегда возможно. Весьма важная информация заключается в характере фрагментации. Соединения, принадлежащие к одному и тому же классу,
10