Материал: Лабораторный практикум
1 – измерительный модуль (медная пластина), 2 – внешний корпус, 3 – влагоудерживающая засыпка (насыщенный раствор медного купороса); 4 – измерительный
кабель, 5 – термоусаживаемая муфта, 6 – вспомогательный электрод, 7 – измерительный провод вспомогательного электрода
чивается через ионообменную мембрану, смачивает ее и создает через раствор сульфата меди гальванический контакт между медным стержнем и грунтом. Возникающая постоянная разница потенциала на границе «медь – насыщенный раствор сульфата меди» сравнивается с разницей потенциала на границе «защищаемый объект — окружающий грунт» с помощью приборов
(рисунок 3.2).
Практическая часть
1.Очистите стальной и цинковый электроды от грязи и продуктов коррозии.
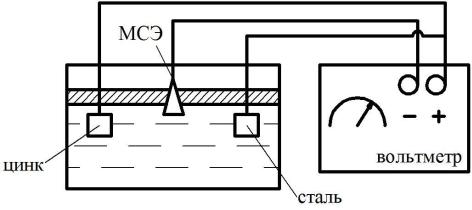
2.Соберите лабораторную установку как показано на рисунке 3.3.
Установите электроды, а также МСЭ в емкость с водой. Для измерения потенциалов металлов необходимо составить гальваническую пару, в которой одним электродом будет один из металлов, вторым – МСЭ.
Рисунок 3.3 – Схема лабораторной установки
21
1 – емкость с водой, 2 - милливольметр
3. Для измерения потенциала каждой пары подключите клемму МСЭ к отрицательной клемме милливольтметра, а металлического электрода – к
положительной клемме. Измерьте электродные потенциалы пластинок и запишите полученные данные в таблицу 3.1.
Таблица 3.1 – Форма записи результатов проведения испытания
Материал |
Значение потенциала, В |
|
|
|
|
|
|
4. Сделать вывод о том, какой металл является более электрически отрицательным, а также какой их двух металлов начнет разрушаться при соединении их в гальваническую пару.
22
Лабораторная работа №4
Пассивность стали
Цель работы: ознакомиться с явлением пассивируемости стали;
экспериментальным путем исследовать пассивируемость стали в
окислителях.
Оборудование и материалы: 4 образца пластинок из углеродистой стали, растворы азотной кислоты HNO3 с различной концентрацией (20, 30, 40, 50 и 60%), медно-сульфатный электрод сравнения, милливольтметр.
Теоретическая часть
Пассивность – состояние относительно высокой коррозионной стойкости металла, вызванное торможением анодного процесса электрохимической коррозии.
Повышенная коррозионная стойкость металлов может быть обусловлена различными причинами, в частности термодинамической устойчивостью, т.е.
инертностью металла, отсутствием в электролите деполяризатора и т.д.
Однако под пассивностью принято подразумевать только состояние повышенной коррозионной устойчивости, связанное с торможением анодного процесса коррозии, наблюдаемого при определенных условиях.
Наступление пассивного состояния металлов характеризуется следующими явлениями:
1)резкое уменьшение скорости коррозии металла в пассивном состоянии;
2)значительное смещение потенциала металла в положительную сторону (у железа может происходить смещение потенциала до +1 В).
23
Пассивное состояние металлов вызывают обычно окислительные процессы, протекающие вследствие наличия в растворе окислителей –
пассиваторов (например, O2, HNO3, K2Cr2O7 и др.) или вследствие анодной поляризации металла – пассивирующих факторов и образующие на поверхности металлов адсорбционный слой кислорода или защитную окисную пленку. Пассивность металлов зависит как от внутренних факторов,
связанных со свойствами металлов (состав и структура, состояние поверхности и др.), так и от внешних условий, при которых металл взаимодействует с электролитом (температура, движение раствора,
наложение постоянного тока и т.д.).
О большей или меньшей склонности металла к пассивированию можно судить по пассивирующей концентрации окислителя или пассивирующей анодной плотности тока. Пассивное состояние металла может в большей или меньшей степени сохраниться и после изменения внешних пассивирующих условий. Нарушают пассивное состояние или затрудняют его наступление восстановители, катодная поляризация, некоторые («активные») ионы
(например, Cl-, SO42- и др.), повышение температуры, механическое нарушение пассивной поверхности и т.д.
Явление пассивности металлов имеет большое практическое значение,
так как коррозионная стойкость многих технических металлов и сплавов определяется их пассивируемостью в определенных условиях. В частности,
правильный выбор стали трубопровода, склонной к пассивированию в данных условиях пролегания трассы, позволит в значительной мере сократить потери металла от коррозии и скорость самой коррозии, тем самым повысить эксплуатационную надежность и долговечность трубопровода.
Практическая часть
24
1.Зачистите наждачной бумагой и обезжирьте органическим растворителем образцы металлических пластинок.
2.Один из стальных образцов поочередно погружайте в стаканы с растворами HNO3, начиная с концентрации 20% и кончая 60% с выдержкой при каждой концентрации по 10 секунд. При каждом погружении образца наблюдайте за скоростью растворения стали в растворе HNO3 и отметьте концентрацию кислоты, при которой наступает пассивность стали –
прекращается выделение пузырьков газа. Результаты наблюдений запишите в таблицу 4.1 (опыты 1-5).
Таблица 4.1 – Форма записи результатов проведения экспериментов
Номер |
Концентрация |
Наблюдения |
Потенциал |
|
опыта |
HNO3, % |
образцов U, В |
||
|
||||
|
|
|
|
|
1 |
20 |
|
|
|
|
|
|
|
|
2 |
30 |
|
|
|
|
|
|
|
|
3 |
40 |
|
|
|
|
|
|
|
|
4 |
50 |
|
|
|
|
|
|
|
|
5 |
60 |
|
|
|
|
|
|
|
|
6 |
50 |
|
|
|
|
|
|
|
|
7 |
40 |
|
|
|
|
|
|
|
|
8 |
30 |
|
|
|
|
|
|
|
|
9 |
20 |
|
|
|
|
|
|
|
|
10 |
20 |
|
|
|
|
|
|
|
3. Извлеките образец стали из 60%-ого раствора кислоты и поочередно погружайте на 10 секунд в растворы начиная с концентрации 50% и кончая
20%. Наблюдайте за поведением образца стали. Результаты наблюдений
(происходит растворение стали или нет) запишите в таблицу 4.1 (опыты 6-9).
4. Погрузите вторую стальную пластинку в 20%-ый раствор кислоты и приведите ее в контакт с находящейся там пассивированной первой
25