Материал: Лабораторный практикум
фазы заряжаются. Энергетическое состояние электронов на концах разомкнутой цепи оказывается неодинаковым: на цинковом электроде энергия Гиббса электронов выше, а на медном электроде – ниже. Разность энергий Гиббса электронов на концах цепи и определяет ЭДС данного элемента.
При замыкании внешней цепи электроны перемещаются от цинкового электрода к медному. В этом случае равновесие на фазовых границах нарушается, происходит направленный переход ионов цинка из металла в раствор, ионов меди – из раствора в металл, электроны протекают от цинка к меди. Так осуществляется окислительно-восстановительная реакция в гальваническом элементе Якоби – Даниэля, так, в принципе, образуется ЭДС в любом гальваническом элементе при контакте двух различных металлов.
Практическая часть
1.Налейте в пробирку 5-6 мл раствора серной кислоты.
2.Поочередно опустите туда алюминиевую, железную и медную пластинку. Наблюдайте медленное выделение водорода. Объясните выделение водорода на пластинках.
3.Опустите в пробирку медную и алюминиевую пластину и приведите их в электрический контакт. Наблюдайте выделение водорода на медной пластинке. Объясните выделение водорода на медной пластинке.
4.Опустите в пробирку медную и железную пластину и приведите их в электрический контакт. Наблюдайте выделение водорода на железной пластинке. Объясните выделение водорода на железной пластинке.
16
5.Опустите в пробирку железную и медную пластину и приведите их в электрический контакт. Наблюдайте выделение водорода на медной пластинке. Объясните выделение водорода на медной пластинке.
6.Сделайте вывод о порядке расположения железа, алюминия и меди в электрохимическом ряду напряженности металлов.
17
Лабораторная работа №3
Электродный потенциал металлов относительно медно-
сульфатного электрода сравнения
Цель работы: ознакомиться с понятием электродного потенциала металлов; экспериментальным путем определить электродные потенциалы представленных образцов металлов.
Оборудование и материалы: образцы стальной и цинковой пластинок,
медно-сульфатный электрод сравнения, милливольтметр, емкость с водой.
Теоретическая часть
Электродный потенциал – это разность электрических потенциалов между электродом и электролитом.
Разность потенциалов между металлом и раствором, в который он погружен, можно измерить, «соединив» раствор проводником с измерительным прибором. Самое трудное – это присоединить к прибору раствор. Такое соединение можно сделать только при помощи металлического проводника, который служит для погружения в раствор. Но при соприкосновении с раствором на поверхности металла проводника образуется двойной электрический слой и появляется разность потенциалов.
Значит, при помощи измерительного прибора можно определить не потенциал одного электрода, а разность потенциалов между двумя электродами.
Электрод сравнения – это электрод, который применяется для определения электродного потенциала некоторого металла. В качестве
18
электродов сравнения выбирают электроды, потенциалы которых характеризуются хорошей стабильностью и воспроизводимостью.
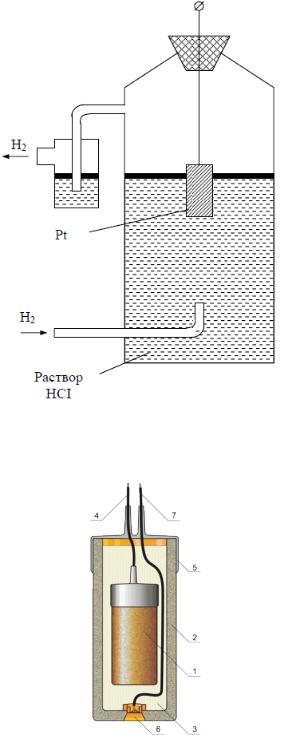
Поскольку электродные потенциалы металлов, измеренные относительно различных электродов сравнения, будут различны для расчетов электродных потенциалов был выбран электрод, потенциал которого условно принят равным нулю. В качестве такого электрода был выбран платиновый электрод, который погружен в раствор, содержащий ионы водорода,
омывается пузырьками газообразного водорода, продуваемого через раствор,
и адсорбирует на своей поверхности водород, образуя водородный мешок
(рисунок 3.1). Количество воды, содержание соляной кислоты и давление обтекающего его потока водорода должны иметь строгое значение.
Водородный электрод, электролит которого в расчете на 1000 г воды содержит 43,18 г соляной кислоты, а обтекающий его поток водорода имеет давление 1 кгс/см2 называется нормальным водородным электродом. Его электродный потенциал по соглашению принимается равным нулю.
Электродный потенциал металлов, измеренный относительно нормально водородного электрода сравнения называется нормальным, или
стандартным, потенциалом металла. Классический электрохимический ряд напряжения металлов построен на основании нормальных потенциалов металлов.
Наибольшее распространение помимо водородного электрода получили следующие электроды сравнения: каломельные, хлорсеребряные,
ртутносульфатные, ртутноокисные, хингидронные и другие.
В области трубопроводного транспорта для измерения защитных потенциалов трубопроводов относительно земли при катодной поляризации применяется медно-сульфатный электрод сравнения. Классическая схема медно-сульфатного электрода сравнения представляет собой медный
19
стержень внутри корпуса из диэлектрика, заполненного насыщенным раствором медного купороса CuSO4, который отделяется от грунта пористой перегородкой (ионообменной мембраной). Раствор медного купороса проса-
Рисунок 3.1 – Нормальный водородный электрод сравнения
Рисунок 3.2 – Медносульфатный электрод сравнения
20