Материал: Кузнецова Л.В., Бабаджан В.Д., Харченко Н.В. та ін. Імунологія

76 |
ІМУНОЛОГІЯ |
численню показника CD4/CD8 - імуно-регуляторного індексу або хел- перно-супресорного відношення (норма 1,8±0,4). Зменшення імуно-ре- гуляторного індексу спостерігається при вірусних інфекціях, у новонароджених і при пересадці кісткового мозку, а збільшення - при аутоімунних захворюваннях, алергії (табл. 11).
Таблиця 11 Клінічні приклади порушення імуно-регуляторного індексу
(хелперно-супресорного відношення, CD4/CD8)
Зменшення індексу |
Підвищення індексу |
|
|
СЧВ з ураженням нирок |
СЧВ без ураження нирок |
|
|
Гостра цитомегаловірусна інфекція |
Ревматоїдний артрит |
|
|
СНІД |
Діабет I типу (інсулінозалежний) |
|
|
Герпес |
Первинний біліарний цироз |
|
|
Інфекція вірусом Епштейн-Бар (інфекцій- |
Атопічний дерматит |
ний мононуклеоз) |
|
Інсоляція або тривала експозиція ультра- |
Хронічний аутоімунний гепатит |
фіолетовими промінями |
|
Новонародженість |
Псоріаз |
|
|
Стан після пересадки кісткового мозку |
|
|
|
В той же час, необхідно відмітити, що частина СD8+ Т-клітин є кілерами, а частина CD4+ - ефекторами, тому нині не існує єдиного досконалого способу оцінки числа лімфоцитів з супресорною або хелперною активністю. Крім того, антигенна структура Т-хелперів 1 і 2 типів практично ідентична. Ось чому оцінку чисельності субпопуляцій лімфоцитів бажано доповнювати функціональними тестами і визначенням спектру цитокінів.
Лазерна проточна цитофлюориметрія
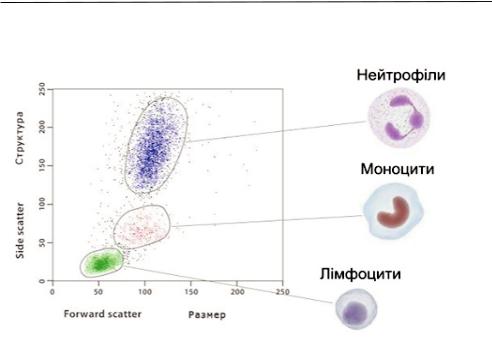
Принцип методу проточної цитометрії заснований на реєстрації світлорозсіювання і флюоресценції від кожної окремо взятої клітини в клітинній суспензії. На основі аналізу світорозсіювання (без застосування антитіл) в досліджуваному зразку можна визначити вміст лімфоцитів, моноцитів і гранулоцитів. Проточна цитометрія проводиться з використанням моноклональних антитіл, пов'язаних з флюоресцентними фарбниками, якими зафарбовують клітини крові. Моноклональні антитіла мають ідентичну специфічність до мембранних антигенів, тому вони згруповані і позначені відповідним номером кластера диференціювання (CD). Таким чином, використовуючи метод імунофлюоресценції (прямої

ІМУНОЛОГІЧНІ МЕТОДИ ДОСЛІДЖЕНЬ |
77 |
|
|
або непрямої), можна визначити чисельність різних субпопуляцій лімфоцитів.
Серед найчастіше вживаних флуорохромів знаходяться наступні: флуоресцеїн ізотіоционат (FITC), фікоеритрин (PE, RD1), перидінінх лорофіл протеїн (Per - CP), алофікоціанін (APC), а також тандемні барвники (фікоеритріни Cy5 і Cy7).
Суспензія клітин під тиском подається в проточний осередок, де за рахунок різниці тисків між зразком і оточуючою рідиною клітини, знаходячись в ламінарному потоці рідини, вишиковуються в ланцюжок один за одним (гідродинамічне фокусування струменя в струмені). Клітини крові поодинці перетинають сфокусований лазерний світловий промінь. Світло певної довжини порушує молекули флуоресціюючих фарбників, пов'язаних з різними клітинними компонентами, при цьому може відбуватися одночасне збудження декількох різних фарбників, що дозволяє оцінити відразу декілька клітинних параметрів.
У момент перетину клітиною лазерного променя детектори фіксують:
• пряме (малокутове) світлорозсіювання (forward scatter) (рис. 3). Детектор прямого світлорозсіювання розташовується по ходу лазерного променя за проточним осередком і реєструє випромінювання лазера, яке розсіюється під кутами 2-19°. Інтенсивність розсіяного під малим кутом світла пропорційна розміру клітини. Більші клітини розсіюють світло сильніше за дрібних;
Рис. 3. Лазерна проточна цитометрія. Пряме (малокутове) світлорозсіяння (forward scatter) (пояснення у тексті)
• бічне світлорозсіювання (side scatter) (рис. 4). Промінь лазера, проходячи крізь клітину, багаторазово заломлюється і розсіюється на всі боки під кутом 10° і більше. Реєстрація
цього випромінювання дозволяє оцінити внутрішню будову клітини (співвідношення ядро/цитоплазма, наявність гранул, інших внутрішньоклітинних включень). Комбінація бічного і прямого світлорозсіювання дозволяє судити про морфологію клітини в цілому, виділяти різні популяції клітин (лімфоцити, моноцити, гранулоцити) для подальшого аналізу;
78 |
ІМУНОЛОГІЯ |
Рис. 4. Лазерна проточна цитометрія. Бічне світлорозсіювання (side scatter) (пояснення у тексті)
• інтенсивність флуоресценції, яка дозволяє визначати субпопуляційний склад клітинної суспензії та ін.
Система для реєстрації світіння флюоресцентних міток складається з комплексу світлофільтрів і фотопомножувачів, кожен з яких реєструє випромінювання в діапазоні довжин хвиль, що відповідають флуорохрому. Вибір типу і кількості флюоресцентних барвників визначається поставленою задачею для цього дослідження. Основними типами таких барвників є моноклональні антитіла, кон’юговані з флюоресцентною міткою (FITC, PE, APC, PerCP та ін.) для визначення мембранних і цитоплазматичних антигенів клітини, барвники, що дозволяють оцінити життєздатність клітин (7AAD, PI) флуорофори, що зв'язуються з нуклеїновими кислотами (DAPI, Hoechst), pH -чутливі флуорофори (Fluo - 3), іон-залежні флуорофори (Indo-1). Наприклад, антигени CD 3 виявляються за допомогою моноклональних антитіл ОКТ 3, ОКТ 1, Leu 4, де ОК – Onto Klon); антигени CD 4 - ОКТ 4 та Leu 2а; антигены СD 8 - ОКТ 8 та Leu 3a; антигени CD 2 - ОКТ 11. Моноклональні антитіла ОКТ 6 виявляють антигени CD 1, ОКТ 9 та ОКТ 10 - на претимічних клітинах, на незрілих та активованих Т-лімфоцитах, моноклональні антитіла ОКВ 1 та Leu 12 – на зрілих В-лімфоцитах, ОКВ 2 – на молодих формах В-
ІМУНОЛОГІЧНІ МЕТОДИ ДОСЛІДЖЕНЬ |
79 |
|
|
лімфоцитів, ОКМ 1 та Leu 7 – на моноцитах, гранулоцитах, натуральних кілерах.
Отриманий сигнал передається в комп'ютер, обробляється, і отримані дані відображуються у вигляді різних графіків і гістограм.
У проточному цитометрі, обладнаному системою для сортування клітин, проточний осередок закріплений на п'єзокристалі. При подачі на нього напруги кристал разом з осередком здійснює коливання із заданою частотою, внаслідок чого струмінь рідини з клітинами розбивається на окремі краплі. Проходячи крізь заряджаюче кільце, крапля може придбавати позитивний або негативний заряд залежно від того, яка клітина міститься усередині краплі. Пролітаючи повз пластини, що відхиляють, крапля з клітиною притягується до них, виходить з основного потоку і потрапляє в пробірку. Метод сортування клітин на проточному цитометрі дозволяє отримати популяції клітин з високою чистотою (до 99.9% позитивних клітин) у відсортованій фракції.
Метод розеткоутворення. Визначення Т-лімфоцитів методом спонтанного розеткоутворення з еритроцитами барана (Е-РУК). Тимусзалежні Т-лімфоцити мають рецептори для еритроцитів барана (Е-рецептори ідентичні CD2, що виявляється моноклональними антитілами), які виступають специфічним маркером для їх розпізнавання (Е-РУК: Erythrocyte - розеткоутворюючі клітини).
Хід виконання дослідження. В пластикові пробірки (від 2 до 5) вносять 0,1 мл суспензії лімфоцитів і додають рівний об'єм 0,5% суспензії еритроцитів барана. Співвідношення еритроцити:лімфоцити не повинне перевищувати 50:1. Інкубують суміш в термостаті 37°С впродовж 10 хв. Потім проби центрифугують 5 хв. при 1000 об/хв.. і залишають на ніч в холодильнику при температурі 4°С. Підрахунок клітин проводять в камері Горяєва. Суспензію клітин фіксують глютаровим альдегідом або ацетальдегідом з наступним приготуванням мазків і прорахунком розеток в забарвлених препаратах, що дозволяє накопичувати скло і аналізувати результати реакцій в будь-який інший день.
Для прорахунку клітин в камері Горяєва осад клітин у витягнутих з холодильника пробірках обережно ресуспендують пастерівською піпеткою (кілька разів повільно набирають і випускають клітинну суспензію) і додають 0,02 мл 0,01 % розчину у фосфатному буфері акридінового помаранчевого. Цей барвник дає яскраво-зелену люмінесценцію при збудженні ультрафіолетом. Через 2-3 хв. заповнюють камеру Горяєва і визначають відсоток Е-РУК шляхом підрахунку 300 лімфоцитів в люмінесцентному мікроскопі.

80 |
ІМУНОЛОГІЯ |
В день узяття крові на Т-лімфоцити необхідно проводити загальний аналіз крові, який дає можливість вираховувати абсолютні значення Т- клітин.
Нормальні величини Т-клітин у здорових донорів: 54,3+0,98 %; 979,8+16,8 кл/мкл.
Визначення активних Т-лімфоцитів, що утворюють розетки з еритроцитами барана (ЕА-РУК). Усі підготовчі операції виконують так, як це описано для Е-РУК, за винятком сироватки, яку при визначенні ЕА-РУК не додають в інкубаційне середовище, і тривалої холодової інкубації. Після термостатування 10 хв. при 37°С і наступного центрифугування при 1000 об/хв. впродовж 5 хв. проводять підрахунок Т-активних лімфоцитів способом, описаним вище.
Вміст Т-активних лімфоцитів у здорових донорів складає: 34,6+1,92 %, 840+123 кл/мл
Визначення теофілинчутливих Т-клітин. У присутності теофіліну Т-лімфоцити з супресорною функцією втрачають здатність до Е-розет- коутворення. Такі клітини дістали назву теофілінчутливих (ТЧ), аналог CD8 Т-супресорів. Так звані теофілінрезистентні (ТР) клітини в значному відсотку випадків містять субпопуляцію CD4 Т-хелперів. Показник ТР/ТЧ в нормі складає 2,5-3,5.
Хід виконання дослідження. Реактиви і устаткування, використовували були аналогічні для описаного вище методу визначення Т-активних лімфоцитів. Перед постановкою методу готують 0,3 М розчин теофіліну на дистильованій воді, підігрітій до 60°С. Охолоджений до кімнатної температури розчин теофіліну додають в інкубаційне середовище (без додавання сироватки), термостатують, центрифугують при 1000 об/хв. впродовж 5 хв. і прораховують клітини так само, як і Т-активні. Виявляють 2 субпопуляції: теофілінчутливі Т-клітини, тобто лімфоцити, що втратили здатність до розеткоутворення під впливом обробки теофіліном,
ітеофілінрезистентні Т-клітини.
Уздорових донорів співвідношення теофілін-чутливих і стійких Т- клітин складає 1:3.
Виявлення Т-лімфоцитів, що утворюють розетки з алогенними і
аутологічними еритроцитами. Т-клітини, що утворюють розетки з аутоеритроцитами, як вважають, несуть кілерну функцію і грають основну роль в механізмах аутоагресії.
Хід виконання дослідження. Суспензію лімфоцитів виділяють вже описаним вище методом. Еритроцити людини: необхідно використову-