Материал: кафедральные лекции
активность и в дальнейшем либо выводится из организма (например через почки), либо подвергается разрушению клетками или неклеточными факторами иммунитета.
Есть несколько классов иммуноглобулинов: Ig G, M, A, E, D.
Иммуноглобулины класса G составляют около 75% всех Ig сыворотки крови и имеют наибольшее значение. Они имеют мономерное строение, нейтрализуют бактериальные токсины и вирусы. В иммунных реакциях вырабатываются позже других антител, при вторичном иммунном ответе преобладают. Активируют систему комплемента, макрофаги и нейтрофилы.
IgG – единственный класс иммуноглобулинов, способный проникать через плацентарный барьер и участвовать в естественном пассивном иммунитете.
Иммуноглобулины класса М составляют около 10% всех Ig сыворотки крови. Состоят из пяти связанных между собой молекул Ig, являясь пентамерами. Они менее специфичны к антигенам, но более эффективны, чем IgG, при нейтрализации токсинов, активации комплемента, лизисе чужеродных клеток. Являются основными антителами, вырабатываемыми на ранних стадиях первичного иммунного ответа. Мономеры IgM являются рецепторами В- лимфоцитов.
Иммуноглобулины класса А содержатся в биологических жидкостях: сыворотке крови, секретах экзокринных желез (слюне, слезе, слизи), моче и т.д. Различают сывороточные и секреторные Ig А.
Сывороточный Ig А1 (10% всех Ig крови) может существовать в димерной, тримерной и тетрамерной формах, причем преобладает димерная форма.
Секреторный IgA2 вырабатывается плазматическими клетками лимфоидных фолликулов миндалины, аппендикса, пейеровых бляшек и пр. для защиты слизистых оболочек, препятствуя прикреплению микроорганизмов к поверхности эпителия, а также играет роль опсонина: покрывая поверхность микроорганизмов, резко стимулирует их фагоцитоз.
Иммуноглобулины класса Е участвуют в аллергических реакциях. Они вырабатываются в основном плазмоцитами слизистых оболочек воздухоносного и пищеварительного трактов, в крови присутствуют в крайне незначительных количествах (0,004%). Комплекс «антиген - антитело класса E» присоединяется к поверхности тучных клеток и вызывает выделение ими гистамина, что приводит к отеку и сдавлению сосудов, уменьшая тем самым концентрацию антигена в тканях и препятствуя его распространению.
Иммуноглобулины класса D составляют 1% всех Ig и выявляются в крови, секрете бронхов, молоке, спинномозговой жидкости. Их количество может увеличиваться при некоторых вирусных инфекциях. Функции IgD до конца не изучены. Известно, что они являются рецепторами В-лимфоцитов и играют важную роль в процессах дифференцировки этих клеток. Установлено, что IgD могут фиксировать комплемент и что они часто направлены против антигенов, длительно циркулирующих в крови.
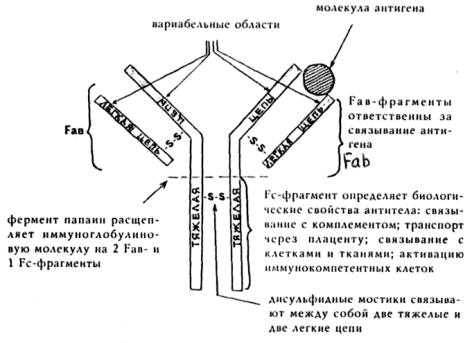
Для понимания механизма действия антител необходимо рассмотреть их структуру (см. рис.3). Молекула антитела напоминает букву Y и состоит из двух тяжелых и двух легких цепей, связанных между собой дисульфидными мостиками. И тяжелые, и легкие цепи идентичны и симметрично расположены. Фермент папаин расщепляет молекулу антитела на два одинаковых Fab-фрагмента (fragment, antigen binding, сокращенно Fab) и Fc-
фрагмент (fragment crystallizable).
Рис. 3.
С помощью Fab-фрагментов антитела формируют активные центры, способные связываться с антигенами. Fcфрагменты не связывают антигены, но определяют ряд биологических свойств антител: способность к связыванию
71
комплемента, транспорту через плаценту, связыванию с иммунокомпетентными и неиммунными клетками, различными тканями. Структурное разнообразие антител определяется прежде всего последовательностью аминокислот в вариабельных областях тяжелых и легких цепей.
Механизмы действия антител.
1.Связывание антигена Fab-фрагментами антитела исключает его действие на клетки, т.к. антитело закрывает активные, цитотоксические центры антигена. Образованный комплекс антиген-антитело в последующем выделяется с мочой, потом, слюной и т.д.
2.Комплекс антиген-антитело при помощи Fc-фрагмента активирует макрофаги, моноциты и гранулоциты, которые включаются в элиминацию антигена путем фагоцитоза.
3.Покрывая поверхность чужеродной клетки, антитела класса G активируют Fc-фрагментами NK-клетки (натуральные киллеры), осуществляющие антителозависимый лизис чужих клеток.
4.Комплекс антиген-антитело при помощи Fc-фрагмента активирует систему комплемента. Эта система включает ряд белков крови, которые составляют 10% всех глобулинов крови. Данные белки, отличаясь от иммуноглобулинов, дополняют их в защитных реакциях. Активация системы комплемента имеет три важных следствия для защиты организма:
а) белки комплемента, действуя по принципу перфоринов, встраиваются в цитолемму чужеродной клетки и образуют в ней сквозные каналы, в результате клетка погибает от осмотического шока;
б) компоненты комплемента активируют макрофаги, которые далее принимают участие в уничтожении антигена путем фагоцитоза;
в) белки комплемента вызывают местную воспалительную реакцию, что ведет к активации нейтрофильных лейкоцитов.
5.Иммуноглобулины класса Е способны вызывать защитные реакции через систему тучных клеток. В комплексе с антигеном они адсорбируются на поверхности этих клеток и вызывают высвобождение гранул с гистамином. Гистамин вызывает расширение сосудов и отек, что уменьшает концентрацию антигена и препятствует его распространению в организме. Одновременно гистамин вызывает сокращение гладких мышц полых органов, что иногда ведет к механическому удалению антигена (например паразита) из организма.
6.Антитела обладают собственной медленной ферментативной активностью (абзимная активность) и могут расщеплять некоторые субстраты, в том числе и антигенного характера.
Клетки иммунной системы
В иммунном ответе участвует целый ряд клеток и выделяемых ими растворимых продуктов. Центральная роль всегда принадлежит лейкоцитам, однако другие клетки (например тканевые) также вносят свой вклад, посылая сигналы лимфоцитам и отвечая на цитокины, выделяемые Т-клетками и макрофагами. К иммунокомпетентным клеткам относятся Т- и В-лимфоциты, макрофаги, тучные клетки (тканевые базофилы), гранулоциты, NK-клетки. По функции все эти клетки делятся на несколько групп: антигенпредставляющие клетки, эффекторные клетки, регуляторные клетки, вспомогательные клетки, клетки иммунологической памяти.
Антигенпредставляющие клетки (АПК) – передают информацию об антигене Т- и В-лимфоцитам. Они сосредоточены на главных путях поступления антигена в организм: в эпидермисе и дерме кожи, в эпителии и собственной пластинке слизистых оболочек, а также в периферических органах иммунной системы. К антигенпредставляющим клеткам относятся:
- макрофаги и моноциты, - интердигитирующие клетки (ИДК),
- фолликулярные дендритные клетки (ФДК) лимфоидных фолликулов, - некоторые субпопуляции В-лимфоцитов, - М-клетки эпителия пейеровых бляшек.
Макрофаги образуются путем дифференцировки из моноцитов крови. Эта дифференцировка происходит в тканях и сопровождается увеличением размеров клетки до 25–50 мкм, приобретением ядра бобовидной формы, накоплением лизосом, митохондрий, канальцев эндоплазматической сети, гипертрофией комплекса Гольджи, нарастанием количества пиноцитозных пузырьков. Резко усложняется поверхность макрофага за счет увеличения количества микроворсинок и складок. Возрастает подвижность, способность к пиноцитозу и фагоцитозу, бактерицидная активность, растет активность лизосомальных ферментов, а также ферментов энергетического обмена. Ферменты лизосом осуществляют обработку антигена и его разрушение до мелких высокоиммунных комплексов, которые связываются с молекулами МНС 2-го класса и выходят на поверхность клетки для последующего контакта с Т- и В-лимфоцитами.
Обработка антигена и передача его лимфоцитам – самая важная функция макрофагов. Кроме того, он выполняет и ряд других функций.
- секреторную функцию – секретирует бактерицидные вещества, ряд ферментов, оказывающих бактерицидное действие, интерфероны, участвующие в противовирусном иммунитете; компоненты комплемента; факторы, стимулирующие размножение лимфоцитов (ИЛ-1), клеток предшественниц миелопоэза, фибробластов; тромбоцитарный фактор роста. Макрофаги выделяют и вещества, подавляющие деление лимфоцитов, опухолевых клеток (фактор некроза опухолей) и стимулирующие их апоптоз. Из других синтезируемых макрофагами факторов следует назвать простагландины и лейкотриены, свободные радикалы кислорода, перекись водорода, оксид азота, катионные белки. Эти вещества либо обладают бактерицидным и цитоцидным действием, либо участвуют в воспалительных реакциях;
72
-функцию фагоцитоза – может фагоцитировать и разрушать антиген до простых соединений – воды и углекислого газа. Он фагоцитирует и крупные частицы, не являющиеся антигенами, например частицы угля, пыли. Накопление в цитоплазме макрофага этих инертных веществ подавляет его фагоцитарную активность и другие
иммунные функции.
Клетки Лангерганса эпидермиса и многослойных эпителиев – разновидность тканевых макрофагов, которые развиваются из моноцитов крови и составляют примерно 3–5% всех кератиноцитов (эпителиоцитов). Они относятся к системе мононуклеарных фагоцитов, локализуются преимущественно в шиповатом слое, а иногда – в базальном, встречаются и в дерме. В их цитоплазме имеются развитые органеллы белкового синтеза, лизосомы, а также специфические гранулы Бирбека в виде теннисной ракетки. Предполагают, что эти гранулы участвуют в транспорте антигена. Эти клетки несут на своей поверхности белки МНС 1-го и 2-го классов в комплексе с антигеном, играют роль антигенпредставляющих клеток в многослойных эпителиях, дерме и собственной пластинке слизистых оболочек, могут мигрировать в регионарные лимфоузлы, превращаясь там в интердигитирующие клетки.
Интердигитирующие клетки (ИДК) также являются разновидностью макрофагов. Располагаются в Т-зависимых зонах периферических органов иммунитета: паракортикальной зоне лимфоузлов, в периартериальных муфтах селезенки, в интерфолликулярных зонах лимфоидных скоплений (пейеровых бляшек, миндалин, аппендикса). Считается, что интердигитирующие клетки (ИДК) образуются из клеток Лангерганса эпидермиса и других эпителиев, мигрирующих в лимфоузел. В процессе миграции происходит изменение фенотипических черт клеток: ИДК приобретают длинные отростки, которые контактируют с большим числом Т-лимфоцитов. ИДК способны перерабатывать антиген, выделять его на свою поверхность, а затем представлять Т-лимфоцитам. Поскольку антиген на поверхности ИДК может сохраняться долгое время и в результате контакта с ним постоянно вырабатывается какое-то количество эффекторных Т-лимфоцитов, способных уничтожать антиген, при повторном попадании антигена в организм иммунная реакция идет значительно быстрее. Таким образом, ИДК участвуют в обеспечении феномена иммунной памяти. Интердигитирующие клетки обладают выраженной способностью к пиноцитозу, однако у них снижена способность к фагоцитозу и довольно слабая активность лизосомальных ферментов.
Фолликулярные дендритные клетки (ФДК) располагаются в В-зависимых зонах периферических органов иммунитета (в лимфоидных фолликулах), имеют длинные отростки, контактирующие с большим числом В- лимфоцитов. Способны удерживать на своей поверхности иммунные комплексы (антиген в комплексе с антителами), передавать их В-лимфоцитам и таким образом играть роль антигенпредставляющих клеток и клеток памяти по отношению к В-лимфоцитам.
В последнее время некоторые авторы (В.Л. Быков, 1998, и др.) считают, что ведущую роль в представлении антигена играют специализированные дендритные клетки, тогда как у прочих макрофагов эта способность существенно ниже. Вместе с тем, у образующихся из макрофагов дендритных клеток по сравнению с моноцитами и макрофагами значительно снижена фагоцитарная и бактерицидная активность. В группу дендритных АПК эти авторы включают функционально единые морфологически похожие клетки, распределенные по всему организму, но в наибольшем количестве встречающиеся в коже, слизистых оболочках и органах иммунной системы. Сюда относятся клетки Лангерганса, дендритные клетки рыхлой соединительной ткани, Т- и В-зависимых зон периферических лимфоидных органов (интердигитирующие клетки отдельно не выделяются) и др.
B-лимфоциты. В последнее время установлено, что передачу антигена в комплексе с Ia-антигеном Т-хелперам могут осуществлять В-лимфоциты. При этом антиген, попавший на рецепторы В-лимфоцита, поглощается путем рецепторноопосредованного эндоцитоза. Далее он подвергается процессингу и выделяется на поверхность В- лимфоцита в комплексе с молекулами МНС 2-го класса.
М-клетки (мембранозные клетки) находятся в эпителии купола пейеровых бляшек, составляя до 10% всех клеток эпителия купола. Они имеют на поверхности немногочисленные микроворсинки со слабовыраженным гликокаликсом, а на базальной поверхности глубокие инвагинации цитолеммы. В этих инвагинациях содержится большое количество интраэпителиальных лимфоцитов. М-клетки первыми контактируют с антигенами в просвете кишки, захватывают их и затем без лизосомального протеолиза передают макрофагам и лимфоцитам. Стимулированные антигенами лимфоциты мигрируют в регионарные лимфоузлы, подвергаются там бласттрансформации, делению и дифференцировке. После этого они поступают в кровь и с ее током возвращаются в собственную пластинку бляшек, где превращаются в плазмоциты, образующие секреторные антитела класса А2.
Лимфоциты – основные клетки иммунных реакций, делятся на Т- и В-клетки.
Т-лимфоциты дифференцируются из стволовых клеток крови в тимусе под влиянием тимусных гормонов тимозина, тималина, тимопоэтина. Это антигеннезависимый Т-лимфоцитопоэз. В ходе его на Т-лимфоцитах (тимоцитах) появляются специфические Т-клеточные рецепторы (ТCR) и дифференцировочные рецепторы CD3, CD4, CD8. Такие клетки, несущие одновременно антигены Т-хелперов (CD4) и Т-супрессоров (CD8), называются двойными позитивными Т-клетками. При контакте тимоцитов со специальными эпителиальными клетками коркового вещества тимуса 95% их подвергается разрушению путем апоптоза. Это аутоагрессивные Т-лимфоциты, способные реагировать на собственные антигены организма. Оставшиеся Т-лимфоциты утрачивают либо рецепторы СD4, либо CD8. Из тимуса Т-лимфоциты поступают во вторичные (периферические) лимфоидные органы, где под влиянием антигена дифференцируются в следующие субпопуляции T-лимфоцитов: Т-лимфоциты памяти, Т- хелперы/индукторы, Т-супрессоры/цитотоксические. Функцию этих субпопуляций Т-клеток рассмотрим несколько ниже.
Зрелые Т-лимфоциты несут на своей поверхности ряд рецепторов: ТCR, рецепторы для распознавания антигенов, для Fc-фрагмента антител, для митогенов (веществ, стимулирующих митоз), гормонов. Т-лимфоциты имеют специфический набор CD-антигенов: CD2, СD3, CD4, CD5, CD6, CD7, CD8 и др.
В-лимфоциты у человека дифференцируются в красном костном мозге из стволовых клеток крови. У птиц этот процесс происходит в сумке Фабрициуса. В указанных органах осуществляется антигеннезависимый В-
73
лимфоцитопоэз, а после этого В-лимфоциты поступают в В-зависимые зоны периферических органов иммунитета, где под влиянием антигена происходит антигензависимая дифференцировка с превращением В-лимфоцитов в плазмоциты, В-лимфоциты памяти и В-супрессоры.
В-лимфоциты несут на своей поверхности ряд рецепторов: для Fc-фрагментов антител, для антигенов, С3компонента комплемента, митогенов, гормонов. Они экспрессируют на своей поверхности молекулы МНС обоих классов, а также CD19, CD20, CD21, CD22, CD23. Основной функцией В-лимфоцитов является продукция иммуноглобулинов (резко возрастающая после дифференцировки В-лимфоцитов в плазматические клетки). Кроме того, В-лимфоциты могут супрессировать иммунные реакции, участвовать в распознавании и презентации антигенов, оказывать цитотоксическое действие на клетки-мишени, покрытые антителами, вырабатывать разнообразные медиаторы.
Эффекторные клетки иммунной системы
Все иммунные реакции условно делятся на два вида: реакции клеточного и гуморального иммунитета.
Реакции клеточного иммунитета направлены против чужеродных клеток или собственных клеток, зараженных вирусами, бактериями, патогенными грибами, а также против раковых клеток. Эти реакции осуществляются иммунокомпетентными цитотоксическими клетками (Т-киллерами).
После распознавания антигена в комплексе с молекулами МНС 1-го класса происходит активация Т- супрессоров/цитотоксических лимфоцитов и превращение их в Т-киллеры. При этом разрушение клетки-мишени может происходить несколькими путями.
1.Цитоплазматические гранулы Т-киллеров, содержащие белки перфорины, перемещаются в зону контакта, перфорины выходят из Т-лимфоцита и встраиваются в цитолемму клетки-мишени, формируя трансмембранные поры. Это вызывает осмотический лизис клетки-мишени. Возможно разрушение клетки-мишени и на расстоянии при помощи растворимых перфоринов, выделяемых Т-киллерами.
2.Индукция апоптоза клетки-мишени ферментами Т-киллера. К таким ферментам относятся гранзимы (сериновые протеазы). Проникнув через перфориновые поры в цитоплазму клеток-мишеней, гранзимы запускают в них программу апоптоза.
3.Рецепторноопосредованная индукция апоптоза клеток-мишеней. Она происходит с участием эндогенных протеолитических ферментов, однако механизмы передачи сигнала с поверхности клетки на систему протеолитических ферментов пока неизвестны.
Реакции гуморального иммунитета направлены против мелкодисперсных антигенов, находящихся в жидкостях (крови, лимфе, слизи и т.д.). Уничтожение антигенов в реакциях гуморального иммунитета идет при помощи высокомолекулярных веществ – антител.
В гуморальном иммунитете основными эффекторными клетками являются плазматические клетки (плазмоциты). Они образуются из В-лимфоцитов после стимуляции последних антигеном и Т-хелпером/индуктором. В процессе дифференцировки плазмоцитов в них накапливается гранулярная эндоплазматическая сеть, гипертрофируется комплекс Гольджи. Плазмоциты являются основными продуцентами антител, способных связывать и инактивировать антиген, однако кроме них в незначительном количестве синтез антител могут осуществлять и В- лимфоциты.
К эффекторным клеткам можно отнести также натуральные киллеры (NКклетки). NK-клетки – это большие зернистые лимфоциты (БЗЛ), содержащие в цитоплазме характерные электронноплотные гранулы, вещество которых обладает выраженной цитотоксичностыо. NK-клеткам приписывают следующие функции:
-контроль роста опухолей;
-контроль микробных инфекций;
-иммунорегуляция путем:
а) продукции медиаторов иммунных реакций; б) контроля над пролиферацией и дифференцировкой гемопоэтических клеток; в) инициации трансплантационного иммунитета;
г) модуляции ряда заболеваний, в том числе и иммунных.
Однако главной функцией NK-клеток принято считать их участие в противоопухолевом иммунитете. Они узнают определенные гликопротеидные структуры на мембране клеток, инфицированных вирусом, благодаря чему отличают такие клетки от нормальных и выделяют содержимое своих гранул: перфорин или цитолизин, сходный с С9 компонентом комплемента. Подобно С9, перфорин встраивается в мембрану клетки-мишени и образует трансмембранную пору, в результате чего клетка гибнет от осмотического шока. Перфоринопосредованный механизм разрушения клеток-мишеней является основным, однако полагают, что возможны также и другие механизмы лизиса, свойственные Т-киллерам. В последнее время установлено, что NK-клетки могут проявлять и антителозависимую клеточную цитотоксичностъ.
NK-клетки развиваются из костно-мозгового предшественника, отличного от предшественников Т- и В- лимфоцитов. Допускается также их образование в тимусе. Полагают, что и печень принимает активное участие в генезе NК-клеток, причем некоторые авторы считают ее центральным органом NK-цитогенеза.
Регуляторные клетки иммунных реакций
К ним относятся Т-хелперы/индукторы (Тх), Т-супрессоры/цитотоксические, В-супрессоры. Регулировать иммунные реакции могут также моноциты, макрофаги, гранулоциты, тучные клетки. Т-хелперы/индукторы несут на своей поверхности специфические антигены Т-лимфоцитов, а также CD4.
Т-хелперы/индукторы подразделяются на Тх1 и Тх2.
Tx1 в основном участвуют в реакциях клеточного иммунитета, хотя могут включаться и в некоторые реакции гуморального иммунитета. Они секретируют ИЛ-2, а также интерферон и фактор некроза опухоли. ИЛ-2 в
74
клеточном иммунитете стимулирует бласттрансформацию Т-лимфоцитов и превращение их в Tx1, Т- супрессоры/цитотоксические, Т-клетки памяти. Он также активирует NK-клетки.
Тх2 в основном задействованы в гуморальном иммунитете, они стимулируют бласттрансформацию В- лимфоцитов и превращение их в плазмоциты путем выработки ИЛ-4, -5, -6, -9, -10, -13. Т-хелперы стимулируются антигеном и ИЛ-1 макрофагов и других АПК. Tx1 и Тх2 развиваются из общего предшественника Тх0. Направление дифференцировки Тх0 зависит от типа антигена, способа его проникновения, генетической предрасположенности индивидуума. Т-хелперы повреждаются ВИЧ, поскольку этот вирус размножается именно в этих клетках и индуцирует апоптоз Т-хелперов. В результате в условиях резкого дефицита Тх иммунные реакции выраженно подавляются, и организм оказывается совершенно беззащитным но отношению к инфекционным агентам.
Т-супрессоры/цитотоксические угнетают иммунные реакции. Они несут на своей поверхности специфические рецепторы Т-лимфоцитов и CD8. Эти клетки путем непосредственного контакта или за счет своих растворимых медиаторов подавляют функции Т-киллеров, Т-хелперов и макрофагов. Т-супрессоры угнетают развитие аутоиммунных процессов. Их содержание нарастает с возрастом. Соотношение в крови Т-хелперов/индукторов (CD4+) и Т-супрессоров/цитотоксических (CD8+) составляет 1:2–3. Снижение этого показателя может свидетельствовать о развитии иммунодефицита, определение его используется для диагностики СПИДа.
Некоторые субпопуляции В-лимфоцитов также могут подавлять бласттрансформацию лимфоцитов и называются В-супрессорами.
Клетки иммунологической памяти. Иммунологическая память – это память об антигене после первого его попадания в организм. При повторном попадании антигена его уничтожение идет быстрее. К клеткам памяти относятся: Т- и В-лимфоциты памяти (долгоживущие кортизонрезистентные лимфоциты), интердигитирующие клетки и фолликулярные дендритные клетки.
Вспомогательные клетки иммуногенеза.
К ним относятся гранулоциты, тучные клетки (тканевые базофилы), натуральные киллеры (NK-клетки). Нейтрофильные гранулоциты также выполняют ряд функций в иммунных реакциях:
-фагоцитируют антигены, главным образом микроорганизмы;
-контролируют действие вазоактивных медиаторов и комплемента;
-вырабатывают интерферон, вызывающий гибель вирусов;
-регулируют дифференцировку В-лимфоцитов в плазмоциты и выработку антител;
-регулируют функции Т-супрессоров и Т-хелперов;
-регулируют пролиферацию тимоцитов и функции макрофагов. Эозинофильные гранулоциты выполняют следующие иммунные функции:
-фагоцитоз,
-активация макрофагов,
-разрушение комплекса антиген-антитело,
-участие в противоаллергических реакциях,
-выделение ряда медиаторов воспаления и цитокинов,
-участие в противогельминтной защите: эозинофилы выделяют белок, который поражает мембраны клеток паразита и его ДНК.
Базофильные гранулоциты и тучные клетки выполняют в иммунных реакциях сходные функции:
-выделяют ряд медиаторов иммунных реакций;
-инактивируют комплекс антиген – антитело, участвуя в аллергических реакциях;
-под действием комплекса антиген – антитело выделяют гистамин, серотонин, гепарин, которые модулируют иммунные реакции и вызывают отек тканей в месте попадания в организм антигена.
Медиаторы иммунитета
Вразвитии иммунного ответа участвует целый ряд молекул-посредников, в том числе выделяемые лимфоцитами антитела и цитокины, а также различные белки сыворотки, обычно содержащиеся в ней в низкой концентрации.
Белки системы комплемента – около двух десятков сывороточных белков, общая функция которых состоит в регуляции воспаления. Они служат медиаторами фагоцитоза, регулируют воспалительную реакцию, взаимодействуют между собой и с другими элементами иммунной системы. Активация комплемента – это каскад реакций, в котором каждый предшествующий компонент действует на последующий (подобно тому, как это происходит при свертывании крови), что в итоге приводит к образованию белков или пептидных фрагментов, вызывающих следующие эффекты:
-опсонизация микроорганизмов с последующим поглощением и внутриклеточным разрушением их фагоцитами;
-привлечение фагоцитов к месту воспаления (хемотаксис);
-усиление тока крови в месте активации и повышение проницаемости капилляров для компонентов плазмы;
-повреждение собственных клеток организмов, грамотрицательных бактерий и вирусов или других микробов, вызвавших активацию комплемента; лизис возбудителя вследствие такого повреждения обеспечивает прекращение инфекции;
-дополнительное выделение медиаторов воспаления из тучных клеток.
Цитокины – разнообразные белки, осуществляющие передачу сигналов между лимфоцитами, фагоцитами и
другими клетками организма. Цитокины подразделяют на несколько групп. Так, цитокины, выделяемые лимфоцитами, часто называют лимфокинами. К цитокинам относят также:
Интерфероны (ИФ) – эти цитокины особенно важны в сдерживании некоторых вирусных инфекций. Две группы интерферонов (ИФα и ИФβ) синтезируют клетки, инфицированные вирусами. Третий тип интерферона (ИФγ) выделяют некоторые активированные Т-клетки. Интерфероны сообщают противовирусную устойчивость еще не
75