Материал: Изучение реакций взаимодействия ди(метилтио)нитримина с гидроксидом натрия и гидроксидом калия
Наличие непрореагировавшего S-метилтио-N-нитрокарбамата после окончания реакции свидетельствует о вовлечении гидразина в побочные реакции, поэтому при получении гидразиниевой соли 4-нитросемикарбазида необходимо брать небольшой избыток гидразина, при этом само полученное соединение не взаимодействует с гидразином-гидратом.
При взаимодействии гидразина-гидрата с натриевой солью S-метилтио-N-нитрокарбамата была получена натриевая соль 4-нитросемикарбазида, которая в УФ-спектре имеет пики с максимумами при длинах волн 255,5 нм и 209,0 нм и интенсивностями 0,723 и 0,529, соответственно. Продукт очень хорошо растворим в воде, в большей своей массе нерастворим в ацетоне, малорастворим в этаноле (при этом в этаноле растворимы окрашивающие продукт примеси).
При взаимодействии гидразина-гидрата с калиевой солью S-метилтио-N-нитрокарбамата была получена калиевая соль 4-нитросемикарбазида, которая в УФ-спектре имеет пики с максимумами при длинах волн 255,5 нм и 209,0 нм и интенсивностями 0,764 и 0,543, соответственно (при mнавески = 8,3 мг и С=1,05·10-4 моль/л).
Результаты УФ-спектроскопического исследования солей 4-нитросемикарбазида представлены в таблице 3.2.
Графики их УФ-спектров представлены на рисунках 3.7-3.9.
Таблица 3.2 - УФ-спектры солей 4-нитросемикарбазида
|
Вещество |
mнавески, мг на Vколбы=500 мл |
Пики максимумов поглощения, длина волны, нм (интенсивность) |
|
Гидразиниевая соль |
7,6 |
207,5 (0,668); 256,0 (0,810), |
|
Натриевая соль |
7,1 |
209,0 (0,529); 255,5 (0,723) |
|
Калиевая соль |
8,3 |
209,0 (0,543); 255,5 (0,764) |
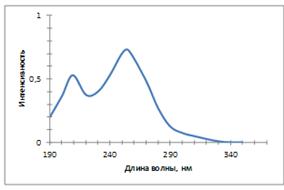
Рисунок 3.7 - УФ-спектр натриевой соли 4-нитросемикарбазида
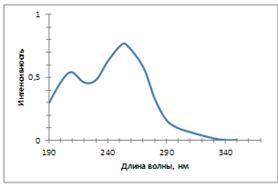
Рисунок 3.8 - УФ-спектр калиевой соли 4-нитросемикарбазида
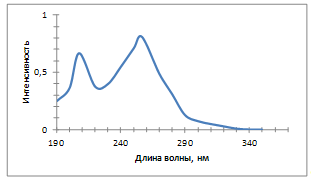
Рисунок 3.9 - УФ-спектр гидразиниевой соли 4-нитросемикарбазида
Данные ИК спектроскопии:
На рисунке 3.10 представлен график сравнения ИК-спектров калиевой соли
4-нитросемикарбазида с 1-амино-2-нитрогуанидином и калиевой солью
нитромочевины.
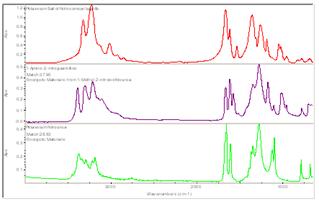
Рисунок 3.10 - График сравнения ИК-спектров калиевой соли
4-нитросемикарбазида с 1-амино-2-нитрогуанидином и калиевой солью
нитромочевины.
Как видно из графика, у калиевой соли 4-нитросемикарбазида, 1-амино-2-нитрогуанидина и калиевой соли нитромочевины схоже проявляются NO2 -группы, карбонильные группы и гидразиниевые фрагменты у соответствующих молекул.
На рисунке 3.11 представлен график сравнения ИК-спектров калиевой, натриевой и гидразиниевой солей 4-нитросемикарбазида.
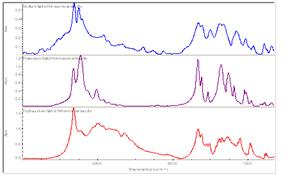
Рисунок 3.11 - График сравнения ИК-спектров калиевой, натриевой и
гидразиниевой солей 4-нитросемикарбазида.
Элементный анализ гидразиниевой соли 4-нитросемикарбазида:
|
Найдено: |
|
Вычислено: |
|
N, %: 55,62 |
|
N, %: 55,25 |
|
C, %: 8,27 |
|
C, %: 7,90 |
|
H, %: 5,11 |
|
H, %: 5,30 |
Элементный анализ натриевой соли 4-нитросемикарбазида:
|
Найдено: Вычислено: |
|
|
|
N, %: 38,44 |
|
N, %: 39,44 |
|
C, %: 8,78 |
|
C, %: 8,46 |
|
H, %: 2,35 |
|
H, %: 2,13 |
Элементный анализ калиевой соли 4-нитросемикарбазида:
|
Найдено: Вычислено: |
|
|
|
N, %: 35,48 |
|
N, %: 35,42 |
|
C, %: 7,38 |
|
C, %: 7,59 |
|
H, %: 1,86 |
|
H, %: 1,91 |
Как видно из данных элементного анализа экспериментальные данные хорошо
соответствуют расчетным.
.4.1 Температуры плавления полученных солей 4-нитросемикарбазида
. Гидразиниевая соль 4-нитросемикарбазида имеет температуру плавления 140-142°C, она плавится с разложением и большим выделением газа (вспениванием).
. Натриевая соль 4-нитросемикарбазида разлагается с газовыделением и последующей вспышкой при 160°C, объем при этом увеличивается в три раза. Температура разложения равна 150°С.
. Калиевая соль 4-нитросемикарбазида вспыхивает при 144°C, разложение сразу переходит во вспышку, поэтому температуры разложения нет. Продукт имеет температуру плавления 162°С.
Гидразиниевая соль 4-нитросемикарбазида на плитке закипает и разлагается без вспышки, а калиевая и натриевая соли разлагаются со вспышкой. Судя по тому, что у калиевой соли разложение перешло сразу во вспышку, можно заключить, что она наиболее чувствительна к тепловому воздействию, чем соединение натриевая соль.
Температуры плавления полученных соединений выше, чем в литературном
источнике [5], где для гидразиниевой и калиевой солей 4-нитросемикарбазида одна
температура плавления, равная 130°C, для соединения натриевой соли литературные
данные отсутствуют.
.5 Результаты изучения реакций взаимодействия S-метилтио-N-нитрокарбамата
с аммиаком
В ходе экспериментов была получена аммонийная соль S-метилтио-N-нитрокарбамата, которая в УФ-спектре имеет пик 281,0 нм с интенсивностью 0,755. Аммониевая соль S-метилтио-N-нитрокарбамата имеет те же пики, что и сам S-метилтио-N-нитрокарбамат, что указывает на то, что соединение S-метилтио-N-нитрокарбамат существует в анионной форме и катионы на УФ-спектры не влияют. Аммониевая соль S-метилтио-N-нитрокарбамата имеет Тпл=104°С, выше, чем у исходного соединения (Тпл=67°С).
Аммониевая соль S-метилтио-N-нитрокарбамата очень хорошо растворима в воде, растворима в этаноле, хуже в ацетоне, в изопропаноле растворима лучше, чем в ацетоне, но хуже, чем в этаноле.
В заключение хотелось бы сказать, что S-метилтио-N-нитрокарбамат представляет интерес не только как промежуточный продукт для синтеза новых энергоемких материалов, но и как индивидуальное вещество, в связи с тем, что весь ряд тиокарбонатов широко используется как гербицидные и фунгицидные вещества.
Выводы:
1. В ходе реакции нуклеофильного замещения гидроксидами натрия и калия меркаптогруппы S,S′-ди(метилтио)-N-нитроимина были получены соответствующие соли S-метилтио-N-нитрокарбамата.
2. Были впервые также получены аммониевая и гидразиниевая соли S-метилтио-N-нитрокарбамата взаимодействием свободного S-метилтио-N-нитрокарбамата с аммиаком и гидразином.
. В результате взаимодействия S-метилтио-N-нитрокарбамата и его солей с гидразином были получены калиевая, натриевая и гидразиниевая соли 4-нитросемикарбазида. Этот способ является новым методом получения производных 4-нитросемикарбазида.
. Строение полученных веществ подтверждено УФ- и
ИК-спектроскопией, элементным анализом.
4. Безопасность и экологичность работы
Улучшение условий труда - самостоятельная и важная задача социальной политики государства. Большое внимание уделяется созданию здоровых и безопасных условий труда. Под охраной труда понимается система законодательных актов и соответствующих социально-экономических, гигиенических и организационных мероприятий, обеспечивающих безопасность, сохранение здоровья и работоспособности человека.
Охрана труда изучает производственные опасности и вредности, разрабатывает методы их предотвращения с целью устранения несчастных случаев, профессиональной заболеваемости, а также аварий и пожаров.
Главным объектом исследования является человек в процессе труда, производственная сфера и обстановка, взаимосвязь человека с оборудованием, технологическим процессом.
Совершенствование условий труда, улучшение контроля за соблюдением
требований действующих норм контроля является необходимым для обеспечения
безопасности работы, как на промышленных предприятиях, так и в химических
лабораториях.
.1 Факторы опасности, вредности при выполнении дипломной работы
Организации безопасного труда химиков должно быть уделено особое внимание ввиду того, что работа в химических лабораториях неизбежно связана с рядом опасных и вредных факторов. Например, при работе с электрооборудованием существует фактор опасности поражения электрическим током при неправильном обращении с электроприборами. Которые представляют пожарную опасность, как в нормальном режиме работы, так и при повреждениях (короткое замыкание, воспламенение изоляции).
Опасность при работе со стеклянной посудой заключается в возможности ранения, порезов вследствие хрупкости стекла.
Также опасность существует при работе с ЛВЖ, так как они способны образовывать взрывоопасные смеси, так как при работе с ними могут быть получены ожоги кожных покровов, а также отравление парами некоторых растворителей.
Норма загрузки лаборатории для ежедневного хранения и использования ЛВЖ,
ГЖ и кислот: ацетон - 2 л., гексан - 1 л., бензол - 1 л, изопропиловый спирт -
1 л, азотная кислота - 1 л, серная кислота - 1 л. Предельная норма хранения
ЛВЖ, ГЖ в лаборатории - 10,0 л.
.2 Характеристика веществ, используемых в работе
Приступая к выполнению работы с химическими веществами, каждый должен ознакомиться с их токсическим действием, влиянием на организм и мерами защиты и профилактики от возможного вредного действия.
Меры индивидуальной защиты от вредных веществ должны оговариваться в
инструкциях и методиках ведения работ, а также должна предусматриваться
возможность замены таких веществ на менее вредные и опасные.
Таблица 4.1 - Токсикологическая характеристика веществ
|
Вещество |
Агрегатное состояние |
Плотность, кг/м3 |
ПДК, мг/м3 |
Характер воздействия на организм |
Средства индивидуальной защиты |
Класс опасности |
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
Метил меркаптан CH3SH |
Газ |
0,868 |
0,8 |
Раздражающее действие на дыхательные пути и на нервную систему |
Противогаз марки А |
2 |
|
Серная кислота h2so4 |
Жидкость |
1,836 |
1,0 |
Раздражающее действие слизистых оболочек; при попадании на кожу дает сильные ожоги |
Перчатки резиновые, фартук, маска |
2 |
|
Азотная кислота hn03 |
Жидкость |
1,515 |
2,0 |
Раздражающе действует на дыхательные пути и глаза ввиду выделения двуоиси азота, вызывает ожоги кожи |
Перчатки резиновые, фартук, маска |
3 |
|
Уксусный ангидрид (СН3СО)2О |
Жидкость |
1,328 |
0,1 |
Контактный яд, раздражающе действует на дыхательные пути и слизистую систему, при попадании на кожу вызывает ожоги и долго незаживающие язвы |
Противогаз марки А, перчатки резиновые, фартук, очки |
1 |
|
Ацетон |
810 |
200 |
Поражение ЦНС, накапливание в организме, раздражение слизистых оболочек. |
Защита кожи, спецодежда, смягчающие крема и мази, противогаз. |
4 |
|
|
Гексан |
Ж |
660 |
300 |
Действует на слизистые оболочки глаз и верхних дыхательных путей, сухость кожи. |
Свежий воздух, противогаз, спецодежда, перчатки. |
4 |
Примечание: ж - жидкость.
Анализ взрыво- и пожароопасных свойств веществ и материалов, применяемых в научно - исследовательской работе, приведён в таблице 4.2.
Таблица 4.2 - Взрыво- и пожароопасные свойства веществ и материалов
|
Вещество |
Агрегатное состояние |
Плотность кг/м3 |
Температура вспышки, С |
Температура самовоспламенения, С |
Средства пожаротушения, |
|
1 |
2 |
3 |
4 |
5 |
6 |
|
Уксусный ангидрид (СН3СО)20 |
Жидкость |
1082 |
40 |
505 |
Пена химическая специальная, СО2, пар водяной. |
|
Ацетон |
Жидкость |
810 |
-18 |
465 |
Пена химическая специальная, СО2, пар водяной. |
|
Гексан |
Жидкость |
660 |
-23 |
200 |
Пена химическая специальная, СО2. |
4.3 Характеристика потенциальных опасностей в процессе выполнения
экспериментальной части работы и методы защиты
Перед началом работы в лаборатории с целью обеспечения безопасности труда, ответственным по технологической безопасности проводится вводный инструктаж непосредственно на рабочем месте.
Соблюдались правила обращения с химической посудой, изделиями из стекла, во избежание порезов.
В процессе выполнения работы соблюдались правила техники безопасности при работе с вредными веществами. При хранении таких веществ соблюдались меры предосторожности: ЛВЖ хранились в специальных железных ящиках. Ёмкости для хранения химических веществ имели этикетки с разборчивыми надписями.
Для работы с электронагревательными приборами и электродвигателем использовался источник переменного тока напряжением 220В. Перед началом работы проверялась исправность электроприборов. Все приборы имели заземление. Для блокировки тока в лаборатории применялись общие рубильники.
Согласно действующим нормам в лаборатории при проведении
экспериментальных работ, использовались средства индивидуальной защиты. Для
защиты одежды при работе используются халаты. Для защиты глаз и лица
используются очки и маска. Для защиты кожи рук использовались резиновые
перчатки.
.4 Санитарно-гигиенические характеристики лаборатории
Помещение химической лаборатории по своему устройству и планировке должно соответствовать требованиям строительных норм и правил, а так же нормам проектирования высших учебных заведений.
Научно - исследовательская работа проводилась в лаборатории, находящейся на территории кафедры "Химической технологии органических соединений азота и экологической безопасности производств", главного учебного корпуса СибГТУ. Помещение занимает площадь 48 м2, объём лаборатории составляет 168 м2 . Оборудование занимает объём помещения лаборатории 18 м2. Количество рабочих мест -4. Лаборатория оснащена следующим: 4 лабораторных стола, 4 вытяжных шкафа, весы аналитические, весы технические, УФ спектрофотометр, 3 письменных стола, термостат; первичные средства пожаротушения (огнетушитель ОУ-2 и ОУ-5, песок, кошма); для оказания первой медицинской помощи - аптечка.