Материал: Изучение реакций взаимодействия ди(метилтио)нитримина с гидроксидом натрия и гидроксидом калия
Изучение реакций взаимодействия ди(метилтио)нитримина с гидроксидом натрия и гидроксидом калия
Реферат
В дипломной работе проведены исследования реакций взаимодействия ди(метилтио)нитримина с нуклеофильными реагентами.
Дипломная работа содержит графическую часть на 5-ти листах формата А1 и
пояснительную записку из 83 страниц текста, 27 таблиц, 18 рисунков.
Содержание
Введение
. Литературный обзор
.1 Ди(метилтио)нитримин
.2 Нитропроизводные мочевины
.3 4-Нитросемикарбазид и его соли
.4 Заключение по литературному обзору
. Экспериментальная часть
.1 Используемые приборы и оборудование
.2 Синтез исходных соединений и ди(метилтио)нитримина
.2.1 Синтез роданистого метила
.2.2 Получение сульфата S-метилизотиомочевины
.2.3 Получение метилмеркаптана
.2.4 Получение гидрохлорида S,S′-ди(метилтио)имина
.2.5 Получение S,S¢-ди(метилтио)-N-нитроимина
.3 Исследование взаимодействия S,S′-ди(метилтио)-N-нитроимина с нуклеофильными реагентами
.3.1 Изучение реакции взаимодействия S,S′-ди(метилтио)-N-нитроимина с едким натром
.3.1.1 Получение S-метилтио-N-нитрокарбамата
.3.1.1.1 Очистка S-метилтио-N-нитрокарбамата
.3.1.2 Получение натриевой соли S-метилтио-N-нитрокарбамата
.3.2 Изучение реакции взаимодействия S,S′-ди(метилтио)-N-нитроимина с едким калием
.3.2.1 Получение калиевой соли S-метилтио-N-нитрокарбамата
.4 Исследование взаимодействия продуктов реакций S,S¢-ди(метилтио)-N-нитроимина с едкими натром и калием с гидразином-гидратом и раствором аммиака
.4.1 Изучение реакции взаимодействия S-метилтио-N-нитрокарбамата с раствором аммиака
.4.2 Изучение реакции взаимодействия S-метилтио-N-нитрокарбамата с гидразином-гидратом
.4.3 Изучение реакции взаимодействия натриевой соли S-метилтио-N-нитрокарбамата с гидразином-гидратом
.4.4 Изучение реакции взаимодействия калиевой соли S-метилтио-N-нитрокарбамата с гидразином - гидратом
. Обсуждение результатов
.1 Результаты синтеза гидрохлорида S,S′-ди(метилтио)имина
.2 Результаты синтеза S,S′-ди(метилтио)-N-нитроимина
.3 Результаты изучения реакции взаимодействия S,S′-ди(метилтио)-N-нитроимина с едким натром, а также с едким калием
.4 Результаты изучения реакций взаимодействия S-метилтио-N-нитрокарбамата и его солей с гидразином
.4.1 Температуры плавления полученных солей 4-нитросемикарбазида
.5 Результаты изучения реакций взаимодействия S-метилтио-N-нитрокарбамата с аммиаком
. Безопасность и экологичность работы
.1 Факторы опасности, вредности при выполнении дипломной работы
.2 Характеристика веществ, используемых в работе
.3 Характеристика потенциальных опасностей в процессе выполнения экспериментальной части работы и методы защиты
.4 Санитарно-гигиенические характеристики лаборатории
.5 Характеристика системы вентиляции
.6 Характеристика системы отопления
.7 Характеристика освещения лаборатории
.8 Пожарная профилактика и средства пожаротушения
.9 Мероприятия личной безопасности при проведении работ
.10 Средства индивидуальной защиты
.11 Охрана окружающей среды
. Гражданская оборона и чрезвычайные ситуации
. Экономическая часть
.1 Организация исследований
.1.1 Организация рабочего места
.1.2 Нормирование труда
.1.3 Охрана труда и эстетика производства
.1.4 Режим труда и отдыха
.1.5 Сетевой график выполнения работ
.1.6 Определение плановой себестоимости выполнения НИР
.1.7 Статья "Сырье и материалы"
.1.8 Статья "Покупные изделия, полуфабрикаты"
.1.9 Статья "Охрана труда и техника безопасности"
.1.10 Статья "Энергетические ресурсы"
.1.11 Статья "Основная заработная плата"
.1.12 Статья " Расчет амортизации помещения и оборудования"
.1.13 Статья "Накладные расходы"
.1.14 Составление калькуляции плановой себестоимости проведения НИР
Заключение
Список
использованных источников
Введение
На сегодняшний день во многих развитых странах мира считается актуальным поиск новых энергоемких соединений, обладающих заданным комплексом физико-химических свойств [1, 2].
Это является одной из основных задач современной химии и данной работы. Большое внимание в работе уделено доказательству строения полученных веществ современными физико-химическими методами такими как ИК- и УФ-спектроскопия, элементный анализ.
Различные нитроимины сами являются энергоемкими соединениями и широко используются для получения других энергоемких веществ [3].
В данной работе будут изучены реакции взаимодействия S,S′-ди(метилтио)-N-нитроимина
с гидроксидом натрия и гидроксидом калия. Получены следующие вещества:
S-метилтио-N-нитрокарбамат, натриевая, калиевая, аммониевая и гидразиниевая
соли S-метилтио-N-нитрокарбамата, калиевая, натриевая и гидразиниевая соль
4-нитросемикарбазида.
1. Литературный обзор
.1 Ди(метилтио)нитримин
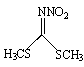
,S′-ди(метилтио)-N-нитроимин имеет в своем строении две легко замещающиеся меркаптогруппы и представляет значительный интерес для синтеза новых нитроиминных соединений.
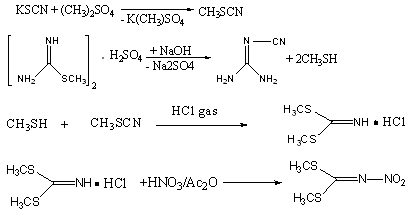
Соединение получают нитрованием гидрохлорида S,S′-ди(метилтио)имина,
который, в свою очередь, синтезируют при взаимодействии роданистого метила и
метилмеркаптана в растворе хлороформа при пропускании через него сухого
хлористого водорода:
Поскольку в данной работе нами были получены производные динитромочевины
и 4-нитросемикарбазида, то в литературном обзоре мы рассмотрим получение и
свойства данных веществ.
1.2 Нитропроизводные мочевины
Нитрование моноалкилмочевин в среде концентрированной серной кислоты
приводит к образованию N-алкил-N¢-нитромочевины. Нитрование атома азота, связанного с
алкильной группой, обычно не происходит.
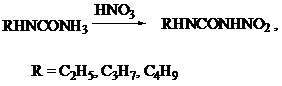
При нитровании симметричной диметилмочевины концентрированной азотной
кислотой, смесью азотной кислоты с уксусным ангидридом или пятиокисью азота в
хлороформе образуется N,N¢-диметил-N,N¢-динитромочевина:
![]()
При нитровании нитромочевины тетрафторборатом и гексафторсиликатом нитрония в среде этил- и бутилацетата или ацетонитрила в течение 2-4 ч при -10 ÷ -20°С образуется динитромочевина.
После обработки реакционных смесей раствором гидроксида калия и отделения
солей неорганических кислот образуется смесь моно- и дикалиевой солей
симметричной динитромочевины:
![]()
При пропускании хлористого водорода в эфирную суспензию как моно-, так и дикалиевой солей выделена динитромочевина:
![]()
Динитромочевину можно получить нитрованием мочевины, нитрата мочевины и
нитромочевины серноазотными кислотными смесями [4]:
![]()
Симметричная N,N¢-динитромочевина - достаточно сильная двухосновная кислота, способная
постадийно отщеплять протоны, с образованием кислых и средних солей:
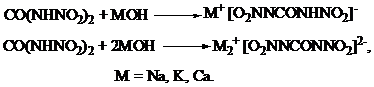
Длительное нагревание водных растворов моносолей приводит к получению
средних солей:
![]()
Избыточное количество щелочи разлагает образующуюся соль полностью:
![]()
При взаимодействии моносолей динитромочевины со щелочами могут образовываться соли, содержащие различные катионы. Так в результате обработки водного раствора моноаммониевой соли динитромочевины водным раствором КОН с последующим осаждением этиловым спиртом получается двойная соль [5]:
нитропроизводный мочевина нуклеофильный синтез
![]()
При нитровании калиевой соли N-метил-N¢-нитромочевины в безводной смеси серной и азотной кислот продуктом реакции является N-метил-N,N¢-динитромочевина. Идентичный продукт получается при нитровании самой N-метил-N¢-нитромочевины.
Аналогично протекает процесс нитрования N-бутил-N¢-нитромочевины [6]:
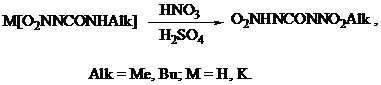
Гидролиз динитромочевины приводит к образованию нитрамида:
![]()
Нуклеофильным реагентом в этой реакции может служить не только вода. Образование нитрамида также наблюдается и в безводных растворителях, что можно объяснить сольволизом [7].
Нитраминные группы, находящиеся в структуре динитромочевины, относятся к первичным, для которых характерна реакция их взаимодействия с формальдегидом. При конденсации N,N¢-динитромочевины с формальдегидом в мольном соотношении 1:1 и водной среде в присутствии серной кислоты при 20÷80°С образуется метилендинитрамин. При обработке этого вещества KOH получается калиевая соль метилендинитрамина [8]:
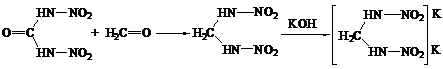
При обработке N,N¢-динитромочевины водным раствором глиоксаля образуется
4,5-дигидрокси-1,3-динитро-1,3-диазациклопентан-2-он [9]:
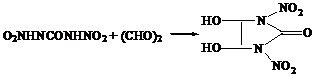
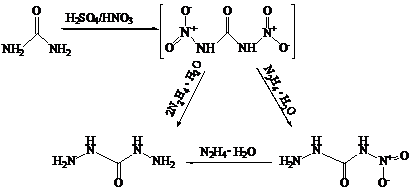
Из N,N¢-динитромочевины можно получить 1,3-диаминомочевину. Способ ее получения включает в себя следующие стадии:
) нитрование мочевины серно-азотной смесью, получение N,N¢-динитромочевины;
) взаимодействие с гидразин-гидратом, получение 1,3-диаминомочевины.
Вторую стадию можно проводить с промежуточным выделением 4-нитросемикарбазида
[10].
.3 4-Нитросемикарбазид и его соли
Соединение впервые было получено и охарактеризовано в работе [5]. При
обработке динитромочевины гидразином при мольном соотношении 1:1-2 после
соответствующих превращений был выделен и идентифицирован 4-нитросемикарбазид.
Избыток гидразина приводит к гидразиниевой соли 4-нитросемикарбазида:
![]()
-Нитросемикарбазид - бесцветное кристаллическое вещество, умеренно
растворимое в воде. В кристаллическом виде находится в виде смеси нейтральной и
заряженной форм, причем разделить смесь очень сложно.
![]()
Нитросемикарбазид плавится в интервале 227-235°С. При повторном нагревании закристаллизовавшегося образца плавление происходит при более высокой температуре 260-263°С. Отмечено, что для нейтральной формы при 60-100°С наблюдается эндоэффект, свидетельствующий о наличии кристаллизационной воды в веществе.
Водный раствор 4-нитросемикарбазида обладает кислотными свойствами и, следовательно, способен взаимодействовать с основаниями [11].
С целью доказательства структуры 4-нитросемикарбазида получены калиевая и
никелевая соли [5].
![]()
Как известно, нитромочевина в реакциях с аминами почти всегда образует амиды с очень хорошими выходами. В этом случае на новый амидный остаток обменивается исключительно нитроамидная группа. Такой метод особенно пригоден для синтеза монозамещенных мочевин.
В результате из соответствующих аминов возможно получение метилмочевины, этилмочевины, н-бутилмочевины, этилендимочевины и т.д.
-Нитросемикарбазид в реакциях нуклеофильного замещения с аминами ведет
себя аналогично мочевине. В случае обработки 4-нитросемикарбазида раствором
аммиака в мольном соотношении 1:1 получается аммониевая соль
4-нитросемикарбазида, а при избытке аммиака - семикарбазид:
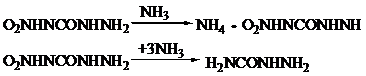
другими аминами реакция пойдет по такому же механизму. Положительные результаты были достигнуты при использовании метиламина и третбутиламина.
В качестве нуклеофильного агента может применяться гидразин-гидрат, в
ходе данной реакции образуется карбогидразид [11].
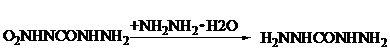
Соли на основе аниона 4-нитросемикарбазида с переходными металлами (Fe, Co, Ni, Zn) образуются с высоким выходом и являются стабильными соединениями с низкой чувствительностью.
Для синтеза солей 4-нитросемикарбазида с металлами IV группы используют катион титана (Ti4+).
При смешивании водных растворов 4-нитросемикарбазида и четыреххлористого титана образуется гидроксид титана.
При использовании солей 4-нитросемикарбазида со щелочными металлами или
аммиаком образуется кристаллогидрат титановой соли 4-нитросемикарбазида [12]:
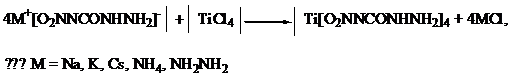
В реакции конденсации при смешивании водных растворов
4-нитросемикарбазида с глиоксалем в мольном соотношении 1:2 продуктом является
бис(нитросемикарбазон) глиоксаля:
![]()
При переводе 4-нитросемикарбазида в калиевую соль конечным продуктом
реакции является дикалиевая соль бис(нитросемикарбазон) глиоксаля. Подкисление
реакционной массы приводит к снятию катиона калия и образованию
бис(нитросемикарбазон) глиоксаля:

Бис(нитросемикарбазон) глиоксаля имеет кислотные свойства и вступает в
реакциию с основаниями. При взаимодействии его с аммиаком при 10°С образуется
диаммониевая соль бис(нитросемикарбазон) глиоксаля. Данное соединение также
образуется при конденсации глиоксаля с аммониевой солью 4-нитросемикарбазида
при комнатной температуре.
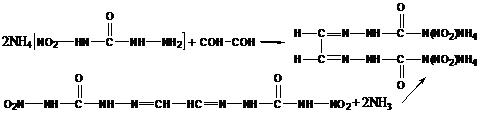
Избыток аммиака в течение 1 часа при температуре кипения раствора
разлагает бис(нитросемикарбазон) глиоксаля до бис(семикарбазон) глиоксаля:
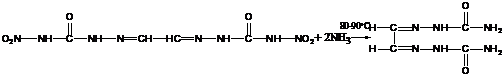
Титановую соль бис(нитросемикарбазон) глиоксаля получают из аммониевой
соли бис(нитросемикарбазон) глиоксаля обработкой четыреххлористым титаном в
водной среде при пониженной температуре [13]:
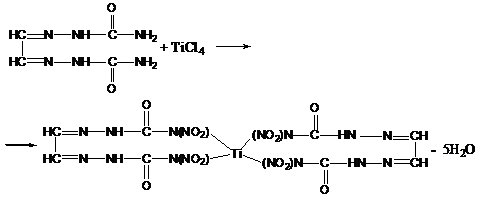
При взаимодействии 4-нитросемикарбазида с камфорой образуется калиевая
соль нитросемикарбазон камфанона [14]:

.4 Заключение по литературному обзору
Благодаря наличию двух легко замещающихся тиометильных групп S,S′-ди(метилтио)-N-нитроимин представляет значительный интерес для синтеза новых нитроиминых соединений. В данной работе мы планируем получить S-метилтио-N-нитрокарбамат, заместив одну из таких групп по механизму нуклеофильного замещения, и изучить реакционную способность этого соединения.
-Нитросемикарбазид представляет интерес как энергоёмкое и химически реакционное соединение, содержащее в своей структуре несколько различных по своей природе функциональных групп при одном атоме углерода в плане получения новых материалов. А разработка удобного способа его получения дает возможность для многотоннажного произвоства.