Материал: ХИМИЯ_Metodichka_organika
ИСТОЧНИКИ ИНФОРМАЦИИ:
1.Тюкавкина Н.А.,Бауков Ю.И. Биоорганическая химия: Учебник. –
М.:Медицина, 1991. – С.54-82, С.256-267.
2.Рево А.Ю., Зеленкова В.В. Малый практикум по органической химии – М.:Высшая школа, 1980.- С.151-152, 154-156.
3.Лекция по биоорганической химии.
4.Граф логической структуры.
ОРИЕНТИРОВАННАЯ ОСНОВА ДЕЯТЕЛЬНОСТИ
Инструкция к лабораторно-практическому занятию:
Образование кислой и средней калиевых солей D-винной кислоты.
Принцип метода: метод основан на различной растворимости кислий и средних солей винной кислоты.
Материальное обеспечение: пробирки, пипетки, штатив, шпатель, дистиллированная вода, 2М раствор винной кислоты, 0,5 М раствор КОН.
Ход работы:
1.В пробирку поместить 1 каплю раствора винной кислоты и добавить 2 капли раствора КОН.
2.Смесь хорошо встряхнуть.
3.Наблюдать образование белого кристаллического осадка.
4.Добавить избыток раствора КОН: еще 4-5 капель и перемешать.
5.Наблюдать постепенное растворение осадка.
6.Полученный раствор сохранить для последующего опыта.
7.Записать уравнение реакцій образования кислой и средней солей. Образование двух различных по растворимости солей свидетельствует о
налички двух карбоксильных групп в структуре винной кислоты.
Доказательство наличия гидроксильных групп в структуре винной кислоты.
Принцип метода: метод основан на способности образовывать внутрикомплексные соли с катионами Cu2+.
Материальное обеспечение: пробирки, пипетки, штатив, шпатель, газовая горелка, дистиллированная вода, раствор средней калиевой соли винной кислоты, 0,2 М раствор CuSO4, 2 М раствор NaOH.
Ход работы:
1.Поместить в пробирку 2 капли раствора сульфата меди и 2 капли раствора гидроксида натрия.
2.Наблюдать образование голубого осадка.
3.Добавить к осадку раствор тартрата калия, полученный в предыдушем опыте.
4.Наблюдать растворение осадка с образованием раствора ярко-синенго цвета.
5.Нагреть раствор над пламенем горелки.
6.Наблюдать отсутствие изменений в цвете раствора.
31
7. Записать уравнение образования комплексной соли и сделать вывод об отсутствии изменений при нагревании раствора.
Данная реакция иллюстрирует возможность использования жидкости Фелинга для подтверждения наличия нескольких гидроксильних групп в структуре моносахаридов.
Доказательство наличия фенольного гидроксила в структуре салициловой кислоты.
Принцип метода: метод основан на качественной цветной реакции с ионами
Fe3+.
Материальное обеспечение: пробирки, пипетки, штатив, шпатель, дистиллированная вода, 0,1 М раствор, кристаллическая салициловая кислота.
Ход работы:
1.В пробирку поместить 1-2 кристалла салициловой кислоты и добавить несколько капель дистиллированной воды, встряхнуть.
2.Добавить к полученному рас твору 1 каплю раствора FeCl3.
3.Наблюдать изменение окрашивания.
4.Записать уравнение реакции.
Доказательство отсутствия фенольного гидроксила в структуре ацетилсалициловой кислоты (аспирина) и ее гидролиз.
Принцип метода: метод основан на качественной цветной реакции фенольного гидроксила с ионами Fe3+.
Материальное обеспечение: пробирки, пипетки, штатив, шпатель, газовая горелка, дистиллированная вода, 0,1 М раствор FeCl3, кристаллический аспирин.
Ход работы:
1.В пробирку насыпать несколько кристаллов аспирина, добавить небольшое количество дистиллированной воды и перемешать до полного растворения.
2.Разделить полученный раствор на две части.
3.В первую пробирку добавить раствор FeCl3.
4.Сделать вывод об отсутствии окрашивания.
5.Раствор аспирина во второй пробирке прокипятить над пламенем горелки полторы минуты.
6.Записать уравнение гидролиза аспирина.
7.К охлажденному раствору добавить раствор FeCl3.
8.Наблюдать появление фиолетового окрашивания.
9.Сделать вывод о налички окрашивания и записат уравнение реакции. Различие в способности салициловой и ацетилсалициловой кислот
взаимодействовать с раствором хлорида железа (ІІІ) с образованием окрашенных соединений используется для определения чистоты аспирина, который при длительном хранении разлагается с образованием салициловой кислоты.
32
НАБОР ЗАДАНИЙ ДЛЯ ПРОВЕРКИ ДОСТИЖЕНИЯ КОНКРЕТНИХ ЦЕЛЕЙ ОБУЧЕНИЯ
Задание 1.
Лимонная кислота принимает участие в цикле трикарбоновых кислот (цикле Кребса). Укажите класс гетерофункциональных соединений, к которому она относится:
A.карбонильные соединения;
B.оксикислоты;
C.оксокислоты;
D.высшие жирне кислоты;
E.аминокислоты.
Задание 2.
Приведенная оксикислота является продуктом метаболизма жирных кислот:
|
|
H |
|
|
|
O |
|
CH3 |
|
C |
|
CH2 |
|
C |
|
|
|
|
|||||
|
|
|
|
|
|
|
OH |
OH
Укажите название данной кислоты:
A.пировиноградная;
B.ацетоуксусная;
C.молочная;
D.щавелевоуксусная;
E.β-гидроксимаслянная.
Задание 3.
Салициловая кислота – основа для синтеза жаропонижающих препаратов. Укажите, какая из приведенных структур, отвечает данной кислоте:
A.
B.
C.
D.
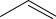
 COOH
COOH
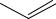
 OH
OH
|
COOH |
COOCH3 |
Е. |
OCH3 |
|
OH |
|

 COOCH3
COOCH3
 OCH3
OCH3

 COOH
COOH
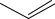
 O C CH3
O C CH3
O
33

Задание 4.
γ-оксимаслянная кислота обладает слабовыраженным наркотическим эффектом, а продукт ее взаимодействия с NaOH используется как анестезиологическое средство. Укажите название класса соединений данного продукта:
A.сложный эфир;
B.соль;
C.простой эфир;
D.амид;
E.кетон.
Задание 5.
Пировиноградная кислота – кетокислота, поэтому она характеризуется реакциями нуклеофильного присоединения, в том числе, реакцией с HCN. Укажите название образующегося продукта:
A.сложный эфир;
B.соль;
C.амид;
D.кетон;
E.оксинитрил.
Задание 6.
Яблочная кислота образуется в цикле Кребса из фумаровой и вступает в далнейшее окисление. Укажите структурную формулу окисленного соединения:
A.
B.
C.
D.
COOH
C O
O
CH3
COOH
COOH
COOH
C O
O
CH2 COOH
O
(пировиноградная кислота);
(щавелевая кислота);
(щавлевоуксусная кислота);
(уксусная кислота);
CH3 C
OH
E. СН3-СН2-ОН (этанол).
Задание 7.
Положение гидроксилной группы в молекуле оксикислоты (α, β, γ) определяет химические превращения, которые происходят с веществом при нагревании. Укажите название оксикислоты, которая в реакции дегидратации образует приведенное соединение:
34
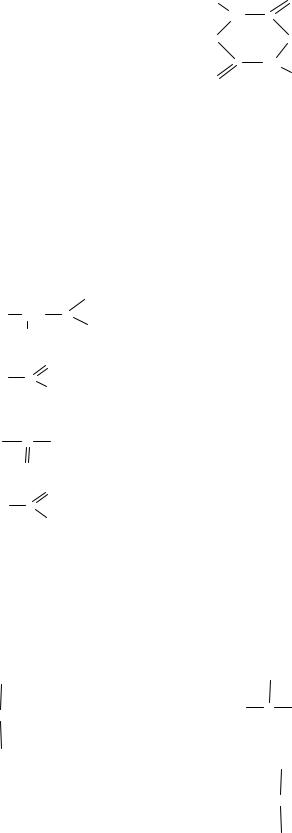
CH3 |
O |
CH |
C |
O |
O |
O
A.β-гидроксимаслянная;
B.молочная;
C.γ-гидроксимаслянная;
D.α- гидроксимаслянная;
E.β-гидроксипропионая.
C CH
CH3
Задание 8.
Пировиноградная кислота образуется в процессе гликолиза, а в дальнейшем происходит ее декарбоксилирование. Укажите продукт данной реакции:
O A. CH3 CH C 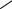
OH OH
O
B. CH3 C
H
C. CH3 C CH3
O
O
D. CH3 C
OH
E. СН3– СН2– ОН
(молочная кислота);
(уксусный альдегид);
(ацетон);
(уксусная кислота);
(этиловый спирт).
Задание 9.
При интенсивной работе, в мышцах накапливается L-(+)-молочная кислота, вследствие чего возникает характерная боль. Укажите структурную формулу данного изомера:
|
|
|
COOH |
|
|
|
COOH |
|||||||||||||
A. |
|
|
|
|
|
|
С. |
H |
C |
H |
||||||||||
H |
|
|
C |
|
|
OH |
|
|||||||||||||
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|||||||||
|
|
|
CH3 |
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
COOH |
|||||||||
|
|
|
|
|
COOH |
|
|
|
|
|
|
|
|
|||||||
B. |
|
|
|
HO |
|
|
|
|
C |
|
|
H |
||||||||
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
HO |
|
|
|
|
|
H |
|
D. |
|
|
|
|
|
CH3 |
||||||
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
CH2-COOH |
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
E. H |
|
|
|
|
|
COOH |
||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2-COOH
35