Материал: ХИМИЯ_Metodichka_organika
Растворимость мочевой кислоты и ее средней натриевой соли в воде.
Принцип метода: метод основан на сравнении растворимости мочевой кислоты и ее производных – натриевых солей.
Материальное обеспечение: пробирки, пипетки, штатив, шпатель, дистиллированная вода, кристаллическая мочевая кислота, раствор 2M NaОН.
Ход работы:
1.В пробирку поместить несколько кристаллов мочевой кислоты, добавить 2-3 капли дистиллированной воды и встряхнуть содержимое пробирки.
2.Добавить еще 5-6 капель воды и так же продолжать встряхивание.
3.Наблюдать образование гетерогенной системы, свидетельствующее о плохой растворимости мочевой кислоты.
4.К содержимому пробирки добавить 1 каплю 2М раствора NaОН.
5.Наблюдать мгновенное растворение кристаллов, вследствие образования легкорастворимой средней двузамещенной натриевой соли.
6.Полученный раствор сохранить для последующих опытов.
7.Записать уравнение образования двузамещенной натриевой соли мочевой кислоты.
Мочевая кислота в лактимной форме способна при взаимодействии со щелочами образовывать соли, которые называются ураты и обладают хорошей растворимостью.
Образование труднорастворимого урата аммония.
Принцип метода: метод основан на сравнительной характеристике растворимостей натриевых и аммониевых солей мочевой кислоты.
Материальное обеспечение: пробирки, пипетки, штатив, раствор урата натрия (полученный в предыдущем эксперименте), насыщенный раствор
NH4Cl.
Ход работы:
1.В пробирку поместить несколько капель, полученного в предыдущем опыте, раствора средней двузамещенной натриевой соли мочевой кислоты.
2.Добавить 1 каплю насыщенного раствора хлорида аммония.
3.Наблюдать образование белого кристаллического осадка мочекислого аммония.
4.Сохранить гетерогенную смесь для последующего эксперимента.
5.Записать уравнение образования урата аммония.
Различная растворимость натриевых и аммониевых солей может быть использована для выделения мочевой кислоты из смеси органических веществ.
Разложение уратов под влиянием минеральной кислоты (выделение кристаллической мочевой кислоты).
Принцип метода: метод основан на образовании кристаллов мочевой кислоты при изменении кислотности среды.
Материальное обеспечение: предметное стекло, пипетки, штатив, раствор урата аммония (полученный в предыдущем эксперименте), раствор 2М HCl.
Ход работы:
56
1.С помощью пипетки нанести на предметное стекло 1 каплю мутного раствора урата аммония, полученного в предыдущем опыте.
2.Добавить в центр капли 1 каплю 2М раствора HCl.
3.Наблюдать образование характерных удлиненных кристаллов образовавшейся мочевой кислоты.
4.Зарисовать в рабочем журнале форму кристаллов полученного препарата.
5.Записать уравнение образования мочевой кислоты из ее солей.
В организме образование кристаллов мочевой кислоты приводит к образованию мочевых камней, подагрических узлов и т.д., что происходит при уменьшении величины рН биологических жидкостей.
Качественная реакция на мочевую кислоту (мурексидная проба).
Принцип метода: метод основан на окислении мочевой кислоты до аллоксантина и образовании его окрашенных аммонийных солей.
Материальное обеспечение: предметное стекло, пипетки, штатив, раствор урата натрия (полученный в предыдущем эксперименте), раствор концентрированной HNO3, раствор 0,5M KOH.
Ход работы:
1.С помощью пипетки нанести на предметное стекло 1 каплю раствора урата натрия, полученного в предыдущем опыте.
2.Добавить в центр капли 1 каплю концентрированного раствора HNO3.
3.Выпарить смесь, держа стекло над пламенем горелки на расстоянии приблизительно 10 см.
4.После полного выпарения смеси, необходимо прекратить нагревание и остудить предметное стекло.
5.Поместить сбоку от высохшего пятна 1 каплю 0,5M раствора KOH.
6.Наблюдать образование полоски пурпурно-фиолетового цвета. Мурексидная проба применяется при анализе мочевых камней и прочих
отложений, когда имеется подозрение на мочевую кислоту. Так же эта качественная реакция применяется для открытия пуриновых производных таких как кофеин, теобромин и т.д.
НАБОР ЗАДАНИЙ ДЛЯ ПРОВЕРКИ ДОСТИЖЕНИЯ КОНКРЕТНЫХ ЦЕЛЕЙ ОБУЧЕНИЯ:
Задание 1.
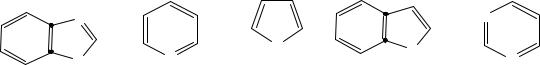
Дибазол – лекарственный препарат, понижающий артериальное давление, является производным бензимидазола. Среди перечисленных соединений укажите бензимидазол:
A. |
N |
B. |
C. |
D. |
|
E. |
N |
|
|
|
|||||
|
|
|
|
N |
N |
|
|
|
|
N |
|
H |
|
|
|
|
N |
|
H |
|
N |
||
|
H |
|
|
|
|
|
|
Задание 2. |
|
|
|
|
|
|
|
|
|
|
|
57 |
|
|
|
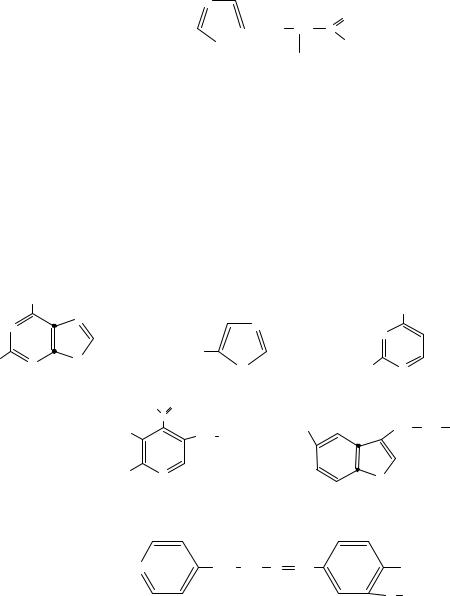
Аминокислота гистидин входит в состав многих белков и имеет в своей структуре гетероциклический радикал. Укажите ядро какого гетероцикла входит в состав этого радикала:
N
 CH2
CH2
N
H
A.индол;
B.пиримидин;
C.пиразол;
D.имидазол;
E.пиррол.
O
CH C
OH
NH2
Задание 3.
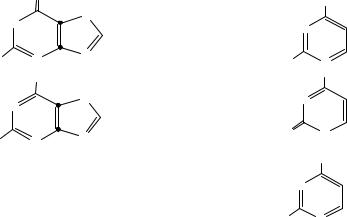
Ксантин образуется в организме в результате метаболизма нуклеиновых кислот и относится к классу гидроксипуринов. Укажите формулу данного соединения:
OH
|
|
N |
|
|
|
|
|
OH |
|
N |
|
|
|
N |
|
|
|
A. |
|
B. |
|
|
C. |
N |
||
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
HO |
|
N |
|
HO |
|
|
|
|
N |
|
|
|
N |
HO |
|
||
|
H |
|
|
|
N |
|||
|
|
|
|
|
||||
|
|
|
|
|
|
H |
|
|
|
|
|
H |
O |
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
HO |
|
CH2 |
OH |
HO |
|
CH2 CH2 NH2 |
|
|
D. |
|
E. |
|
|
||
|
|
|
|
|
|
|
||
|
|
CH3 |
N |
|
|
|
|
N |
|
|
|
|
|
|
|
|
H |
Задание 4.
Фтивазид является эффективным противотуберкулезным препаратом:
N |
CH2 NH N CH |
OH |
|
|
O CH3 |
Укажите гетероцикл, который входит в его состав:
A.пиррол;
B.пиразол;
C.пиримидин;
D.пиридин;
E.пурин.
Задание 5.
Гетероциклическое соединение пиррол имеет ароматический характер. Укажите количество электронов, которое отдает атом азота в замкнутую систему π-связей:
A.один;
B.электронную пару;
58
C.две электронные пары;
D.два неспаренных электрона;
E. ни одного электрона.
Задание 6.
В ходе лабораторной работы студент должен подтвердить кислотные свойства пиррола. Укажите реагент, позволяющий это осуществить:
A.CH3COOH;
B.HCl;
C.NaOH;
D.SO2Cl2;
E.H2/Ni.
Задание 7.
Для образования комплиментарной пары с цитозином в системе полинуклеотидных цепей, гуанин должен существовать в лактамной форме. Укажите структурную формулу данного изомера:
|
|
O |
|
|
|
|
H |
|
HN |
|
N |
A. |
|
C. |
|
|
|
||
H2N |
|
N |
N |
|
|
||
|
|
OH |
|
|
|
|
H |
|
N |
|
N |
|
|
|
B. |
|
D. |
H2N |
N |
N |
|
E.
OH
N
HO N
NH2
N
ON H
OH
N  CH3
CH3
HO N
Задание 8.
Опишите биологическую роль тетрапиррольного соединения – порфина:
A.образует комплекс с Fe2+, являющийся частью гема;
B.является коферментом окислительно-восстановительных процессов в организме;
C.используется как болеутоляющее и успокаивающее средство;
D.является структурным компонентом нуклеиновых кислот;
E.является нейромедиатором головного мозга.
Эталоны ответов к заданиям:
1 |
– А; |
5 – B; |
|
2 |
– D; |
6 |
– C; |
3 |
– A; |
7 |
– D; |
4 |
– D; |
8 – A. |
|
59
КРАТКИЕ МЕТОДИЧЕСКИЕ УКАЗАНИЯ ДЛЯ РАБОТЫ НА ПРАКТИЧЕСКОМ ЗАНЯТИИ
В начале занятия осуществляется проверка подготовки студентов к самостоятельной работе. Студенты решают учебные задания, разбирают и закрепляют теоретический материал, интерпретируют строение и свойства гетероциклических соединений, учатся писать реакции взаимодействия с другими соединениями и формулы пуриновых и пиримидиновых оснований, которые входят в состав нуклеиновых кислот.
После решения обучающих заданий студенты приступают к выполнению самостоятельной работы. Используя инструкцию к лабораторно-практическому занятию, они выполняют опыты и оформляют протокол лабораторной работы.
Далее проводится анализ и коррекция самостоятельной работы студентов. Занятие заканчивается тестовым контролем и подведением итогов.
α – АМИНОКИСЛОТЫ. ПЕПТИДЫ
АКТУАЛЬНОСТЬ ТЕМЫ:
Белки – это основа всего живого. Химия белков особая отрасль, которая никогда не была только “ химической”, а всегда объединяла в себе методы биологии, медицины, химии и физики. Белки - материальная основа клетки.
В то же время белки и пептиды построены из α– аминокислот. В состав белков входят около 70 α– аминокислот. Очевидно, что знание строения и свойств α– аминокислот необходимо для объяснения и прогнозирования структуры белковых молекул и их химических свойств. А также необходимы при дальнейшем изучении биологии, биохимии, функции белков на молекулярном уровне.
Вам необходимо ознакомиться с целями занятия, обдумать их, осознать необходимость изучения этой темы.
ЦЕЛИ ОБУЧЕНИЯ.
ОБЩАЯ ЦЕЛЬ.
Уметь интерпретировать строение и свойства важнейших аминокислот, а также структуру белковых молекул для дальнейшего изучения биологических функций белков на молекулярном уровне.
Достижение этой цели обеспечивается решением конкретных целей:
КОНКРЕТНЫЕ ЦЕЛИ.
УМЕТЬ:
1.Прогнозировать реакции α– аминокислот, исходя из свойств кислотной группы.
2.Прогнозировать реакции α– аминокислот, исходя из свойств основной группы.
3.Объяснить лиофильные и лиофобные свойства аминокислот и белков на основании природы и структуры радикалов.
60