Материал: ХИМИЯ_Metodichka_organika
Классиф. по строению радикала
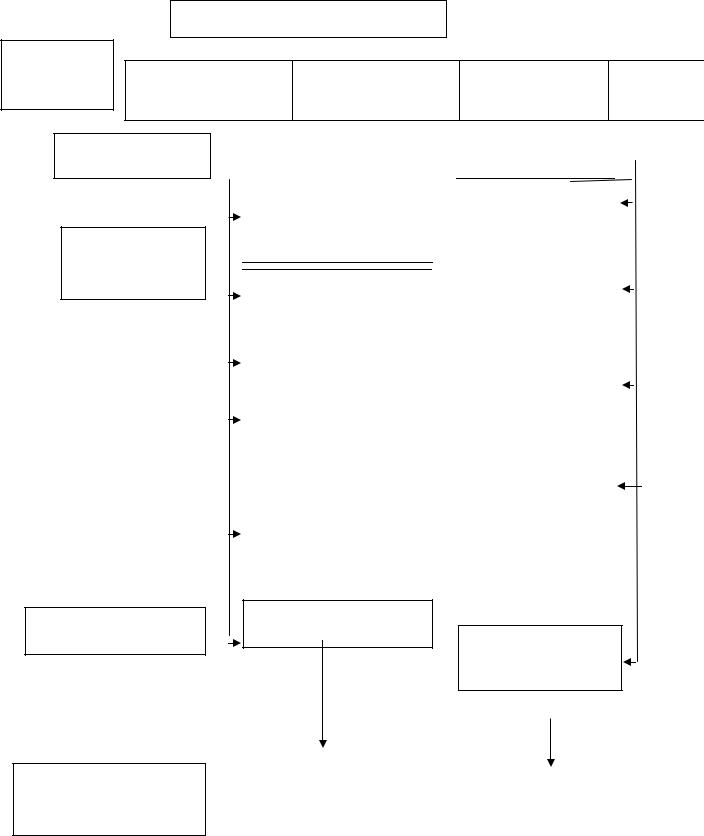
ГРАФ ЛОГИЧЕС КОЙ СТРУКТУРЫ ТЕМЫ:
«Строение и свойства альдегидов и кетонов».
Карбонильные соединения
Алифатические Ароматические Насыщенные Ненасы
Структура
Химические
свойства
Идентификация
Медико-биологическое значение
|
|
|
|
Электронное строение |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Альдегиды |
|
|
|
|
|
|
Кетоны |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
Реакции |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
нуклеофильного |
|
|
|
||||||
|
|
|
Реакции |
|
|
|
|
||||||||
|
|
|
нуклеофильного |
|
|
присоединения |
|
|
|
||||||
|
|
|
замещения |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
Реакции |
|
|
|
|
Реакции |
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
окисления |
|
|
восстановления |
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Реакции |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
восстановления |
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
Реакция |
|
|
|
|||||
|
|
|
|
|
|
|
|
альдольной |
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
конденсации |
|
|
|
||||||
|
|
|
Реакции |
|
|
|
|
||||||||
|
|
|
альдольной |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
конденсации |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
Реакция |
|
|
|
|
|
|
|
Реакции |
|
|
|
|
замещения |
в |
|
|
||||
|
|
|
замещения |
в |
|
|
|
радикале |
|
|
|
||||
|
|
|
радикале |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Реакция серебряного зеркала Реакция с
нитропрусидом
натрия
Формальдегид, |
|
Ацетон |
уксусный |
|
|
|
|
|
альдегид |
|
|
- 6 -

ОРИЕНТИРОВАННАЯ ОСНОВА ДЕЯТЕЛЬНОСТИ:
Инструкция к лабораторно-практическому занятию.
Окисление формальдегида гидроксидом меди (II) в щелочном растворе.
Принцип метода: метод основан на реакции окисления альдегидов. Материальное обеспечение: пробирки, пипетки, 2Н раствор NaOH, 0,2H
раствор CuSO4 , 40% раствор формальдегида, дистиллированная вода.
Ход работы:
1.Поместите в пробирку 6 капель 2Н NaOH, разбавьте его 6 каплями воды и добавьте 1 каплю 0,2H CuSO4.
2.К выпавшему осадку добавьте 2-3 капли 40% раствора формалина и взболтайте раствор.
3.Нагрейте до кипения только верхнюю часть раствора так, чтобы нижняя часть раствора осталась для контроля холодной. В нагретой части пробирки выделится осадок, сначала жёлтый, затем красный.
O |
O |
|
HC + Cu(OH) |
|
HC + CuOH +H2O |
2 |
||
H |
OH |
|
Жёлтый осадок гидроксида меди (I) при нагревании легко теряет воду и превращается в оксид меди (I) красного цвета:
2CuOH → H2O + Cu2O
Это очень важная качественная реакция восстановительную способность. Она широко медицине как проба Троммера. В химии количественного определения.
на альдегидную группу, её применяется в биохимии и сахаров применяется для
Осаждение белковых тел формалином.
Принцип метода: метод основан на осаждении белковых тел формалином. Материальное обеспечение: Пробирки, раствор куриного белка, 40%
раствор формалина. Ход работы:
1.Налейте в пробирку 0.5 мл раствора куриного белка и добавьте несколько капель формалина.
2.Перемешайте – происходит свёртывание белка под действием формалина.
Цветная реакция на ацетон с нитропруссидом натрия.
Принцип метода: метод основан на открытии ацетона цветной реакцией с нитропруссидом.
Материальное обеспечение: пробирки, дистиллированная вода, раствор 2Н NaOH, раствор 0,5Н нитропруссида натрия. Na2[Fe(CN)5NO], водный раствор ацетона, раствор 2Н CH3COOH.
Ход работы:
1.Налейте в пробирку 1 каплю 0.5Н раствора нитропруссида натрия, 5 капель дистиллированной воды и 1 каплю водного раствора ацетона.
2.Добавьте 1 каплю 2Н раствора NaOH. Что вы наблюдаете?
3.Разлейте раствор в две пробирки и в одну пробирку добавьте 1 каплю 2Н раствора CH3COOH. Сравните окраску растворов в обеих пробирках.
4.Цветная реакция с нитропруссидом натрия (проба Легаля) широко применяется в клинической практике для открытия ацетона в моче при сахарном диабете.
НАБОР ЗАДАНИЙ ДЛЯ ПРОВЕРКИ ДОСТИЖЕНИЯ КОНКРЕТНЫХ ЦЕЛЕЙ ОБУЧЕНИЯ.
Задание №1.
Формалин используют как консервант для хранения биологических тканей. Среди приведенных формул найдите это соединение:
О
A.Н – С |
D. СН3 – О – СН3 |
|
Н |
|
О |
В. СН3ОН |
Е. Н – С |
|
ОН |
|
О |
С. СН3 |
СН3 |
|
Задание №2.
Состояние атома углевода карбонильной группы определяет характер и тип реакции соединений, которые её содержат.
Какое состояние гибридизации характерно для этого атома?
A.Sp-гибридизация с отрицательным зарядом.
B.Sp-гибридизация с положительным зарядом.
C.Sp²-гибридизация с отрицательным зарядом.
D.Sp²-гибридизация с положительным зарядом.
E.Sp²-гибридизация без электрического заряда.
Задание №3.
Реакции нуклеофильного присоединения характерны для альдегидов и кетонов. Укажите, чем обусловлен механизм этих реакций.
A.Эффектом ароматичности.
B.Отрицательным зарядом на атоме углерода карбонильной группы.
C.Отсутствием заряда на атоме углерода карбонильной группы
D.Положительным зарядом на атоме углерода карбонильной группы.
E.Эффектом сопряжения.
8
Задание №4.
Ацетон образуется в организме при различных нарушениях метаболизма. Укажите вещество, которое образуется в результате реакции восстановления этого соединения.
A.Пропан-1.
B.Пропан-2.
C.Пропановая кислота.
D.Пропаналь-1.
E.Пропаналь-2.
Задание №5.
Хлорирование пропионового альдегида обусловлено подвижностью одного из атомов водорода в радикале.
Укажите продукт этой реакции:
A.β-хлорпропионовый альдегид.
B.ά-хлорпропионовый альдегид.
C.ά-хлорпропионовая кислота.
D.Хлорацетон.
E.2-хлорпропан.
Задание №6.
Кетоны обладают более низкой реакционной способностью, чем альдегиды. Каким электронным эффектом это можно объяснить?
A.–M- эффектом заместителей.
B.+ M- эффектом заместителей.
C.– Ǐ- эффектом заместителей.
D.+ Ǐ - эффектом заместителей.
E.Эффектом сопряжения.
Задание №7.
В медицинской практике широко применяется формалин. Укажите 35-40% раствор этого вещества
A.Этаналя в воде.
B.Метаналя в воде.
C.Этанола в воде.
D.Метанола в воде.
E.2,3-диметилпропаналя в воде.
Приложение.
Задачи для достижения конкретных целей.
Задача №1.
Формальдегид применяется в производстве лекарственного средства уротропина.
Какие химические преобразования могут произойти при взаимодействии формальдегида с синильной кислотой?
9
Эталон ответа:
О
Формальдегид Н – С вступает в большое количество реакций, пред-
Н
ставляет собой одну из наиболее реакционных групп в соединениях.
Этап 1:
Взаимодействия метаналя с синильной кислотой, которая приводит к получению оксинитрила, осуществляется по механизму нуклеофильного присоединения.
Для повышения реакционной способности карбонильной группы применяется кислотный катализ, который приводит к увеличению положительного заряда на атоме углерода (повышение электро-
отрицательности): |
ОН+ |
|
О |
ОН |
|
Н – С + Н+ → Н – С |
→ Н – С+ |
|
Н |
Н |
Н |
Этап 2:
Протонированный метаналь присоединяет нуклеофильную часть молекулы
HCN.
Присоединение сопровождается выбросом протона и образованием оксинитрила:
OH |
OH |
H – C + |
+ CN ¯ → H – C ––– CN |
H |
H |
Вывод: При взаимодействии метаналя с синильной кислотой образуется оксинитрил по механизму нуклеофильного присоединения.
Задача №2.
Реакция получения полуацеталей лежит в основе образования циклических форм глюкозы. Какое химическое преобразование произойдёт с 5- гидроксигексаналем в кислой среде?
Эталон ответа:
5-гидроксигексаналь – гетерофункциональное соединение, которое содержит две функциональные группы: спиртовую и альдегидную, то есть оно сочетает в себе свойства спиртов и альдегидов.
О
CH3 – CH – CH 2 – CH 2 – CH 2 – C
| |
H |
OH
Все атомы углерода в углеводородном радикале находятся в Sp²гибридизованном состоянии, поэтому углеродная цепь может принимать
10