Материал: ХИМИЯ_Metodichka_organika
различные конформации. При этом в пространстве сближаются углеродные атомы С1-С5 или С1-С4.
В случае сближения С1-С5 в 5-гидроксигексанале в кислой среде возможно взаимодействие между гидроксильной и альдегидной группами с образованием циклического полуацеталя.
Вывод: В связи с присутствием в молекуле 5-гидроксигексаналя альдегидной и гидроксильной групп в кислой среде между ними происходит внутримолекулярное взаимодействие (реакция нуклеофильного присоединения), которое приводит к образованию циклического полуацеталя - пиранозного цикла.
Задача №3.
Имины - промежуточные продукты во многих ферментативных процессах, например, биосинтезе ά - аминокислот в организме.
Напишите схему реакции присоединения метиламина к пропаналю и ацетону. Почему эти реакции классифицируют как реакции присоединения - отщепления?
Задача №4.
Альдегиды легко окисляются, поэтому они могут служить хорошими восстановителями. Какие химические превращения будут происходить при взаимодействии уксусного альдегида с оксидом серебра, и как называется эта реакция?
Задача №5.
Какое из соединений: бензальдегид или пропаналь может вступать в реакцию альдольной конденсации. Свой ответ обоснуйте.
КРАТКИЕ МЕТОДИЧЕСКИЕ УКАЗАНИЯ ДЛЯ РАБОТЫ НА ПРАКТИЧЕСКОМ ЗАНЯТИИ.
На занятии студенты решают учебные задачи, в процессе этого разбирается и закрепляется теоретический материал. Студенты должны усвоить механизм реакции нуклеофильного присоединения, исходя из электронного строения альдегидов и кетонов, должны уметь составлять уравнения реакций окислениявосстановления, присоединения, замещения в радикале.
После решения заданий необходимо выполнить опыты, которые подтверждают теоретический материал. После выполнения опытов необходимо оформить протокол лабораторной работы.
Вконце занятия проводится тестовый контроль, анализ результатов работы,
вкотором принимают участия все студенты под руководством преподавателя.
11
СТРОЕНИЕ И ХИМИЧЕСКИЕ СВОЙСТВА МОНО- И ДИКАРБОНОВЫХ КИСЛОТ.
АКТУАЛЬНОСТЬ ТЕМЫ.
Карбоновые кислоты и их эфиры в большом количестве распространены в природе. Запахи цветов, плодов, ягод обусловлены эфирными веществами. Карбоновые кислоты и их производные поступают в организм человека с пищей, а затем превращаются в более простые вещества. Карбоновые кислоты и их соли входят в состав буферных систем (бикарбонатной, фосфатной, гемоглобиновой и др.), которые поддерживают постоянство рН крови и тканей. Некоторые карбоновые кислоты и их соли являются лекарственными препаратами. Например, изовалериановая кислота входит в состав валидола, бензоат натрия – откаркивающее и слабо дезинфицирующее средство, уретаны - эфиры карбаминовой кислоты обладают снотворным и транквилизирующим действием и применяются в психиатрической практике.
Эта тема имеет больше значение для изучения курса биохимии, фармакологии и других медицинских дисциплин.
ЦЕЛИ ОБУЧЕНИЯ:
ОБЩАЯ ЦЕЛЬ:
Уметь прогнозировать химические свойства карбоновых кислот и их производных, которые берут участие в протекании большинства биохимических процессов.
Достижение этой цели обеспечивается выполнением конкретних целей. КОНКРЕТНЫЕ ЦЕЛИ:
УМЕТЬ:
1.Идентифицировать карбоксильную группу.
2.Прогнозировать химические свойства карбоновых кислот на основании электронного строения их молекул.
3.Открывать экспериментально уксусную кислоту.
4.Прогнозировать свойства дикарбоновых кислот и их специфические реакции.
5.Получать экспериментально натриевую соль щавелевой кислоты и доказывать строение молекул этой кислоты.
СОДЕРЖАНИЕ ОБУЧЕНИЯ.
Содержание обучения должно обеспечивать достижение целей обучения.
ТЕОРЕТИЧЕСКИЕ ВОПРОСЫ:
1.Классификация и номенклатура карбоновых кислот. Электронное представление о строении карбоксильной группы.
2.Химические свойства карбоновых кислот. Кислотные свойства -
образование солей. Реакции нуклеофильного замещения (SN) взаимодействие со спиртами (реакция этерификации), с аммиаком и аминами, образование ангидридов, замещение водорода при α-углеродном атоме.
3.Классификация и номенклатура дикарбоновых кислот. Реакции образования солей, амидов и сложных эфиров. Отношение к нагреванию.
12
4.Ненасыщенные дикарбоновые кислоты малеиновая и фумаровая, их различие и участие фумаровой кислоты в обменных процессах.
5.Угольная кислота и ее производные: уретаны, уреиды, мочевина. ИСТОЧНИКИ ИНФОРМАЦИИ:
Обязательные:
1.Тюкавкина Н.А.. Биоорганическая химия, 1985, с.191-193, 196-197, 204-
211, 216-225.
2. Тюкавкина Н.А.. Биоорганическая химия, 1991, с.194-205, 207-213, 247252.
3.Рево А.Я., Зеленкова В.В., Малый практикум по органической химии, 1980, опыты 42, 43, 44, 45.
4.Граф логической структуры.
5.Лекции по биоорганической химии.
Дополнительные:
1. Черных В.П. и др., Органическая химия, книга 2, Харьков, Основа, 1995,
с.358-371, 383-395.
13
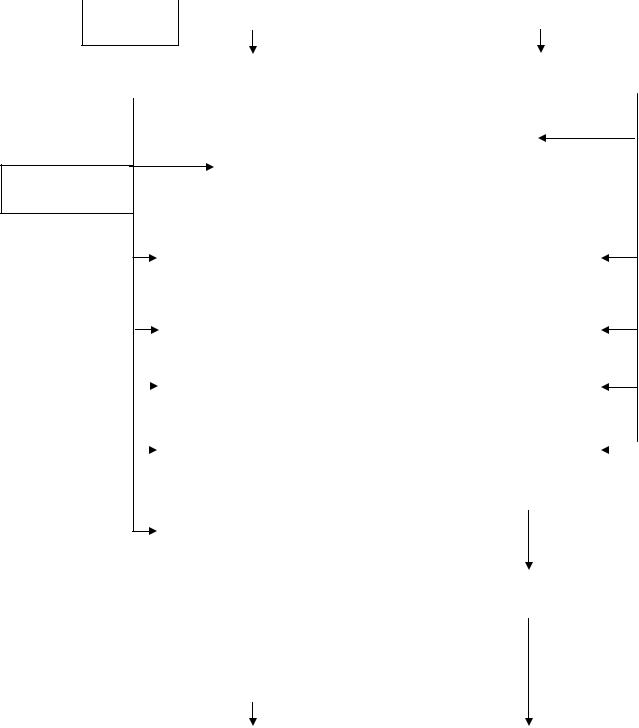
ГРАФ ЛОГИЧЕСКОЙ СТРУКТУРЫ ТЕМЫ:
«Строение и свойства моно - и дикарбоновых кислот»
|
|
|
|
|
|
КАРБОКСИЛЬНЫЕ СОЕДИНЕНИЯ |
|
||||||||
Классификация |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||
по радикалу |
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
Ароматические |
|
Насыщенные |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
Алифатиические |
|
|
|
|
Ненасыщенные |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
Электронное строение |
|
|
|||||
|
Структура |
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Структура
|
|
Дикарбоновые |
Монокарбоновые |
|
|
|
|
|
|
|
|
|
|
|
Реакция |
|
Реакция |
диссоциации |
|
диссоциации |
|
|
|
Химические
свойства
Реакция нуклеофильного |
|
Реакция нуклеофильного |
замещения |
|
замещения |
|
|
|
|
|
Реакция образования |
|
|
|
|
Реакция образования |
|
|
|
|
солей |
|
|
|
|
солей |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Реакция этерификации |
|
|
|
|
Реакция образования |
|
|
|
|
|
|
|
|
|
амидов |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Реакция образования |
|
|
|
Специфические реакции, |
|
|
|
|
|
амидов, ангидридов |
|
|
|
отношение к нагреванию |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Реакция замещения в |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
радикале |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Идентификация |
|
|
|
|
|
|
Открытие щавелевой |
|
|
|
|
|
|
|
|
|
кислоты |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Открытие уксусной |
|
|
|
|
|
|
|
|
|
кислоты образованием |
|
|
|
|
|
|
|
|
|
комплексной соли |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Медико- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
биологическое |
|
|
|
|
|
|
|
|
|
|
Муравьиная, уксусная, |
|
|
|
Щавелевая, малоновая, янтарная, |
||||
значение |
|
|
|
|
|||||
|
|
масляная, валериановая |
|
|
|
малеиновая, фумаровая кислоты |
|||
|
|
|
|
||||||
|
|
кислоты |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
14 |
|
|
|
|
|
|
|
|
ОРИЕНТИРОВАННАЯ ОСНОВА ДЕЯТЕЛЬНОСТИ.
Инструкция к лабораторно-практическому занятию.
Диссоциация уксусной кислоты
Принцип метода: метод основан на диссоциации карбоновых кислот в воде. Материальное обеспечение: пробирки, пипетки, дистиллированная вода,
раствор уксусной кислоты, лакмус.
Ход работы: Налейте в пробирку 2-3 капли уксусной кислоты, добавьте 2-3 капли воды и исследуйте реакцию раствора на лакмусе. Запишите в тетрадь схему диссоциации.
Устойчивость уксусной кислоты к окислителям.
Принцип метода: метод основан на устойчивости карбоновых кислот к окислителям.
Материальное обеспечение: пробирки, пипетки, дистиллированная вода, раствор уксусной кислоты, раствор серной кислоты.
Ход работы: К раствору уксусной кислоты, полученной в предыдущем опыте, добавьте несколько капель перманганата калия и 2н H2SO4, перемешайте. Что наблюдается? Какой вывод можно сделать из этого опыта, об отношении уксусной кислоты к окислителям?
Открытие уксусной кислоты. Получение комплексной железной соли и разложение ее при кипячении.
Принцип метода: метод основан на получении комплексной железной соли уксусной кислоты.
Материальное обеспечение: пробирки, пипетки, дистиллированная вода, раствор ацетата натрия, 0,1н раствор хлорида железа, газовая горелка.
Ход работы: поместите в пробирку несколько крупинок ацетата натрия CH3COONa. Убедитесь в том, что он не имеет запаха. Добавьте в пробирку 3 капли воды и 2 капли 0,1н FeCl3. Появляется желто-красная окраска в связи с образованием железной соли уксусной кислоты (ацетата железа). Запишите схему реакции.
Фактически ацетат железа частично гидролизуется с образованием комплексного соединения, которое имеет более сложное строение.
Подогрейте раствор до кипения. Сразу происходит гидролиз железной соли, выпадает красно-бурый осадок нерастворимого в воде основного ацетата железа:
CH3 – C |
– O |
|| |
FeOH |
O |
|
2
Раствор, который образуется над осадком, не содержит ионов железа и обесцвечивается.
Описанную реакцию используют в качественном анализе для выделения оксида железа (|||) из раствора. Эту реакцию можно проделать и со свободной
15