Материал: ХИМИЯ_Metodichka_organika
C.Балластовый компонент питания, не расщепляется ферментами ЖКТ;
D.Полисахарид соединительной ткани, находится в стекловидном теле глаза, хрящах, суставной жидкости.
E.Главный резервный полисахарид, в больших концентрациях находится в мышцах и печени.
Эталоны ответов к заданиям:
1 |
– А; |
6 |
– Е; |
2 |
– А; |
7 |
– А; |
3 |
– С; |
8 – С; |
|
4 |
– А; |
9 – С; |
|
5 |
– D; |
10 – . |
|
КРAТКИЕ МЕТОДИЧЕСКИЕ УКАЗАНИЯ ДЛЯ РАБОТЫ НА ПРАКТИЧЕСКОМ ЗАНЯТИИ.
На занятии проверяется подготовка студентов к проведению практического занятия, проводится инструктаж по технике безопасности при работе с химическими реактивами. Под руководством преподавателя студенты решают учебные задания, разбирают и закрепляют теоретический материл: интерпретируют строение и свойства ди- и полисахаридов, записывают реакции, которые иллюстрируют их химические свойства .
Далее, после решения учебных задач, студенты начинают выполнять самостоятельную работу. Используя инструкцию к лабораторно-практическому занятию, они выполняют опыты и оформляют протокол лабораторной работы.
Далее проводится анализ и коррекция самостоятельной работы студентов. Занятие заканчивается тестовым контролем и подведением итогов.
СТРОЕНИЕ И СВОЙСТВА ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ.
АКТУАЛЬНОСТЬ ТЕМЫ:
Гетероциклические соединения – структурные компоненты биологически активных веществ и лекарственных препаратов. Они входят в состав аминокислот (триптофан, гистидин), нуклеиновых кислот, витаминов (никотиновая кислота, цианкобаламин), ферментов и коферментов (НАД, ФАД) и других биологически активных веществ (гемоглобин, хлорофилл, АТФ).
Большое количество лекарственных препаратов содержит в своем составе ядра гетероциклов: анальгетики (амидопирин, анальгин), противотуберкулезные средства (тубазид, фтивазид), антибиотики (пенициллинового и цефалоспоринового рядов) и т.д.
Гетероциклические соединения также входят в состав метаболитов, например, мочевая кислота – продукт превращения пуринових оснований в организме. При нарушении обмена веществ, накопление гетероциклических
51
соединений может стать причиной различных патологических состояний, например, соли мочевой кислоты образуют камни в почках.
Механизмы превращения гетероциклических соединений в организме обусловлены химическими свойствами данных соединений, которые в свою очередь, определяются структурой гетероциклов. Таким образом, умение интерпретировать структуру гетероциклов, прогнозировать их химические свойства и качественно определять присутствие данных соединений в различных медицинских и биологических растворах являются необходимыми для формирования общего понимания биологических превращений в организме и развития навыков практического определения биологически важных веществ.
ЦЕЛИ ОБУЧЕНИЯ:
ОБЩАЯ ЦЕЛЬ:
Уметь интерпретировать строение и свойства гетероциклических соединений как структурных компонентов биологически активных веществ и лекарственных препаратов.
Достижение этой цели обеспечивается решением конкретных задач.
КОНКРЕТНЫЕ ЦЕЛИ.
УМЕТЬ:
1.Интерпретировать строение гетероциклических соединений.
2.Анализировать химические свойства пяти- и шестичленных гетероциклических соединений с учетом количества гетероатомов и ароматичности соединений.
3.Интерпретировать лактим – лактамную и амин – иминную таутомерию гетерофункциональных производных шестичленных гетероциклов.
4.Трактовать биологическое значение гетероциклических соединений как структурных единиц нуклеиновых и аминокислот, витаминов, лекарственных препаратов.
СОДЕРЖАНИЕ ОБУЧЕНИЯ.
Содержание обучения должно обеспечивать достижение целей обучения.
ТЕОРЕТИЧЕСКИЕ ВОПРОСЫ:
1.Классификация гетероциклических соединений по общему количеству атомов в цикле (пяти- и шестичленные), по количеству гетероатомов. Электронное строение и ароматический характер основных представителей гетероциклических пяти- (пиррол) и шестичленных (пиридин) соединений.
2.Строение и химические свойства пятичленных гетероциклов с одним гетероатомом: пиррола и с двумя: имидазол, пиразол, тиазол, оксазол. Биологически активные производные (тетрапиррольные соединения, гистидин, амидопирин, анальгин, тиамин).
3.Строение и химические свойства шестичленных гетероциклов с одним гетероатомом: пиридина и с двумя: пиримидина, и его производных – урацил,
52
тимин, цитозин. Биологически активные производные (никотинамид, пиридоксаль).
4.Строение конденсированного гетероциклического соединения – пурина, и его производных – аденина, гуанина и мочевой кислоты.
5.Лактам – лактимная и амин – иминная таутомерия пиримидиновых и пуриновых оснований.
6.Медико-биологическое значение гетероциклических соединений и их производных.
53
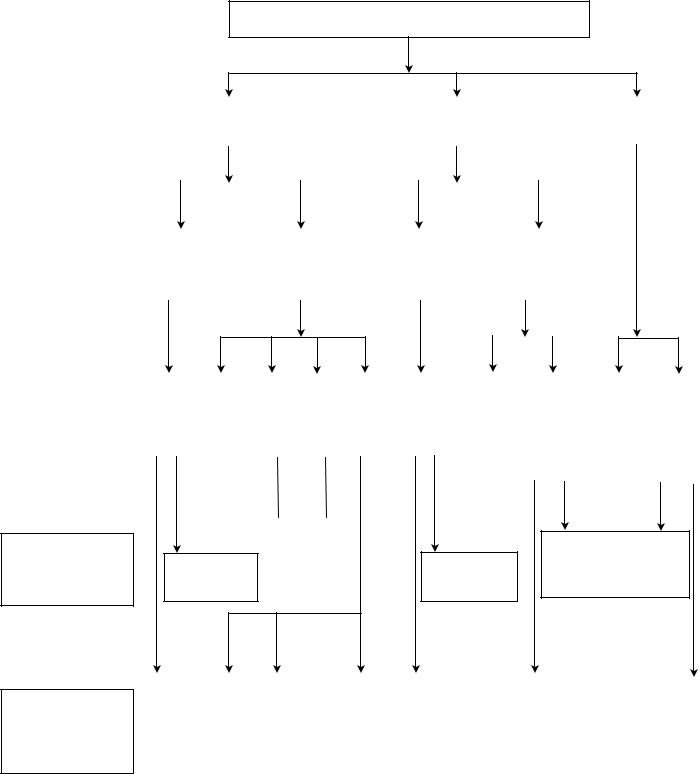
ГРАФ ЛОГИЧЕСКОЙ СТРУКТУРЫ ТЕМЫ:
ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
|
|
ПЯТИ- |
|
|
ШЕСТИ- |
|
|
КОНДЕНСИРО- |
строение, |
|
|
|
|
|
|||
ароматичност |
|
ЧЛЕННЫЕ |
|
|
ЧЛЕННЫЕ |
|
|
ВАННЫЕ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
классификация |
|
|
|
|
|
|
|
|
|
|
|
с одним |
|
с двумя |
|
с одним |
|
|
с двумя |
|
|
с учетом |
|
|
|
|
|
|
||||
|
гетеро- |
|
гетеро- |
|
гетеро- |
|
|
гетеро- |
|
|
количества |
|
|
|
|
|
|
||||
|
атомом |
|
атомами |
|
атом |
|
|
атомами |
|
|
гетероатомов |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
пиррол |
|
пиразол |
|
имидазол |
|
оксазол |
|
тиазол |
||
основные |
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
представители |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
химические свойства, кислотные
изомерия свойства
пиридин |
|
пиримиди |
|
пиримидиновые основания |
|
пурин |
|
пуриновые основания |
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
лактим-лактамная,
основные амин-иминная свойства таутомерия
медикобиологическое значение производных
тетрапиррольные |
|
|
амидопирин, анальгин |
|
гистидин, гистамин |
|
|
|
никотинамид, пиридоксаль |
|
цитозин, урацил, тимин |
|
|
соединения |
|
|
|
тиамин |
|
|
|
аденин, гуанин |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
54
ИСТОЧНИКИ ИНФОРМАЦИИ:
1.Тюкавкина Н.А.,Бауков Ю.И. Биоорганическая химия: Учебник. –
М.:Медицина, 1991.- С.275-304.
2.Рево А.Ю., Зеленкова В.В. Малый практикум по органической химии – М.:Высшая школа, 1980.- С.151-152, 154-156.
3.Лекции по биоорганической химии.
4.Граф логической структуры.
ОРИЕНТИРОВАННАЯ ОСНОВА ДЕЯТЕЛЬНОСТИ
Инструкция к лабораторной работе на практическом занятии.
Реакция антипирина с хлоридом железа (III).
Принцип метода: метод основан на способности гетероциклических соединений образовывать окрашенные внутрикомплексные соли с ионами Fe3+.
Материальное обеспечение: пробирки, пипетки, штатив, шпатель, дистиллированная вода, раствор 0,1М FeCl3, кристаллический антипирин.
Ход работы:
1.В пробирку поместить несколько кристаллов антипирина и растворить в 2-3 каплях дистиллированной воды.
2.Добавить к полученному раствору 1 каплю 0,1М раствора FeCl3.
3.Наблюдать появление окрашивания.
4.Записать формулу антипирина.
Наличие стойкого оранжево-красного окрашивания обусловлено образованием комплексного соединения – ферропирина.
Реакция антипирина с азотистой кислотой.
Принцип метода: метод основан на способности гетероциклических соединений в реакции с азотистой кислотой образовывать нитрозосоединения, обладающие характеристическим окрашиванием.
Материальное обеспечение: пробирки, пипетки, штатив, шпатель, дистиллированная вода, раствор 1М H2SO4, раствор 0,5M NaNO2, кристаллический антипирин.
Ход работы:
1.В пробирку поместить несколько кристаллов антипирина и растворить в 2-3 каплях дистиллированной воды.
2.Добавить к полученному раствору 1 каплю 1М раствора H2SO4.
3.В небольшом количестве поместить в пробирку 0,5M раствор NaNO2.
4.Наблюдать появление окрашивания, исчезающего при длительном хранении.
5.Записать уравнение реакции образования нитрозосоединения.
Появление постепенно исчезающего изумрудно-зеленого окрашивания обусловлено образованием нитрозоантипирина.
55