Материал: guidelines_atherosclerosis_2020

|
Рекомендации |
С 2016 года в РФ одобрены к применению |
зировках 75 и 150 мг в одном шприце-ручке. Оба |
и с 2017 года вошли в список жизненно необходи- |
препарата вводятся подкожно 2 раза в месяц. |
мых и важных лекарственных препаратов ингиби- |
Рекомендации по медикаментозной терапии |
торы PCSK9 – белка, контролирующего экспрессию |
ГХС представлены в таблицах 17 и 18. |
рецепторов к ХС ЛНП на гепатоцитах [40]. Повы- |
В Российских рекомендациях по коррекции на- |
шенные уровень/функция PCSK9 снижают число ре- |
рушений липидного обмена с целью профилакти- |
цепторов ЛНП и увеличивают концентрацию ХС ЛНП |
ки и лечения атеросклероза, выпущенных в 2017 |
в плазме, в то время как снижение уровня/функции |
году, были впервые представлены новые целевые |
PCSK9 вызывает уменьшение ХС ЛНП в плазме |
уровни ХС ЛНП для категории очень высокого |
крови [41]. Ингибиторы PCSK9 в клинических ис- |
ССР [3]. Это было сделано после публикации |
следованиях существенно снижали уровень ХС ЛНП |
результатов двух крупных рандомизированных |
и, соответственно, число ССО у больных с АССЗ. |
клинических исследований (РКИ), в которых было |
В Российской Федерации одобрены к применению |
показано дополнительное снижение риска ССО |
эволокумаб в дозировке 140 мг и алирокумаб в до- |
при снижении уровня ХС ЛНП ниже 1,5 ммоль/л |
Таблица 17.Рекомендации по медикаментозной терапии ДЛП
Рекомендации |
Класс |
Уровень |
|
|
|
|
|
Терапия статинами в максимально переносимых дозах |
I |
А |
|
|
|
|
|
Если на фоне максимально переносимых доз статинов целевой уровень |
I |
В |
|
ХС ЛНП не достигнут, добавить эзетимиб |
|||
|
|
||
|
|
|
|
Для вторичной профилактики у пациентов с очень высоким риском, |
|
А |
|
если целевой уровень ХС ЛНП не достигнут на фоне максимально |
I |
||
переносимых доз статинов и эзетимиба, добавить ингибитор PCSK9* |
|
|
|
|
|
|
|
Для первичной профилактики у пациентов с очень высоким риском, |
|
С |
|
если целевой уровень ХС ЛНП не достигнут на фоне максимально |
I |
||
переносимых доз статинов и эзетимиба, добавить ингибитор PCSK9* |
|
|
|
|
|
|
|
При непереносимости статинов в любой дозе следует рассмотреть |
IIа |
С |
|
назначение эзетимиба |
|||
|
|
||
|
|
|
|
При непереносимости статинов в любой дозе можно рассмотреть |
IIb |
С |
|
добавление ингибитора PCSK9* к эзетимибу |
|||
|
|
||
|
|
|
Примечания: * эволокумаб или алирокумаб. ХС ЛНП – холестерин липопротеидов низкой плотности; PCSK9 – про- протеин-конвертаза субтилизин/кексин типа 9.
Таблица 18. Расчет степени снижения ХС ЛНП при различных вариантах гиполипидемической терапии
Терапия |
Снижение ХС ЛНП в % |
|
|
|
|
Терапия статинами умеренной интенсивности |
≈ 30 |
|
|
|
|
Терапия статинами высокой интенсивности |
≈ 50 |
|
|
|
|
Терапия статинами высокой интенсивности + |
≈ 65 |
|
эзетимиб |
||
|
||
|
|
|
Ингибиторы PCSK9 |
≈ 60 |
|
|
|
|
Ингибиторы PCSK9 + терапия статинами |
≈ 75 |
|
высокой интенсивности |
||
|
||
|
|
|
Ингибиторы PCSK9 + терапия статинами |
≈ 85 |
|
высокой интенсивности |
||
|
||
|
|
|
Аферез липопротеидов |
≈ 75 |
|
|
|
Примечания: ХС ЛНП – холестерин липопротеидов низкой плотности; PCSK9 – пропротеин-конвертаза субтилизин/ |
|
кексин типа 9. |
19 |
|
|
|
|
¹1 2020 |
|
|
|

Рекомендации
за счет добавления к статинам гиполипидемических препаратов других классов.
В исследовании IMPROVE-IT (Improved Reduction of Outcomes: Vytorin Efficacy International Trial) 18144 больных, госпитализированных по поводу ОКС и имевших относительно невысокий уровень ХС ЛНП (1,3–3,2 ммоль/л или 50–125 мг/дл), получали монотерапию симвастатином или его комбинацию с эзетимибом в течение 7 лет. Через 1 год наблюдения средний уровень ХС ЛНП в группе эзетимиба составил 1,4 ммоль/л, что было на 0,4 ммоль/л меньше, чем в группе монотерапии симвастатином. В группе комбинированного лечения наблюдали значимое снижение количества смертельных исходов от сердечно-сосудистых заболеваний, инфаркта миокарда, госпитализации по поводу нестабильной стенокардии, коронарной реваскуляризации и инсульта на 6,4% (ОР=0,936; 95%, ДИ=0,89–0,99, р=0,016), снижение абсолютного риска на 2,0% [42].
Исследование FOURIER (Further cardiovascular OUtcomes Research with PCSK9 Inhibition in subjects
with Elevated Risk) включало 27 564 |
пациента |
с атеросклеротическим поражением |
различных |
сосудистых бассейнов: 22 040 пациентов (81%) в прошлом перенесли инфаркт миокарда, у 5 330 (19%) в анамнезе был ишемический инсульт и у 3 640 (13%) – периферический атеросклероз. Пациенты находились на адекватной гиполипидемической терапии: 69,2% получали статины в режиме высокой интенсивности и 30,4% – в режиме умеренной интенсивности, у 5,1% дополнительно к статинам назначали эзетимиб. Участники, рандомизированные в группу активного лечения, получали эволокумаб подкожно в дозе 140 мг 1 раз в 2 недели или 420 мг в месяц, тогда как пациентам в группе контроля на протяжении исследования подкожно вводили плацебо [43]. Медиана наблюдения в исследовании составила 2,2 года. В группе эволокумаба уровень ХС ЛНП снизился на 59% с 2,40 ммоль/л до 0,78 ммоль/л, а риск сердечно-сосудистых осложнений снизился на 15–20% по сравнению с группой плацебо. На
основании этих данных был предложен пересмотр целевого уровня ХС ЛНП для лиц очень высокого сердечно-сосудистого риска [44, 45].
Позднее исследование ODYSSEY OUTCOMES (Evaluation of Cardiovascular Outcomes After an Acute Coronary Syndrome During Treatment With Alirocumab) с участием 18924 пациентов с перенесенным ОКС показало, что алирокумаб по сравнению с плацебо значимо снижал риск ССО – на 15% [46].
Таким образом, с учетом данных, полученных в перечисленных клинических исследованиях, следует считать целесообразным и безопасным лечить пациентов очень высокого ССР до достижения целевого уровня ХС ЛНП < 1,4 ммоль/л с целью профилактики ССО.
Остаточный риск и его связь с триглицеридами
Исследователями было замечено, что, несмотря на достижение целевого уровня ХС ЛНП,
уряда пациентов сохраняется риск ССО. Такое явление определяется как остаточный риск. Наиболее частыми причинами остаточного риска являются высокий уровень ТГ и низкий уровень ХС ЛВП в плазме крови.
По данным эпидемиологического Фремингемского исследования, уровень ТГ более 1,7 ммоль/л достоверно связан с более высоким риском развития ССО [47]. Вместе с тем риск ССО у пациентов с ХС ЛВП < 1,0 ммоль/л был на 64% выше, чем
упациентов с ХС ЛВП ≥1,4 ммоль/л [48]. Повышенные уровни ТГ и низкий уровень ХС ЛВП увеличивают риск сердечно-сосудистых осложнений
упациентов с уже достигнутым целевым уровнем ХС ЛНП [49]. Показано, что у пациентов с ТГ более 2,3 ммоль/л и ХС ЛВП менее 0,8 ммоль/л риск ССО увеличивается в 10 раз по сравнению с пациентами с оптимальными значениями ТГ и ХС ЛВП [49, 50].
По данным NCEP-ATP III, нормальное значение концентрации ТГ составляет менее 1,7 ммоль/л,
промежуточно-высокий уровень ТГ находится в пределах от 1,7 до 2,3 ммоль/л, ГТГ – от 2,3 до 5,6 ммоль/л, выраженная ГТГ – более 5,6 ммоль/л [51]. Среди первичных, наследственных причин повышения ТГ выделяют варианты, связанные с гиперпродукцией ЛОНП, дефектом гидролиза ТГ, дефектом клиренса ремнантов ТГ в печени. Частым клиническим проявлением семейной ГТГ является острый панкреатит [52].
Вторичная ГТГ может быть обусловлена инсу-
линорезистентностью и связанными с ней состояниями – СД 2 типа, метаболическим синдромом и ожирением. При этих состояниях дислипидемия характеризуется высоким уровнем ТГ и ЛОНП и низким уровнем ХС ЛВП [50]. По данным исследования NHANES (The National Health and Nutrition Examination Survey), атерогенная ДЛП (повышенный уровень ТГ и низкий уровень ХС ЛВП) отмечается у 62% кардиологических больных [53]. Среди 22063 пациентов, получающих
20
АТЕРОСКЛЕРОЗ И ДИСЛИПИДЕМИИ

Рекомендации
монотерапию статинами в Европе и Канаде, повышенный уровень ТГ и низкий уровень ХС ЛВП наблюдались у 38,8% и 26% соответственно [54]. Весьма частыми причинами повышения уровня ТГ могут быть ХБП, гипотиреоз, избыточное употребление алкоголя, системная красная волчанка, длительный прием кортикостероидов [55].
Преобладающим механизмом, лежащим в основе атеросклеротического процесса при ГТГ, является гиперпродукция в печени частиц ЛОНП. Отмечено, что при атерогенной смешанной дислипидемии происходит формирование в большом количестве мелких, плотных ЛНП с высоко атерогенными свойствами [56].
В связи с этим у пациентов с ожирением и СД 2 типа значительно большую информацию для оценки ССР несёт ХС, не связанный с ЛВП (ХС неЛВП), рассчитываемый по формуле: ОХС – ХС ЛВП. Показатель ХС неЛВП имеет более высокий уровень прогностической значимости по сравнению с ХС ЛНП у пациентов с метаболическим синдромом и СД [57].
Обоснованную позицию в вопросе о роли ТГ и ХС ЛВП в атерогенезе показали результаты исследования ACCORD-LIPID (The Action to Control Cardiovascular Risk in Diabetes (ACCORD)-Lipid trial) (субанализ данных пациентов с повышенным уровнем ТГ) и исследования REDUCE-IT (The Reduction of Cardiovascular Events with Icosapent Ethyl–Intervention Trial) [58, 59].
Терапия ГТГ и атерогенной дислипидемии
Современные рекомендации при выявлении ГТГ нацеливают на назначение статинов, а при недостижении целевого уровня ТГ – на добавление к терапии фибратов и n-3-ПНЖК [5, 59]. Механизм действия фибратов заключается в активации ядерных альфа-рецепторов пероксисом (РРARĮ). Основная роль PPARĮ-рецепторов заключается в регуляции метаболизма липидов и липопротеидов, воспаления, функции эндотелия. В России из фибратов зарегистрирован фенофибрат. Назначение фенофибрата снижает уровень ТГ на 50% и повышает уровень ХС ЛВП на 10–30% [60, 61].
Втаблице 19 приводятся механизмы действия
исравнительная эффективность фенофибрата, статинов и эзетимиба по влиянию на липидный профиль.
Помимо снижения уровня ТГ фенофибрат снижает концентрацию мочевой кислоты в среднем на 25%, фибриногена – на 21%, С-реактивного
белка – на 34% [60, 61].
Тактика медикаментозной терапии снижения уровня ТГ представлена в таблице 20 и на рисунке 2.
Этиловые эфиры n-3-ПНЖК эффективно снижают концентрацию ТГ и риск сердечно-сосуди- стых событий. Недавно завершилось исследование REDUCE-IT с участием 8179 пациентов, которое продемонстрировало снижение ОР развития неблагоприятных сердечно-сосудистых событий на 25% (р < 0,001) в группе пациентов, принимавших n-3- ПНЖК в дозе 4 г/сут в сравнении с плацебо [59].
Таблица 19.Сравнение эффективности фенофибрата, статинов и эзетимиба [42, 51, 60, 61, 62, 63]
|
Фенофибрат |
Статины |
Эзетимиб |
|
Механизм действия |
|
|
|
|
активирует |
ингибируют фермент |
селективно ингибирует |
||
|
работу клеточных |
абсорбцию холестерина |
||
|
ГМГ-КоА-редуктазу |
|||
|
PPARĮ-рецепторов |
в кишечнике |
||
|
|
|||
|
|
|
|
|
Снижение |
5–20% |
18–55% |
15–30% |
|
концентрации ХС ЛНП |
||||
|
|
|
||
|
|
|
|
|
Снижение уровня |
20–50% |
7–20% |
не изменяет |
|
триглицеридов |
||||
|
|
|
||
|
|
|
|
|
Повышение уровня |
10–20% |
5–15% |
3–5% |
|
ХС ЛВП |
||||
|
|
|
||
|
|
|
|
|
Увеличение размеров |
50% |
нет |
нет |
|
частиц ЛНП |
||||
|
|
|
||
|
|
|
|
Примечания: ХС ЛНП – холестерин липопротеидов низкой плотности; ХС ЛВП – холестерин липопротеидов высокой плотности.
21
¹1 2020
Рекомендации
Таблица 20.Рекомендации по лекарственной терапии гипертриглицеридемии [64]
Рекомендации |
Класс |
Уровень |
|
|
|
|
|
При уровне ТГ > 2,3 ммоль/л начать терапию статинами |
I |
B |
|
|
|
|
|
С целью вторичной профилактики у пациентов, достигших целевого |
IIa |
B |
|
уровня ХС ЛНП, но с ТГ > 2,3 ммоль/л, добавить фенофибрат |
|||
|
|
||
|
|
|
|
У больных высокого/очень высокого риска с ТГ 1,5–5,6 ммоль/л, |
|
|
|
несмотря на терапию статинами, добавить фенофибрат и при |
IIа |
B |
|
недостаточном эффекте или при непереносимости фенофибрата |
|||
|
|
||
добавить n-3-ПНЖК 2 г u2 раза в день |
|
|
|
|
|
|
|
У больных высокого риска, достигших целевого уровня ХС ЛНП и ТГ |
|
C |
|
> 2,3 ммоль/л, добавить фенофибрат; при его непереносимости |
IIa |
||
добавить n-3-ПНЖК 2 г × 2 раза в день |
|
|
|
|
|
|
Примечания: ТГ – триглицериды; ХС ЛНП – холестерин липопротеидов низкой плотности; ПНЖК – полиненасыщенные жирные кислоты.
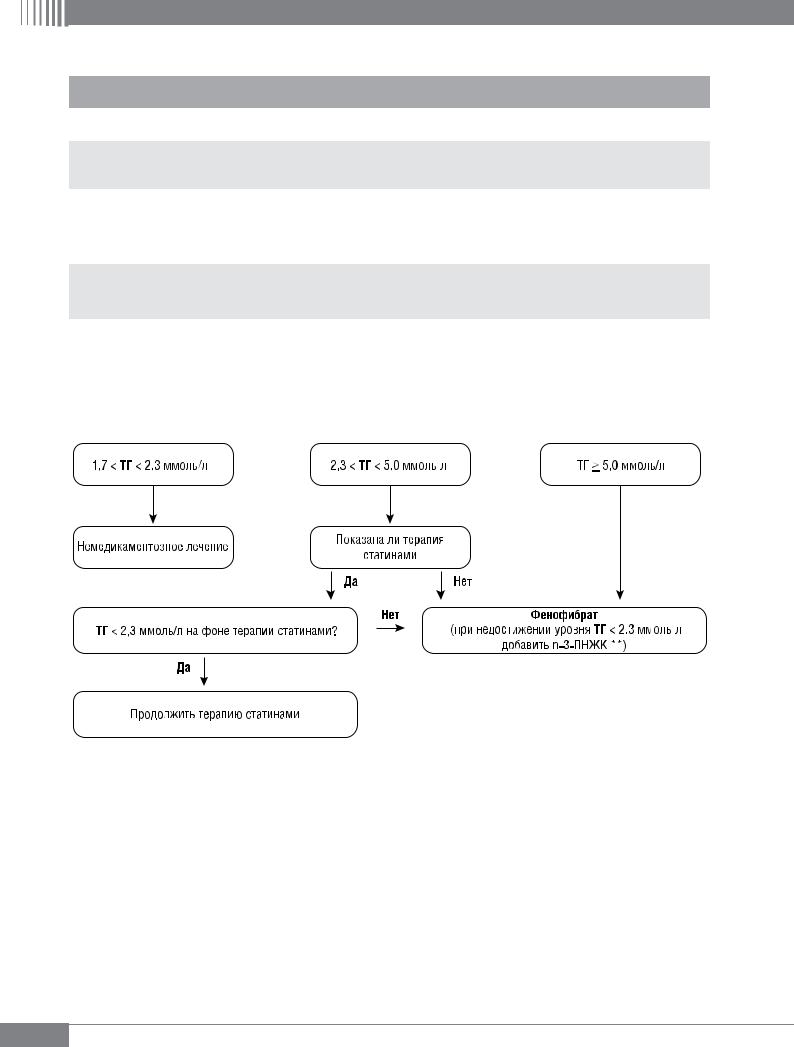
Рис. 2. Алгоритм лечения ГТГ [65, 66]
Примечания: с учетом клинического фенотипа пациента.
** n-3-ПНЖК – этиловые эфиры омега-3-полиненасыщенных жирных кислот в дозе 2–4 г/сут. При выраженной гипертриглицеридемии рассмотреть вопрос о направлении для экстракорпоральной терапии (плазмаферез).
ТГ – триглицериды.
22
АТЕРОСКЛЕРОЗ И ДИСЛИПИДЕМИИ
