Материал: Физика1
![]()
С помощью этого уравнения давление p газа может быть выражено соотношением
где – плотность газа; n – концентрация его молекул. Записанное для одного моля газа основное уравнение принимает следующий вид:
где представляет собой среднюю кинетическую энергию хаотического движения молекул газа; NА – число Авогадро.
Внутренняя энергия идеального газа. Закон равномерного распределения энергии по степеням свободы.
Внутренней энергией U системы называется энергия, зависящая только от термодинамического состояния системы. Она определяется характером движения и взаимодействия частиц, входящих в систему, и включает в себя: а) кинетическую энергию теплового движения всех частиц системы;
б) потенциальную энергию взаимодействия частиц системы; в) энергию электронов в атомах и внутриядерную энергию этих атомов. В рассматриваемых термодинамических системах изменением энергии электронов и внутриядерной энергии можно пренебречь и оценивать внутреннюю энергию системы как сумму кинетической энергии теплового движения частиц и потенциальной энергии их взаимодействия.
Внутренняя энергия является функцией термодинамического состояния системы, т. е. зависит от ее термодинамических параметров и не зависит от того, каким образом система пришла к этому состоянию. При переходе системы из одного состояния в другое изменение внутренней энергии U U 2 U1 не зависит от характера этого перехода. В случае кругового процесса, при котором система возвращается в исходное состояние, U 0 . Внутренняя энергия идеального газа включает в себя только кинетическую энергию теплового движения его молекул, так как взаимодействие между молекулами такого газа пренебрежимо мало:
![]()
С учетом того, что средняя кинетическая энергия теплового движения молекул одноатомного однородного газа

Так как число молекул , внутренняя энергия идеального одноатомного газа равна
а ее изменение
Очевидно, что внутренняя энергия идеального газа является функцией абсолютной температуры Т, и ее изменение определяется только изменением температуры T.
Используя уравнение состояния идеального
газа
,
изменение внутренней энергии можно
представить в виде
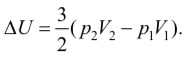
Приведенные формулы справедливы для одноатомного идеального газа. Для многоатомного идеального газа внутренняя энергия зависит еще от одного параметра – числа степеней свободы.
Число степеней свободы молекулы – число независимых величин, полностью определяющих ее положение в пространстве.
Молекулу одноатомного газа (гелий, ксенон и др.) можно рассматривать как материальную точку, ее положение в пространстве характеризуется тремя декартовыми координатами, которым соответствуют три степени свободы поступательного движения, которым соответствует кинетическая энергия этого движения.
Молекула двухатомного газа (водород, кислород, азот) в первом приближении рассматривается как совокупность двух жестко связанных материальных точек. Эта молекула кроме трех степеней свободы поступательного движения имеет еще две степени свободы вращательного движения – вокруг двух осей, перпендикулярных оси молекулы, в них запасается кинетическая энергия вращения. Вращение вокруг третьей оси, проходящей через два атома молекулы, не меняет расположения последней в пространстве, при таком вращении энергия вращения не запасается, так как момент инерции молекулы относительно этой оси равен нулю. Таким образом, двухатомная молекула обладает пятью степенями свободы.
Трехатомная (углекислый газ, вода) и многоатомная нелинейные молекулы имеют шесть степеней свободы: три поступательные и три вращательные.
Естественно, жесткой связи между атомами в молекуле не существует. Поэтому необходимо учитывать также степени свободы колебательного движения, при котором изменяется расстояние между атомами. Отметим, что двухатомная молекула имеет одну колебательную степень свободы.
В классической статистической физике справедлив закон Больцмана о равномерном распределении энергии по степеням свободы молекул: для статистической системы, находящейся в состоянии термодинамического равновесия, на каждую поступательную и вращательную степени свободы приходится кинетическая энергия, в среднем равная kT/2, а на каждую колебательную степень свободы – в среднем равная kT.
Колебательная степень свободы имеет вдвое большую энергию, так как на нее приходится не только кинетическая энергия, но и потенциальная, а средние значения этих энергий одинаковы.
Таким образом, средняя энергия молекулы
![]() ,
,
где i – суммарное число степеней свободы молекулы i = iпост + iвращ + 2iколеб. Так как в идеальном газе потенциальная энергия взаимодействия молекул равна нулю, его внутренняя энергия равна сумме энергий молекул, т. е.
Для 1 моля газа N = NA, и его внутренняя энергия
Если в газе содержится ν = N/NA молей, то

Используя уравнение состояния идеального газа, изменение внутренней энергии можно представить в виде
Работа в термодинамике. Выражения для работы при изопроцессах идеального газа.
Работа в термодинамике – это форма изменения внутренней энергии системы, связанного с изменением объема данной системы и расположения ее частей относительно друг друга.
Различают работу А, которая совершается системой над внешними телами, и работу А, которая совершается внешними телами над системой. Эта работа равны по модулю и противоположна по знаку: А = – А . Работа А газа, совершаемая в изобарном процессе, Ар(V2 V1)pV, где р – давление газа; V V2 V1 – изменение его объема.
При расширении газа совершается положительная работа против внешних сил ( V 0). При сжатии газа совершается отрицательная работа (V0).
Работу расширения газа можно выразить
и другой формулой, применив уравнение
Менделеева–Клапейрона для двух
состояний газа – до изобарного
расширения
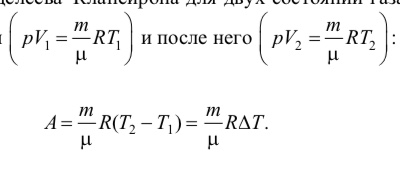 и
после него
:
и
после него
:
С помощью последней формулы можно установить физический смысл универсальной газовой постоянной R: универсальная газовая постоянная R численно равна работе, которую совершает в изобарном процессе 1 моль идеального газа при повышении его температуры на 1 К.
При изохорном процессе (V = const, V 0) объем газа остается постоянным, и работа газом не совершается: А = 0.
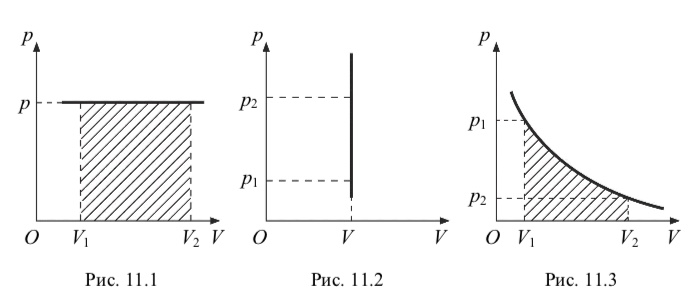
Работе газа А можно дать простое геометрическое истолкование: на графике зависимости давления р от объема V при изобарическом процессе работа, которую совершает газ при изменении объема от V1 до V2, численно равна площади прямоугольника с основанием V2 – V1 и высотой р = const (рис. 11.1). В частности, график зависимости р = f(V) для изохорного процесса (рис. 11.2) подтверждает, что работа газа равна нулю.
Работа расширения при любом процессе измеряется площадью на pV-диаграмме, ограниченной кривой процесса p = f(V), осью абсцисс и вертикальными прямыми V = V1 и V = V2 (рис. 11.1–11.3), т. е. интегралом

Из этой формулы следуют приведенные выше выражения работы газа, совершаемой в изобарном процессе (рис. 11.1). В изохорном (рис. 11.2) A = 0, поскольку dV = 0. В изотермическом процессе (рис. 11.3), используя уравнение Менделеева–Клайперона, получаем
При круговом процессе (цикле) (рис. 11.4) на участке 1а2 газ расширяется и совершает положительную работу А1а2, численно равную площади под указанной кривой. На участке 2б1 газ сжимается и производит отрицательную работу А2б1, численно равную площади под кривой 2б1. Суммарная работа газа за цикл численно равна разности этих двух площадей (А = А1а2 – А2б1), т. е. площади, охватываемой замкнутой кривой 1а2б1. Эта работа записывается в виде кругового интеграла
![]()
Если бы газ переходил из состояния 1 в состояние 2 по пути 1б2, а возвращался в исходное состояние по пути 2а1, то работа газа, совершенная за цикл, оказалась бы отрицательной. Таким образом, работа за цикл численно равна площади, охватываемой кривой цикла на диаграмме рV. Работа положительна, если состояние газа изменяется в цикле по часовой стрелке, и отрицательна, если изменение происходит против часовой стрелки.
Первое начало термодинамики. Количество теплоты. Теплоемкость идеального газа. Уравнение Майера.
Теплообменом называется процесс передачи энергии от одного тела другому без совершения работы. Различают следующие виды теплообмена: теплопроводность, конвекция, лучистый теплообмен.
Количеством теплоты Q называется энергия, переданная телу в результате теплообмена. При теплообмене часть внутренней энергии одного тела переходит во внутреннюю энергию другого.
Теплоемкостью тела называется величина, численно равная количеству теплоты, которое необходимо сообщить телу, чтобы изменить его температуру на один градус:
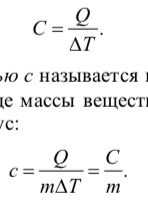
Удельной теплоемкостью с называется количество теплоты, которое необходимо сообщить единице массы вещества для того, чтобы изменить его температуру на один градус:
Молярной теплоемкостью называется количество теплоты, которое необходимо сообщить одному молю вещества для того, чтобы изменить его температуру на один градус.
Молярная и удельная теплоемкость связаны между собой соотношением С с. Количество теплоты, необходимое для нагревания вещества массой т (или числом молей ) на Т градусов, можно определить по формуле QcmT CT.
Если система тел изолирована, то в соответствии с законом сохранения энергии энергия такой системы не изменяется, т. е. U = const. Если в такой системе происходят процессы, при которых работа не совершается, то изменение внутренней энергии любого тела системы равно количеству теплоты, отданной или полученной этим телом: Ui Qi. Суммируя подобные выражения для всех тел системы, получаем
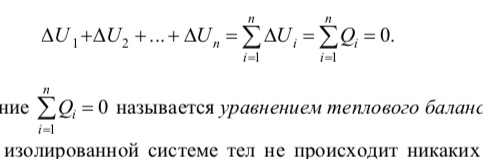 Уравнение
называется
уравнением теплового баланса.
Уравнение
называется
уравнением теплового баланса.
Если в изолированной системе тел не происходит никаких превращений энергии кроме теплообмена, то количество теплоты, отданное телами, внутренняя энергия которых уменьшается, равно количеству теплоты, полученному телами, внутренняя энергия которых увеличивается.
Закон сохранения энергии, распространяемый как на механические, так и на тепловые явления, называется первым законом (началом) термодинамики: изменение внутренней энергии системы равно сумме работы, совершаемой над системой внешними силами, и количества теплоты, полученного системой: U A Q. Так как работа внешних сил А и работа, совершаемая системой над другими телами А, равны и противоположны по знаку ( A A) , имеем Q U A, т. е. количество теплоты, сообщенное системе, идет на приращение внутренней энергии системы и на совершение этой системой работы над внешними телами.
Необходимо подчеркнуть, что совершенная работа А и переданное количество теплоты Q в отличие от U зависят не только от начального и конечного состояний системы, но и от процесса, с помощью которого происходило изменение состояния.
В этой связи следует отметить, что теплоемкость вещества также зависит от процесса, в котором происходит передача теплоты. Различают теплоемкость при постоянном объеме СV и постоянном давлении Cp, если в процессе нагревания вещества его объем или давление постоянны.
Согласно первому началу термодинамики для 1 моля идеального газа получаем
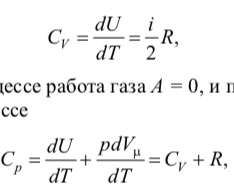
так как в изохорном процессе работа газа A = 0, и поэтому Q = ΔU.
В изобарном процессе
поскольку в этом процессе согласно уравнению Менделеева–Клайперона
pVμ = RT, и, следовательно, для 1 моля идеального газа,
pdVμ = RdT.
Уравнение, связывающее Сp, CV и R, называется уравнением Майера.
Отметим, что для любых веществ Cp > CV, так как в процессе при постоянном давлении часть подводимой теплоты дополнительно расходуется на совершение работы по расширению тела (газа).
При изохорном процессе (V = const) газ работу не совершает, и все количество теплоты Q расходуется только на увеличение внутренней энергии газа:
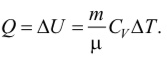
При изобарном процессе (р = const) количество теплоты, подводимое к газу, Q 0 , расходуется как на увеличение внутренней энергии (U 0), так и на работу расширения ( A 0) , которую совершает газ против внешнего давления: Q U A. Поскольку A pV RT , а изменение внутренней энергии газа
![]() ,
имеем
При
изотермическом процессе (Т =
const) температура остается постоянной
(T
0) , внутренняя энергия газа при этом не
меняется (U
0) , поэтому вся подводимая теплота идет
на работу, совершаемую газом: Q = A.
,
имеем
При
изотермическом процессе (Т =
const) температура остается постоянной
(T
0) , внутренняя энергия газа при этом не
меняется (U
0) , поэтому вся подводимая теплота идет
на работу, совершаемую газом: Q = A.