Материал: Физика1
Адиабатический процесс. Уравнение Пуассона.
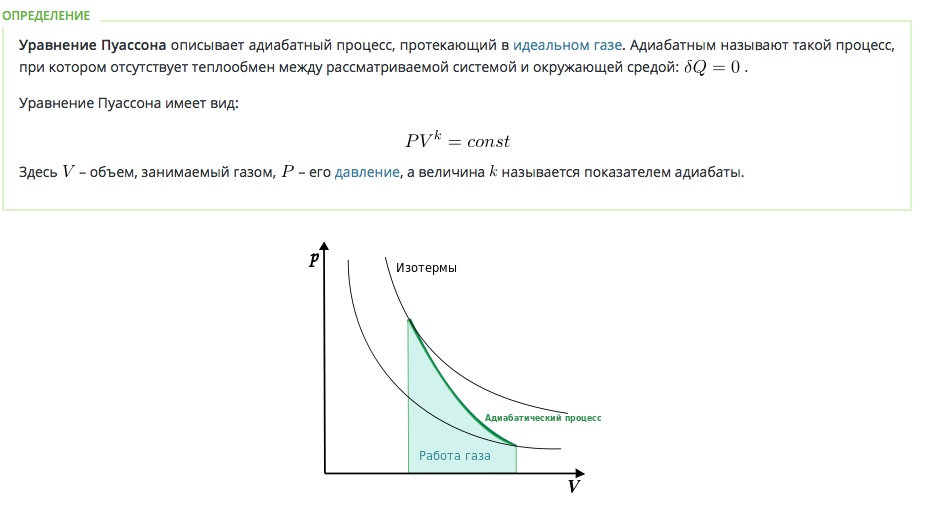
Адиабатическим процессом называется процесс, протекающий в системе тел без теплообмена с окружающей средой.
На диаграмме в координатах p, V (рис. 11.5) адиабатический процесс изображается кривой, которая называется адиабатой. На этой диаграмме приведена также изотерма, которая соответствует температуре начального состояния газа. Из сравнения адиабаты и изотермы следует, что при адиабатическом сжатии газа его давление возрастает быстрее, чем при изотермическом. Это связано с тем, что увеличение давления происходит вследствие уменьшения объема газа и возрастания температуры.
Так как адиабатический процесс протекает без теплообмена (Q = 0), первый закон термодинамики для него записывается следующим образом: U A = 0. Отсюда следует, что Q=0, т. е. в адиабатическом процессе газ совершает работу за счет убыли внутренней энергии системы.
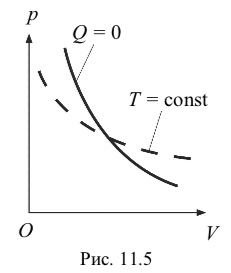
Если газ расширяется адиабатически (A > 0, U 0), то происходит его охлаждение (T 0 ), если газ адиабатически сжимается (A 0, U 0), то он нагревается (T 0).
Практически адиабатический процесс осуществляется при достаточно быстром расширении или сжатии газа таким образом, что теплообмен между ним и внешней средой не успевает произойти.

Принцип действия теплового двигателя и его к.П.Д.
Тепловой двигатель представляет собой устройство, в котором рабочее тело (газ) совершает работу в ходе циклического процесса благодаря теплоте, полученной извне. Для того чтобы работа за цикл была положительной, давление, а следовательно, и температура газа при расширении должны быть выше, чем при сжатии. Для этого в тепловом двигателе имеется нагреватель – тело, от которого при расширении газу сообщается теплота Q1, и холодильник – тело, которому в процессе сжатия газ отдает теплоту Q2. Схема теплового двигателя показана на рис. 11.6.
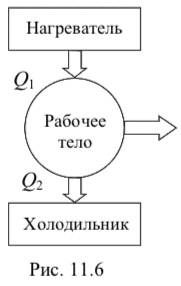
Так как изменение внутренней энергии при возвращении рабочего тела в первоначальное состояние равно нулю, первое начало термодинамики для Q2 цикла имеет вид А = Q1 – Q2.
Коэффициентом полезного действия (КПД) теплового двигателя называется величина, равная отношению совершаемой за цикл работы А к количеству теплоты Q1, переданному рабочему телу:
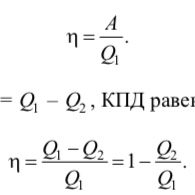
С учетом того, что А=Q1 –Q2, КПД равен
Из определения КПД следует, что он не может быть больше единицы.
Цикл Карно и его к.П.Д.
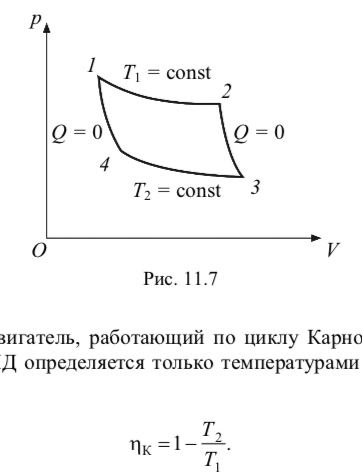
Из всех возможных циклов максимальный коэффициент полезного действия имеет цикл Карно (рис. 11.7).
Французский ученый С. Карно рассмотрел идеализированный цикл тепловой машины, рабочим телом которой является идеальный газ, находящийся между нагревателем с температурой T1 и холодильником с температурой Т2. Этот цикл составлен из определенной последовательности обратимых процессов (см. рис. 11.7): изотермического расширения 1→2, адиабатического расширения 2→3, изотермического сжатия 3→4 и адиабатического сжатия 4→1.
 Тепловой
двигатель, работающий по циклу Карно,
называется идеальным, и его КПД
определяется только температурами
нагревателя Т1 и холодильника
Т2:
Тепловой
двигатель, работающий по циклу Карно,
называется идеальным, и его КПД
определяется только температурами
нагревателя Т1 и холодильника
Т2:
Коэффициент полезного действия любого теплового двигателя, работающего с нагревателем температурой Т1 и холодильником температурой Т2, всегда меньше КПД идеального теплового двигателя, работающего при тех же температуре нагревателя и холодильника ( К).
Обратимые и необратимые процессы. Энтропия идеального газа. Статистический смысл энтропии.
Обратимым термодинамическим процессом называется термодинамический процесс, допускающий возможность возвращения системы в первоначальное состояние без того, чтобы в окружающей среде остались какие-либо изменения. Необходимым и достаточным условием обратимости термодинамического процесса является его равновесность. Необратимым термодинамическим процессом называется термодинамический процесс, не допускающий возможности возвращения системы в первоначальное состояние без того, чтобы в окружающей среде остались какие-либо изменения. Все реальные процессы протекают с конечной скоростью. Они сопровождаются трением, диффузией и теплообменом при конечной разности между температурами системы и внешней среды. Следовательно, все они неравновесны и необратимы. Всякий необратимый процесс в одном направлений (прямом) протекает самопроизвольно, а для осуществления его в обратном направлении так, чтобы система вернулась в первоначальное состояние, требуется компенсирующий процесс во внешних телах, в результате которого состояния этих тел .оказываются отличными от первоначальных. Например, процесс выравнивания температур двух соприкасающихся различно нагретых тел идет самопроизвольно, т. е. не связан с необходимостью одновременного существования каких-либо процессов в других (внешних), телах. Однако для осуществления обратного процесса увеличения разности температур тел до первоначальной нужны компенсирующие процессы во внешних телах, обусловливающие, например, работу холодильной машины.
Кроме внутренней энергии существуют и другие функции состояния. Важнейшая из них – энтропия S, введенная Р. Клаузиусом в 1865 г. Ее изменение ΔS определяется уравнением

где ΔQ – теплота, полученная телом; T – температура теплоотдающего тела. При переходе идеального газа из состояния, характеризуемого объемом V1, температурой Т1 и давлением Р1, в состояние с термодинамическими параметрами V2, Т2 и Р2 для ΔS, используя первое начало термодинамики и уравнение Менделеева–Клапейрона, нетрудно получить
В термодинамике доказывается, что в обратимых процессах (могут происходить как в прямом, так и обратном направлении, причем при возвращении системы в исходное состояние в ней и окружающей среде не происходит никаких изменений) ΔS = 0, в необратимых – ΔS >0.
На этих свойствах энтропии основано второе начало термодинамики (или закон возрастания энтропии): в процессах, происходящих в замкнутой системе, энтропия системы не убывает (в необратимых она возрастает, в обратимых – постоянна).
Первое начало термодинамики – это закон сохранения энергии, из которого следует, какие процессы возможны (например, возможны и прямые, и обратные процессы, но при условии выполнения закона сохранения энергии). Второе начало указывает направление протекания термодинамических процессов: из возможных процессов выбираются те, которые реально осуществимы.
В статистической физике энтропия связывается с термодинамической вероятностью состояния системы. Термодинамическая вероятность W – это число способов (микросостояний), с помощью которых может быть реализовано данное состояние макроскопической системы (по определению W ≥ 1). Согласно Больцману S k lnW, где k – постоянная Больцмана. Второе начало термодинамики теперь можно сформулировать так: процессы в замкнутой системе идут от менее вероятных к более вероятным до тех пор, пока вероятность системы W не станет максимальной.