Материал: Фарм производство БАР
большинства актуальных возбудителей инфекционных болезней. Началась гонка по созданию все новых и новых антибактериальных препаратов, большинство из которых быстро становились малоэффективными. В настоящее время описано более 6000 антибиотиков. Однако только 2–3 % известных антибиотиков применяется на практике. Остальные из-за их токсичности, инактивации в организме и других причин не используются. Большую часть выпускаемых антибиотиков составляют пенициллины, цефалоспорины, тетрациклины, эритрин, стрептомицин.
С учетом этих данных стали появляться высказывания об отказе от производства и применения антибиотиков. Но в настоящее время пока нет других надежных лекарственных препаратов, которыми можно заменить антибиотики. Поэтому их продолжают выпускать и применять во врачебной практике. Наряду с выпуском известных антибиотиков ведутся поиски новых, более эффективных препаратов.
Необходимо остановиться еще на одном вопросе. Весьма перспективной является липосомальная форма антибиотика, открывающая значительные возможности для воздействия на внутриклеточных возбудителей.
При лечении инфекционных заболеваний липосомы применяют в качестве носителей антимикробных агентов – антибиотиков различной структуры. Преимуществом липосомальной формы антибиотиков для ле-
чения бактериальной контаминации является:
антибиотики, инкапсулированные в липосомы не подвергаются действию экзогенных гидролаз, что является одним из путей борьбы с резистентностью к антибиотикам;
при попадании в организм липосомальные лекарственные формы антибиотиков обладают выраженным пролонгированным действием по сравнению со свободными формами антибиотиков;
липосомы, содержащие антибиотики сливаются с наружной мембраной клеточной стенки бактерий, проникая во внутрь бактериальной клетки, что приводит к её гибели.
78
липосомы, содержащие антибиотики приводят к снижению проявления побочных эффектов по сравнению со свободными формами антибиотиков;
антибиотики, инкапсулированные в липосомы проявляют большую антимикробную активность по сравнению со свободными формами антибиотиков.
За прошедший период изучения липосомальных форм антибиотиков были изучены липосомы, содержащие: адриамицин, амикацин, амфотерицин, ампицилин, азаитромицин, блеомицин, доксициклин, доксорубицин, вакомицин, стрептомицин, изониазид, гентамицин, канамицин, тобрамицин, рифампицин, цефалин и многие другие. Созданы липосомальные коммерческие препараты содержащие антибиотики: доксорубицин, даунорубицин, амфотерицин В, тобрамицин, амикацин и ряд других. Для большинства антибиотиков установлена возможность преодоления резистентности при их использовании в липосомальной форме. По нашему мнению,
вряде случаев, липосомальная форма антибиотиков позволит расширить их применение в клинике.
Таким образом, развитие исследований в биотехнологии, создание новых штаммов-продуцентов антибиотиков, включая рекомбинантные, производство высокоэффективного оборудования даст возможность пополнить номенклатуру антибиотиков и их лекарственных форм.
79
Контрольные вопросы
1.Описать историю открытия антибиотиков.
2.Классификация антибиотиков по спектру действия и химической структуре.
3.Классификация антибиотиков по молекулярному механизму дей-
ствия.
4.Назовите бактерии продуценты антибиотиков на примере пенициллина.
5.Как определяют антагонистический спектр и активность антибио-
тиков?
6.Какие требования предъявляют к ферментерам для производства антибиотиков?
7.Охарактеризуйте основные технологические этапы получения антибиотиков и методы их очистки.
8.Условия культивирования продуцентов антибиотиков (состав питательных сред, температура, аэрация и др.).
9.Схема производства гентамицина.
10.Как получают и для чего используют 6-АПК?
11.Почему существует необходимость в создании нескольких поколений антибиотиков?
12.Схема производства пенициллина. Какие формы пенициллина сегодня используются в медицине?
13.Схема производства стрептомицина.
14.Физико-химические и фармакологические свойства антибиотика.
15.Какие основные лекарственные формы антибиотиков?
16.Какие методы применяют для очистки антибиотиков?
17.Влияние состава питательных сред и предшественника на эффективность синтеза антибиотика штаммами продуцентами.
18.Чем объясняется необходимость создания новых антибиотиков?
19.Что означает резистентность бактерий?
80
ГЛАВА 3. ТЕХНОЛОГИЯ ПОЛУЧЕНИЯ ГЕПАРИНОВ
3.1.Нефракционированные гепарины: выделение и характеристика
Препараты на основе гепаринов хорошо известны сегодня, и трудно представить профилактику и лечение патологических поражений сосудов и тканей без этой группы биологически активных соединений. Известно, что гепарины применяют для лечения большого числа заболеваний: тромбозы и тромбоэмболии, ишемическая болезнь сердца и инфаркт миокарда, гломерулонефрит и другие. Препараты гепарина вводят человеку в виде инъекций, гелей в форме липосомальных препаратов и перорально.
Гепарин – протеогликан, в котором несколько полисахаридных цепочек связаны с общим белковым ядром. Дисахаридный компонент полисахаридных цепочек гепарина содержит глюкозамин и уроновую кислоту. Большинство аминогрупп остатков глюкозамина существуют в N-сульфатированной форме, но есть и небольшое количество ацетилированных аминогрупп. Более 90 % уроновой кислоты представлено идуроновой кислотой и только 10 % – глюкуроновой. Белковая составляющая протеогликана уникальна тем, что состоит только из сериновых и глициновых остатков.
Нефракционированные гепарины (НФГ) представляют собой гетеро-
генную смесь мукополисахаридов. Они связываются с поверхностью эндотелиальных клеток и различными белками плазмы. Биологическая актив-
ность НФГ зависит от плазменного протеазного ингибитора – антитром-
бина III. Антитромбин III ингибирует факторы свертывания – протеазы, особенно тромбин (фактор IIа), факторы IХ и Ха, при помощи формирования эквимолярных стабильных комплексов с ними. При отсутствии гепарина эти реакции протекают медленно, присутствие гепарина ускоряет их в 1000 раз. Только три молекулы в коммерческих препаратах НФГ имеют этот ускоряющий эффект ввиду наличия уникального пентасахаридного участка, необходимого для высокоаффинной связи с антитромбином. Активная молекула гепарина связывается с антитромбином и вызывает кон-
81
формационные изменения этого ингибитора. Конформационные изменения антитромбина предоставляют его активный участок для более интенсивного взаимодействия с протеазами. С тканевыми фактором (ТФ) фактор VII формирует активированный комплекс (VII-ТФ), который катализирует активацию ферментного каскада от фактора IX до фактора IХa. Активированный фактор XIa также катализирует эту реакцию. Ингибитор тканевого фактора ингибирует каталитическое действие VIIa-ТФ комплекса. Результатом этого каскада является превращение фибриногена в фибрин, эссенциальный компонент функционального сгустка. Гепарин, действующий в крови, прямо активирует противосвертывающие факторы, особенно антитромбин, который в свою очередь инактивирует ряд факторов.
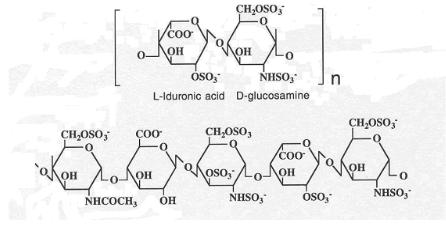
Препараты гепарина представляют собой гетерогенную смесь сульфатированных мукополисахаридов (гликозаминогликанов) с различными молекулярными массами. В полимере гепарина главная повторяющаяся дисахаридная единица имеет следующую формулу: 4)-2-дезокси-2- сульфамино-α-D-глюкопираноза-6-сульфат-(1 4)-α-L-идопиранозилуро- новая кислота-2-сульфат (1 . Повторяющаяся единица составляет в гепарине из легких крупного рогатого скота свыше 90 %, а в слизистой оболочке (мукозе) тонкого кишечника свиней около 75 %. В макромолекуле мукозного гепарина, кроме указанных дисахаридных фрагментов, присутствуют остатки 2-ацета-мидо-2-дезокси-α-D-глюкопиранозы и β-D- глюкуроновой кислоты. На pис. 13 представлены структурные компоненты гепарина. Высокое содержание сульфатных и карбоксильных групп обуславливает высокий отрицательный заряд гепарина; изоэлектрическая точка составляет pI – 3,2–4,2.
82
А
В
Рисунок 13 – Структурные компоненты гепарина:
А– наиболее частый тип дисахаридной единицы;
В– схематическое изображение уникальной пентасахаридной последовательности (места связывания для антитромбина III (АТ III)),
являющейся основным структурным центром, определяющим антикоагулянтную способность гепарина
НФГ неоднородны по своему составу. Их молекулярная масса колеблется от 2 кDа до 80 кDа. Фракции НФГ с низкой молекулярной массой (менее 5 кDа) обладают более мощной анти-Ха активностью, но меньшей антитромбиновой активностью. Фракции гепарина с высокой молекулярной массой (более 20 кDа) имеют противоположные свойства, т. е. в основном, обладают антитромбиновой активностью. Обнаружено, что антикоагулянтная активность гепарина связана с особенностями строения его молекулы. Так, антикоагулянтная активность зависит от содержания серы, степени сульфатирования, количества и расположения О-сульфатных групп, а также от размера скелета молекулы. Более высокая активность в препаратах с большим содержанием эфирсвязанной серы. Показано, что активность фракции, в которой на дисахаридную структурную единицу
83
приходится четыре остатка серной кислоты, в 1,4 раза превышает активность фракции гепарина с тремя остатками.
В качестве примера технологии получения субстанции гепарина натрия мы приводим методику получения гепарина из легких сельскохозяйственных животных:
1.Подготовка сырья (дефростация легких, отмывка от крови, взвешивание ткани, измельчение (4,5–5,0 мм)).
2.Экстракция гепарина (суспензию легких помещают в 20-й % раствор хлорида натрия, добавляют натрия карбонат, доводят 20 %-ным раствором натрия гидроокиси до значения рН 8,5–8,7; кипятят 5 мин, охлаждают до 50–60 °С).
3.Отделение экстракта гепарина от ткани легких и проведение осветляющей фильтрации раствора.
4.Сорбция гепарина (проводят последовательную сорбцию при 60–65 °С на нескольких ионообменных колонках с анионитом; после сорбции последовательно промывают анионит 1 М раствором хлорида натрия, очищенной водой, раствором для удаления липидов и снова очищенной водой).
5.Десорбция гепарина (проводят 20 %-ным раствором хлорида натрия, содержащим трилон Б с рН 7,5–8,0).
6.Выделение гепарина сырца (раствор гепарина охлаждают до 10–15 °С прибавляют охлажденный до 0–2 °С этанол, перемешивают и выдерживают для формирования осадка, который отделяют на нутч-фильтре, промывают охлажденным этанолом).
7.Сушка осадка при комнатной температуре, а затем при
50–60 °С.
8.Очистка гепарина сырца (сухой гепарин помещают в очищенную воду, доводят рН до 8,3–8,5 при помощи 18 %-ого раствора кислоты хлористоводородной, нагревают до 68–72 °С, прибавляют 5–10 %-ный раствор калия марганцовокислого, нагревают до 90–95 °С; осадок отделяют на мембранных фильтрах; доводят рН раствора 18 % -ным раствором кислоты хлористоводородной до значения 6,9–7,1; добавляют безводный натрий сернокислый, нагревают при 40–50 °С в течение 10 мин, охлаждают до
84
20–25 °С, прибавляют хлорид натрия, выдерживают 12 часов и раствор гепарина отделяют мембранной фильтрацией).
9. Выделение гепарина (к раствору гепарина прибавляют трилон Б из расчета 0,7 грамма на 1 литр раствора, доводят рН раствора 18 %-ным раствором кислоты хлористоводородной до значения 6,0–6,2; охлаждают до 5–10 °С и прибавляют этанол, выдерживают 24 часа; осадок отделяют на нутч-фильтре, промывают охлажденным этанолом; сушка осадка при комнатной температуре, а затем при 50–60 °С);
Однако НФГ имеют ряд существенных недостатков: они не способ-
ны ингибировать тромбин, связанный с тромбом, который продолжает активировать свертывание крови и ингибировать фибринолиз (процесс растворения тромбов и сгустков крови). Известным осложнением применения НФГ является гепарин-индуцированная тромбоцитопения. Кроме того, действие тромбина зависит от наличия кофактора – антитромбина III. Также гепарин может быть инактивирован тромбоцитарным фактором IV, белками плазмы крови или путем связывания его макрофагами. В следствии этого, для повышения эффективности антикоагулянтного действия НФГ необходимо прибегать к непрерывной внутривенной инфузии с си-
стематическим контролем активированного частично тромбопластиново-
го времени (АЧТВ) для корректировки дозы препарата. Тем не менее, даже такой подход может не обеспечить получение адекватного эффекта из-за несовершенства АЧТВ как показателя антикоагулянтной активности гепарина и отсутствия других, более эффективных, лабораторных тестов.
3.2.Биотехнологическое получение низкомолекулярных гепаринов
Наличие побочного действия у НФГ привело во второй половине 80-х годов к созданию низкомолекулярных гепаринов (НМГ). НМГ получа-
ют различными химическими и ферментативными способами деполимеризации гепарина из НФГ, полученного из слизистой кишечника свиньи. Образуются фрагменты от 4,0 до 6,5 кDа. НМГ обладают большей активностью в ингибировании фактора Ха и меньше влияют на тромбин
85
(фактор II). Отношение анти-Ха к анти-IIа (антитромбин) у различных НМГ варьирует от 2 : 1 до 4 : 1. В отличие от НФГ, у которого соотношение анти-Ха к активности АЧТВ составляет 1 : 1 ингибирование Ха фактора свертывания НМГ значительно более выражено, чем его влияние на АЧТВ. Это оказывает более благоприятное влияние на эффективность и переносимость НМГ и, соответственно, на ожидаемую противотромбическую активность и риск развития кровотечения. С химической и фармако-
логической точки зрения НМГ являются гетерогенной смесью полисаха-
ридов, которые содержат также биологически неактивные компоненты. По мнению ряда исследователей, способы получения НМГ: ферментативная деполимеризация, химическая деградация или фракционирование не влияют на их активность. Относительное содержание высоко- (более 7,5 кDа) и низко- (менее 2,5 кDа) молекулярных фрагментов полисахаридных цепочек определяет фармакодинамический и фармакокинетический профиль отдельных препаратов в клинических исследованиях. НМГ получают из слизистой оболочки кишок свиней, при этом НФГ был получен из слизистой оболочки кишок крупного рогатого скота с помощью ферментативной деполимеризации или прямой экстракции серной кислотой. При этом образуются фрагменты разной длины: а) молекулы, которые содержат около 16 моносахаридов и могут ингибировать не только фактор Ха, но и тромбин (IIа); б) молекулы из 8–18 моносахаридов (молекулярная масса меньше 5,4 кDа), которые ингибируют только фактор Ха; в) молекулы, которые имеют меньше, чем 8 моносахаридов и не проявляют ингибирующего эффекта; г) по меньшей мере, 24 сахаридных остатка должны быть в молекуле гепарина (что соответствует молекулярной массе около 7,2 кDа), чтобы он мог ускорять инактивацию тромбина антитромбином III.
Сегодня существует около 20 препаратов НМГ с молекулярной средней массой около 5 кDа. Главное преимущество НМГ следует из их фармакокинетических свойств: в 2–4 раза большее время полувыведения из организма, заметно лучшая биодоступность при подкожном введении и более стабильная дозовая реакция (доза может быть рассчитана только исходя из веса пациента, без дополнительного лабораторного исследования). Меньший токсический эффект связан с вызываемой НФГ тромбоцитопе-
86
нией, которая в свою очередь обусловлена взаимодействием НМГ с тромбоцитами. Кроме того, на лабораторных животных продемонстрирована возможность проникновения гепарина с молекулярной массой 1,9–4,6 кDа через гематоэнцефалический барьер.
Одним из первых способов получения НМГ явилась работа по ферментативной деполимеризации НФГ при помощи гепариназы, вы-
деленной из Flavobacterium heparinum. Для этой цели использовали гепарин натрия с молекулярной массой 17,3 кDа. НФГ растворяли в 0,1 М натрия ацетата и 0,01 М кальция ацетата. К раствору прибавляли гепариназу с активностью 1050 МЕ/мг, растворенную в 0,1 М натрия ацетата. Смесь термостатировали при 30 °С при постоянном перемешивании. Были получены НМГ со средней молекулярной массой около 5 кDа. С целью повышения эффективности технологии предложено использовать биотехнологический процесс деполимеризации НФГ на иммобилизованном комплексе ферментов.
Предложен способ получения НМГ путем ферментативной депо-
лимеризации с помощью комплекса ферментов (гепариназы), выделен-
ных из Streptomyces kurssanovii, иммобилизованных на силохроме, при весовом соотношении – гепарин (выделенный из слизистой оболочки свиньи с молекулярной массой 7,5–15 кDа) : иммобилизованный фермент (1 : 1). Суспензию перемешивают при 37 °С в течение 3 часов. Иммобилизованный фермент отделяют центрифугированием, промывают 0,5 М раствором натрия хлорида и водой для инъекций. Имеются данные о целесообразности проведения гидролиза гепариназами Streptomyces kurssanovii при температуре 40–45 °С. Промывную жидкость объединяют с супернатантом и обессоливают на колонке с сефадексом G-10. Элюирование проводится водой со скоростью 80 мл/ч. Полученный продукт НМГ подвергают лиофилизации. Получают НМГ с выходом около 70 % и молекулярной массой на 50–75 % ниже, чем у исходного гепарина. Анти-Ха активность составляет 130–170 МЕ/мг, что соответствует удельной активности таких препаратов как Фраксипарин и Дельтапарин. Молекулярная масса полученного НМГ составляла 4,5 кDа (при использовании исходного гепарина с молекулярной массой 15 кDа) и 2,7 кDа (при использовании исходного гепарина с молекулярной массой 7,5 кDа).
87