Материал: Фарм производство БАР
могут подаваться либо по заранее заданной программе, либо по мере необходимости при повышении уровня пены.
Стерилизация питательных сред и аппаратуры. В биотехнологии наибольшее распространение получила термическая стерилизация. В технических системах, работающих в асептических условиях, должна обеспечиваться стерилизуемость всех точек внутренних объемов аппаратов, коммуникаций, арматуры, контрольно-измерительных приборов, непосредственно соприкасающихся с чистыми культурами целевых микроорганизмов или со стерильными материальными потоками. Для этого в каждой точке необходимо создать требуемую температуру и поддерживать её в течение заданного промежутка времени.
Наибольшим бактерицидным эффектом обладает насыщенный водяной пар под давлением. При стерилизации насыщенным водяным паром споры наиболее устойчивых термофилов гибнут при температуре 121 °С и времени экспозиции 25 мин, при 132 °С – за 4 мин. При использовании сухого пара время гибели спор составляет при 160 °С – 60 мин., а при 180 °С
– 10 мин. Инактивация спор в кипящей воде при 100 °С происходит медленно, они гибнут через 8–9 часов. Большое значение имеет содержание воды в клетке микроорганизма – чем больше воды, тем ниже температура коагуляции белков. Именно этим объясняется высокий стерилизующий эффект насыщенного водяного пара – он не только нагревает, но и увлажняет клетки, что повышает термочувствительность.
Стерилизацию жидких питательных сред при работе с небольшими объемами целесообразно вести в периодическом режиме в несколько этапов:
стерилизация всех коммуникаций и ферментера острым или глухим паром;
наполнение аппарата прогретой гомогенизированной средой;
нагревание питательной среды до температуры стерилизации;
выдерживание при температуре стерилизации в течение времени, необходимого для гибели всех микроорганизмов;
охлаждение стерильной питательной среды в этой же емкости. Этот способ стерилизации длителен, и поэтому во избежание суще-
ственных изменений в составе среды, процесс ведут при избыточном дав-
58
лении 0,5–1 атм при температуре 110–120 °С в течение 1–1,5 часов с момента достижения заданной температуры.
Особое внимание следует уделять стерилизации аппаратуры и ком-
муникаций, предназначенных для подачи пеногасителя (125–135 °С в тече-
ние 1,5–2 часов). Стерилизацию осуществляют в следующей последовательности:
входной и выходной фильтры тонкой очистки, трубопроводы, ар-
матура;
ферментеры;
питательная среда при следующих режимах: температура – 120–124 °С, время выдержки после достижения заданной температуры –
40–60 мин.
2.6.1. Получение пенициллина
Для производства пенициллина используют специально отобранные расы плесневых грибов (суперпродуцентов), принадлежащие к роду Penicillium. Для промышленного производства пенициллина применяют биореакторы-ферментеры с механическим перемешиванием, объемом свыше 10000 дм3. Питательная среда, используемая для производства пенициллина, обычно содержит кукурузный экстракт, лактозу, глюкозу и др.
После стерилизации и охлаждения среда засевается проросшими спорами гриба, аэрируется путем пропускания через нее воздуха и перемешивается с помощью мешалки. Температуру культивирования поддерживают в пределах 24–25 °С. Для предотвращения чрезмерного образования пены применяются химические пеногасители. После окончания ферментации мицелий гриба отделяется вакуумной фильтрацией или центрифугированием.
Технологическая схема производства пенициллина приведена на рис. 9.
59
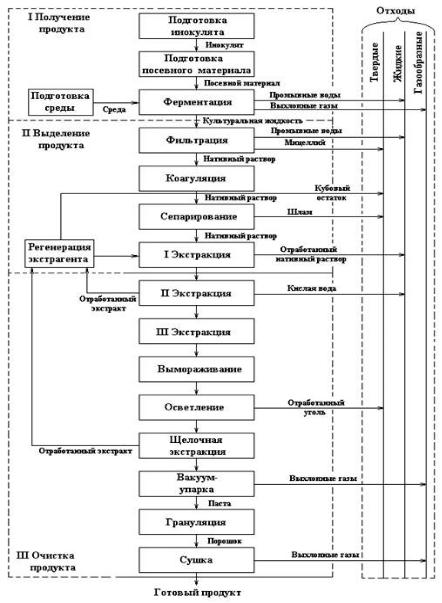
Рисунок 9 – Технологическая схема производства пенициллина
60
Для концентрирования пенициллина применяется экстракция органическими растворителями и адсорбция на активированном угле. Возможно также применение упаривания и осаждения.
Для промышленного производства антибиотика используют культуру Penicillium chrysogenum и среду, содержащую кукурузный экстракт, гидрол, лактозу и минеральные соли.
Вместо кукурузного экстракта может быть применена арахисовая мука, жмыхи, мука из хлопковых семян и другие источники. Возможность широкого использования продуктов растительного происхождения обусловлена тем, что у P. сhrysogenum имеются сильные протеолитические ферменты. В качестве углеводов часто используют сахарозу или смесь лактозы с глюкозой в соотношении 1 : 1. Глюкоза может снижать биосинтез антибиотика; на средах, содержащих лактозу или сахарозу (в условиях депрессии), биосинтез антибиотика идет активнее. Важную роль в процессе биосинтеза пенициллина играет сера, которая содержится в структуре антибиотика. В качестве источника серы используются натрия сульфат и натрия тиосульфат. Избыток ионов меди не влияет на рост гриба, но подавляет биосинтез пенициллина. Эффект торможения биосинтеза снимается добавлением в среду ионов железа. P. Сhrysogenum в качестве источника фосфора может использовать не только фосфаты, но и фитаты (соли инозитфосфорных кислот). Этот продуцент содержит фермент, разрушающий фитин с освобождением неорганического фосфора.
Температура в период первой фазы должны быть 30 °С, во вторую фазу – 20 °С; рН в период роста гриба ниже 7,0; потребление углеводов должно быть медленным, что достигается использованием лактозы, либо дробным введением глюкозы.
Синтез того или иного пенициллина зависит от наличия специфического вещества в среде, иначе говоря, предшественника, который микроорганизм включает в молекулу антибиотика без предварительного расщепления. Следует отметить, что предшественники биосинтеза пенициллина (фенилуксусная кислота, фенилацетамид, феноксиуксусная кислота) при определенных концентрациях и рН среды оказывают токсическое влияние
61
на продуцент. Фенилуксусная кислота (С6Н5СН2СООН) наименее токсична. Добавление её в среду в концентрации выше 500 мкг/мл угнетает рост мицелия, особенно в первые 24 часа его развития. При таких условиях обеспечивается наибольший выход бензилпенициллина, который через 72 часа развития может достигать 500–1000 мкг/мл.
При развитии гриба без внесения предшественника образуется около 45 % бензилпенициллина (пенициллин G) и около 53 % пенициллина К (радикал – n-гептилпенициллин). При добавлении к среде фенилуксусной кислоты меняется соотношение образующихся компонентов в сторону резкого увеличения бензилпенициллина, количество которого в зависимости от возраста достигает 75–99 % от смеси пенициллинов. В процессе культивирования P. Сhrysogenum в среде, не содержащей фенилуксусной кислоты, в ней накапливаются серосодержащие соединения не-лактамного характера, близкие к цистеину и метионину. Добавление в среду фенилуксусной кислоты способствует более интенсивному метаболизму серосодержащих компонентов в соединения -лактамного характера.
При развитии продуцента пенициллина (гриба P. Сhrysogenum) на кукурузно-лактозной среде выделяют три фазы.
Первая фаза – рост мицелллия, выход антибиотика низок. Всегда присутствующая в кукурузном экстракте молочная кислота потребляется продуцентом с максимальной скоростью, лактоза используется медленно. Потребление кислорода высокое. Усиливается азотный обмен, в результате в среде появляется аммиак и резко поднимается значение рН.
Вторая фаза – максимальное образование пенициллина. Это связано
сбыстрым потреблением лактозы и аммонийного азота. Увеличение массы мицелия незначительное, потребление кислорода снижается, рН среды остается почти без изменений.
Третья фаза – снижение концентрации антибиотика в среде в связи
сначавшимся автолизом мицелия и выделением в результате этого процесса аммиака, что сопровождается повышением рН среды.
62
В настоящее время описано шесть условно выраженных возрастных фаз продуцента пенициллина. Заметное количество пенициллина начинает образовываться с IV возрастной фазы гриба, максимум накопления приходится на VI фазу – в период автолиза.
Определение возрастных фаз путем микроскопического контроля позволяет установить: 1) ход общего темпа развития гриба, его состояние, пригодное для использования посевного материала, контроль за ходом образования антибиотика; 2) дефекты развития и возможные причины этих дефектов; 3) момент окончания развития гриба в реакторе.
По мере развития гриба меняется и химический состав мицелия. Количество общего азота и белка в мицелии уменьшается, содержание моносахаридов в период максимального биосинтеза пенициллина (96 часов) увеличивается почти в 6 раз по сравнению с начальным периодом, количество дисахаридов уменьшается. Изменяется количество отдельных аминокислот.
Процесс биосинтеза пенициллина ведется при самом тщательном соблюдении стерильности всех операций, так как загрязнение культур посторонней микрофлорой резко снижает накопление антибиотика. Это связано с тем, что многие бактерии воздуха способны образовывать пенициллиназу. Особенно активно продуцируют этот фермент B. subtilis и B. cereus. Одним из активных продуцентов пенициллиназы является туберкулезная палочка (Mycob. tuberculosis). Предположительно именно с этим свойством связана резистентность этого микроорганизма к пенициллину.
Механизм биосинтеза молекулы пенициллина представлен на рис. 10.
63
Кетоглутарат + Ацетил-КоА
Гомоцитрат
α-кетоадипиновая кислота
α-кетоадипиновая кислота
L- -аминоадипиновая кислота (L- -ААК)
L-цистеин
L- -ААК-L-цистеин (LL –дипептид)
L-валин
L- -ААК-L-цистеин-D-валин (LLD-трипептид)
Моноциклический -лактам
L- -ААК-L-цистеин-D-валин (LLD-трипептид)
Изопенициллин N (L- -АКК-6-АПК)
С6Н5СН2СООН
Бензилпенициллин (С6Н5СН2СО-6-АПК)
Рисунок 10 – Механизм биосинтез молекулы пенициллина
64
Современная биотехнологическая промышленность получает культуральные жидкости, содержащие свыше 55 тыс. ед/мл пенициллина. Выделение пенициллина начинается с фильтрации или центрифугирования (отделения мицелия гриба).
Из культуральной жидкости антибиотик, где он находится в виде кислоты, выделяют путем экстракции неполярными органическими растворителями (амилацетатом, хлороформом, бутилацетатом, бутанолом и др.). Очистку антибиотика проводят путем замены растворителей, поскольку соли пенициллина плохо растворимы в органических растворителях. Экстрагированный пенициллин в виде кислоты переводят в водный раствор в виде соли, добавляя щелочь. Повторяя эти операции, пенициллин кон-центрируют и очищают. Большинство пенициллинов производят в виде натриевых или калиевых солей. Новокаиновые и бензатиновые соли являются основой пролонгированных препаратов пенициллина для внутримышечного введения.
Всухой кристаллической форме пенициллиновые соли достаточно стабильны в течение длительного времени при температуре 4 °С. Растворы быстро теряют активность (в течение 24 часов при температуре 20 °С), их готовят непосредственно перед введением.
Внастоящее время большое практическое значение имеет
полусинтетический (биологический + химический) способ получения аналогов природного пенициллина. Исходным продуктом служит
6-аминопенициллановая кислота (6-АПК). Эту кислоту получают в результате биосинтеза при развитии P. Сhrysogenum при отсутствии предшественника в среде или путем ферментативного дезацилирования бензилпенициллина или феноксиметилпенициллина при участии фермента пенициллинацилазы (пенициллинамидазы). Второй способ наиболее перспективен. Используется иммобилизованная пенициллинацилаза, которая гидролизует бензилпенициллин с образованием 6-АПК и фенилуксусной кислоты. Пенициллинацилаза образуется различными группами микроорганизмов, в том числе она образуется всеми продуцирующими пенициллин грибами. В настоящее время предложен способ получения иммобилизо-
65
ванных клеток E. Coli с высокой пенициллинацилазной активностью, пригодных для многократного применения.
Сама по себе 6-АПК не активна. Её подвергают химическому ацилированию и получают аналоги пенициллина (оксациллин, ампициллин, метициллин, амоксициллин и др.) с улучшенными или новыми свойствами. Всего в настоящее время используется порядка четырех десятков таких препаратов.
Из всего общего количества природных пенициллинов примерно 35 % используется как медицинские препараты, а 65 % – для получения 6-АПК.
2.6.2. Получение стрептомицина
Для производства стрептомицина используют штаммы актиномицета Streptomyces griseus, образующего воздушный мицелий и споры. Продуцент образует максимальное количество стрептомицина в жидкой питательной среде, содержащей мясной экстракт.
В качестве основы питательных сред используют продукты гидролиза растительных или животных белков. Среду стерилизуют при 120 °С, охлаждают и засевают посевным материалом. Культивирование проводится при 25–30 °С и сопровождается аэрацией и перемешиванием.
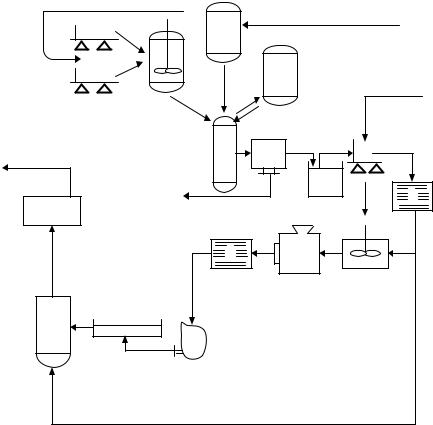
На рис. 11 представлена аппаратурная схема производства стрептомицина.
66
Сырье |
Посевной материал из качалок |
|||||
|
||||||
1 |
4 |
|
|
|
|
|
|
3 |
|
|
|
|
|
2 |
|
|
17 |
|
|
|
|
|
|
|
|
|
Каолин |
Готовая |
5 |
6 |
|
Биомасса 8 |
Каолин |
|
продукция |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
7 |
Биомасса |
|
|
Центрифугат в |
|
|
|
9 |
|
16 |
|
|
|
|
||
канализацию |
|
|
|
|
||
|
|
|
|
|
||
|
|
|
|
|
|
|
|
12 |
|
11 |
|
10 |
|
|
|
|
|
|
||
15 |
14 |
|
|
|
|
|
|
|
|
|
|
|
|
|
13 |
|
|
|
|
|
Рисунок 11 – Аппаратурная схема производства стрептомицина:
1,2 – весы для сырья; 3 – емкость для приготовления питательной среды; 4 – аппарат для посева; 5 – биореактор; 6 – центрифуга; 7 – емкость для биомассы; 8 – весы для биомассы и каолина; 9 – электросушильный шкаф для стерилизации
каолина; 10 – смеситель; 11 – гранулятор; 12 – электросушильный шкаф для сушки гранулированной биомассы с каолином; 13 – мельница; 14 – вибрационное сито; 15 – емкость для стандартизации продукта; 16 – агрегат для упаковки и маркировки готового продукта; 17 – емкость для дезинфицирующего раствора
67