Материал: Фарм производство БАР
щается продуктами обмена и продуктами автолиза клеток, возрастает значение рН, происходит интенсивный процесс биосинтеза и максимальное накопление антибиотика.
Биосинтез антибиотиков возрастает в фазе замедленного роста клеточной популяции (конец трофофазы) и достигает максимума в стационарной фазе (идиофазе). Считают, что в конце трофофазы изменяется энзиматический статус клеток, появляются индукторы вторичного метаболизма, освобождающие гены вторичного метаболизма из-под влияния катаболитной репрессии. Поэтому любые механизмы, тормозящие клеточную пролиферацию и активный рост, стрессовые ситуации, активируют процесс образования антибиотиков.
Процесс культивирования идиолитов происходит в две фазы (двух-
ступенчатое культивирование). На первой фазе происходит накопление достаточного количества биомассы, которая выращивается на среде для роста микроорганизма. Эта фаза должна быть быстрой, а питательная среда дешевой. На второй фазе осуществляется запуск и активный синтез антибиотика. На этой фазе ферментацию ведут на продуктивной среде.
2.3.1. Получение антибиотиков с использованием биосинтеза
Методы получения антибиотиков путем химического синтеза достаточно сложны и не могут конкурировать с их биосинтезом методом биотехнологии. Существует несколько способов получения как природных, так и полусинтетических антибиотиков. Направленный биосинтез антибиотиков осуществляется путем прямой ферментации микроорганизма – продуцента с подходящим предшественником, что индуцирует синтез ферментов вторичного метаболизма в идиофазе. Точный механизм индуцирования первичными метаболитами генов, кодирующих синтез ферментов вторичного метаболизма, окончательно не расшифрован, однако выяснено, что молекулы предшественника необходимо добавлять в среду в период фазы роста микроорганизмов. Установлено, что вводимый предшественник должен лимитировать скорость биосинтеза антибиотика. Например, производство бензилпенициллина в значительной степени стимулируется добавками его метаболического предшественника – фенилуксусной кислоты; пропионовая кислота и пропиловый спирт индуцируют биосин-
38
тез макролидов через метилмалонил КоА; L-фенилаланин – предшественник фенилаланина – ускоряет синтез грамицидина-S. Аналогичный эффект вызывает использование ингибиторов метаболизма. Так, при подавлении процесса введения хлора микроорганизм S. aureofaciens образует тетрациклин, а не хлортетрациклин, а при ингибировании реакции метилирования им синтезируются деметилированное производное хлортетрациклина.
Другой способ получения антибиотиков состоит в использовании для их биосинтеза блокированных мутантов, у которых отсутствует (блокировано) определенное звено в цепи реакций, ведущих к синтезу антибиотика. Блокированные мутанты не способны образовывать нужный антибиотик, используя низкую субстратную специфичность ферментов вторичного метаболизма и вводя аналоги предшественника антибиотика, последние переводят в аналоги самого антибиотика в ходе процесса, известного как мутационный биосинтез, или мутасинтез. Схема мутационного биосинтеза антибиотика показана на рис. 2.
Предполагаемая
последовательность реакций, А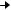 В
В 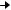 Фермент
Фермент 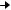 С
С 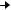 D
D 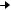 E
E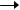 Антибиотик ведущая к синтезу антибиотика
Антибиотик ведущая к синтезу антибиотика
Отсутствие синтеза
антибиотика у А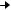 В
В  С
С 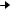 D Блокированное звено метаболизма
D Блокированное звено метаболизма
«блокированного» мутанта
Синтез модифицированного
антибиотика после введения А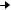 В
В ...D*
...D*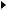 Е*
Е*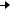 Модифицированный антибиотик аналога предшественника (D*)
Модифицированный антибиотик аналога предшественника (D*)
Рисунок 2 – Схема мутационного биосинтеза антибиотика
39

Так, мутанты Nocardia mediterranei, у которых нарушена способность к ацилированию, образуют аналог предшественника рифамицина В – рифамицин SV, который служит исходным веществом для получения многих синтетических рифамицинов.
Особенно успешны разработки в области биосинтеза полусинтетических пенициллинов и цефалоспоринов. Получение новых более эффективных аналогов пенициллина основано на изменении его ацильной группировки при сохранении в неизменном виде ядра пенициллина – 6-аминопенициллановой кислоты (6-АПК). В промышленности 6-АПК получают путем гидролиза природных пенициллинов с помощью специфического фермента пенициллинацилазы, образующейся с высоким выходом в процессе ферментации ряда штаммов микроорганизмов. Ацилазы различают по их субстратной специфичности. Некоторые из них способны катализировать и обратные реакции – процессы ацилирования аминогруппы 6-АПК с образованием модифицированного пенициллина. Таким путем было получено более 40000 полусинтетических пенициллинов. Существенным является то, что во многих случаях 6-АПК не выделяют из культуральной жидкости, например, при превращении бензилпенициллина в ампициллин (рис. 3).
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
S |
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
СН2 |
|
|
СО |
|
|
|
NH |
|
|
|
|
|
|
|
CH3 |
+H2O, пенициллинацилаза |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
СН2 |
|
СООH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
O |
|
|
C N |
|
|
|
COOH |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
Бензилпенициллин |
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
S |
|
|
CH3 |
|
|
|
|
|
|
|
||
|
|
|
|
H2N |
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
O |
|
|
C |
N |
|
|
COOH |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
6-АПК
Рисунок 3 – Схема превращения бензилпенициллина в 6-АПК
40
Бензилпенициллин гидролизуют ацилазой мутанта Kluyvera citrophila при рН 7,8–8,0 и температуре 40–50 °С. Затем в ферментер вносят мутант Pseudomonas melanogenum и фенилглицин. Условия ферментации изменяют таким образом (рН 5,0–5,5), чтобы ацилаза второго мутантного организма осуществляла синтез ампициллина (рис. 4).
|
|
|
|
NH2 |
|
|
|
|
S |
|
CH3 |
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
СН |
|
СООH H2N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ацилаза |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-H2О |
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
O |
|
|
C |
N |
|
|
|
|
COOH |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
Фенилглицин |
|
|
|
6-АПК |
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
S |
CH3 |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
СН |
|
СО |
|
NH |
|
|
|
|
|
|
|
CH3 |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
C N |
|
|
COOH |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ампициллин |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
Рисунок 4 – Схема получения ампициллина
Замена ацильного остатка приводит к синтезу других полусинтетических антибиотиков. Так, например, если в структурной формуле антибиотика ацильный остаток представлен в виде (см. рис. 5), а радикал в молекуле пенициллина представлен в виде (см. рис. 6) – образуется метициллин, а в случае представления радикала в виде (см. рис. 7) – оксациллин.
RC
O
Рисунок 5 – Вид ацильного остатка
41
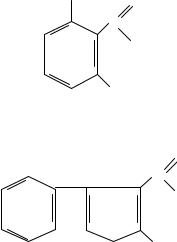
OCH3 O
C
OCH3
Рисунок 6 – Вид радикала в молекуле пенициллина (метициллин)
O
C
N
O CH3
Рисунок 7 – Вид радикала в молекуле пенициллина (оксациллин)
2.3.2.Получение антибиотиков с использованием генной инженерии
Весьма перспективным является получение новых антибиотиков путем создания генно-инженерных продуктов, в частности рекомбинантных штаммов продуцентов. Большой эффект может дать технология рекомби-
нантных ДНК. При создании рекомбинантных штаммов Streptomyces (основного микроорганизма, используемого для получения антибиотиков) важно понять, что трансформация и отбор трансформированных клеток не должны быть слишком сложными. Однако, в отличие от E. Coli, Streptomyces существует не в виде изолированных клеток, а в виде протяженных мицелл, поэтому перед трансформацией необходимо разрушить клеточную стенку и высвободить отдельные протопласты. Без этого будет невозможно отличить трансформированные клетки от нетрансформированных, поскольку видимые колонии на твердой среде будут образовываться из группы клеток, а не из индивидуальной клетки. Соответственно колонии, растущие в присутствии селективного антибиотика, будут представлять собой смесь трансформированных и не трансформированных кле-
42
ток. Проникновение плазмидной ДНК в протопласты Streptomyces облегчается в присутствии полиэтиленгликоля. После трансформации протопласты сначала высевают на твердую среду, чтобы образовалась клеточная стенка, а затем для отбора трансформированных клеток переносят на селективную среду, обычно содержащую неомицин, либо тиострептон. Актиномицеты являются продуцентами большинства промышленно важных антибиотиков. Известно, что один из эффективных путей воздействия на геном актиномицетов – это протопластирование их клеток. Показано, что протопластирование может влиять на уровень антибиотической активно-
сти. Метод слияния протопластов различных штаммов может служить для получения рекомбинантов, способных синтезировать новый антибио-
тик, или обладающих более высоким уровнем образования антибиотика. Биотехнология данного процесса следующая: мицелий отмывают от питательной среды, промывают специальными средами путем центрифугирования; проводят лизис в питательной среде, содержащей 20 % сахарозу и лизоцим в концентрации 1–2 мг/мл; нелизированный материал отделяют центрифугированием при 1000 об/мин; протопласты осаждают путем центрифугирования при 3000 об/мин; протопласты высевают на питательные среды и инкубируют при (27 ± 1) °С в течение 15 суток.
Кроме того, с помощью генной инженерии можно не только создавать новые антибиотики, но и увеличивать эффективность синтеза уже известных. Лимитирующим фактором в промышленном производстве антибиотиков с помощью Streptomyces часто является количество доступного клеткам кислорода. Вследствие плохой растворимости кислорода в воде и высокой плотности культуры Streptomyces его часто оказывается недостаточно, рост клеток замедляется, и выход антибиотика снижается. Решить эту задачу можно двумя способами: во-первых, изменить конструкцию ферментера, в котором выращивается культура Streptomyces, а во-вторых, используя методы генной инженерии, создать штаммы Streptomyces, более эффективно использующие имеющийся кислород. Эти два подхода не исключают друг друга. Одна из стратегий, которая используется некоторыми аэробными микроорганизмами для выживания в условиях недостатка кислорода, состоит в синтезе гемоглобинподобного продукта, способного аккумулировать кислород и доставлять его в клетки. Например, аэробная
43
бактерия Vitreoscilla синтезирует гомодимерный гемсодержащий белок, функционально подобный эукариотическому гемоглобину. Ген гемоглобина Vitreoscilla был выделен, встроен в плазмидный вектор Streptomyces и введен в клетки этого микроорганизма. После его экспрессии на долю гемоглобина Vitreoscilla приходилось примерно 0,1 % всех клеточных белков Streptomyces coelicolor даже в том случае, когда экспрессия осуществлялась под контролем собственного промотора гена гемоглобина Vitreoscilla, а не промотора Streptomyces. Трансформированные клетки Streptomyces coelicolor, растущие при низком содержании растворенного кислорода (примерно 5 % от насыщающей концентрации) синтезировали в 10 раз больше актинородина на 1 г сухой клеточной массы и имели большую скорость роста, чем нетрансформированные. Этот подход можно использовать и для обеспечения кислородом других микроорганизмов, растущих в условиях недостатка кислорода.
Исходным материалом при химическом синтезе ряда цефалоспоринов – антибиотиков, обладающих незначительным побочным эффектом и обладающий высокой антибактериальной активностью, – является 7-аминоцефалоспорановая кислота (7АСА), которая в свою очередь синтезируется из антибиотика цефалоспорина С. К сожалению, природных микроорганизмов, способных синтезировать 7АСА, до сих пор не выявлено. Предложен путь биосинтеза 7АСА за счет включения специфических генов в плазмиду гриба Acremonium chrysogenum, который в обычных условиях синтезирует только цефалоспорин С. Один из этих генов был представлен кДНК гриба Fusarium solani, кодирующий оксидазу D-аминокислот, а другой происходил из геномной ДНК Pseudomonas diminuta и кодировал фермент – цефалоспоринацилазу. В плазмиде гены находились под контролем промотора Acremonium chrysogenum. На первом этапе нового биосинтетического пути цефалоспорин С превращается в 7- -(5-карбокси-5-оксопентанамид) цефалоспорановую кислоту (кето-AD- 7АСА) при помощи оксидазы D-аминокислот. Часть этого продукта, вступая в реакцию с пероксидом водорода, одним из побочных продуктов, превращается в 7- -(4-карбосибутанамид) цефалоспорановую кислоту (GL-7ACA). И цефалоспорин С, и кето-AD-7АСА, и GL-7ACA могут подвергаться гидролизу цефалоспоринацилазой с образованием 7АСА, однако
44
только 5 % цефалоспорина С напрямую гидролизуется до 7АСА. Исходя из полученных данных установлено, что для образования 7АСА с высоким выходом необходимы оба фермента.
2.3.3.Получение антибиотиков с использованием иммобилизованных ферментов
Хорошо известно, что 6-АПК является исходным соединением для получения эффективных полусинтетических аналогов природных пенициллинов. Получение 6-АПК в промышленности путем химического гидролиза бензилпенициллина сопряжено с большими трудностями в связи с крайней неустойчивостью лактамного цикла его молекулы. Так, при щелочном гидролизе бензилпенициллина выход 6-АПК составляет всего 1 %.
Продуктивность этого метода удалось значительно повысить благодаря применению гидролиза иммобилизованных бактериальных клеток, содер-
жащих пенициллинамидазу. Со второй половины 70-х годов ХХ века вся 6-АПК, выпускаемая в России и значительная часть 6-АПК, выпускаемой в Италии производится с помощью иммобилизованных ферментов. Применяют фермент, иммобилизованный путем включения клеток E. Coli в волокна триацетата целлюлозы, а на российских предприятиях используют бактериальные клетки, иммобилизованные в полиакриламидном геле. Переход к технологии, применяющей иммобилизованные бактериальные клетки обеспечивают высокий выход 6-АПК, составляющий 80–85 %. По данным японских исследователей, время полуинактивации пенициллинамидазы в полиакриламидном геле бактериальных клеток равно 42 суткам при 30 °С или 17 суткам при 40 °С.
Одним из перспективных методов получения антибиотиков является использование ферментов в качестве катализаторов. Ферментативный синтез полусинтетических β-лактамных антибиотиков является объектом пристального внимания исследователей в течение нескольких десятилетий, а в последние годы он находит все большее практическое применение, благодаря преимуществам биокатализа, перед традиционными химическими технологиями. Прежде всего, это связано с возможностью достижения высокой чистоты конечного продукта, так как уникальная специфичность и высокая реакционная способность ферментов позволяет проводить
45
направленные реакции, избегая побочных процессов и риска рацемизации. Неоспоримы преимущества биокаталитических технологий с точки зрения охраны окружающей среды: ферментативные реакции протекают в мягких условиях (рН, температура); исключается использование токсических реагентов на стадии активации карбоксильной группы ацилирующего агента и особо вредных галогенсодержащих растворителей; значительно уменьшается общее количество используемых органических растворителей и реагентов. На сегодняшний день известны единичные случаи применения энзиматического синтеза для промышленного производства β-лактамных антибиотиков (например, выпуск цефалексина компанией DSM, Нидерланды).
Исходными соединениями для получения беталактамных антибиотиков являются пенициллины, такие как цефалоспорин С и цефамицин С или получаемые путем их химической или энзиматической трансформации производные (например, 7-фенилацетамидодезацетксицефалоспорановая кислота, называемая цефалоспорином G).
Для ферментативного синтеза β-лактамных антибиотиков чаще всего используют широко специфичную пенициллинацилазу из различных микроорганизмов, а также другие ферменты, принадлежащие к тому же классу гидролаз, но более специфичные к синтезу определенных групп антибиотиков (например, синтетазу цефалоспоринов – из E. Coli). Пенициллинацилаза проявляет специфичность предпочтительно к фенилуксусной и феноксиуксусной кислотам, а также к их производным, содержащим небольшие заместители в положении (амин, гидроксил, метил) или в ароматическом ядре.
Известно два направления синтеза β-лактамов:
1.Термодинамически контролируемый синтез – прямое образование ациламидной связи из свободной карбоновой кислоты и ключевой аминокислоты (ядра антибиотика), являющееся наиболее простым энзиматическим способом синтеза β-лактамных антибиотиков;
2.Кинетически контролируемый синтез является альтернативой прямому синтезу, который предусматривает синтез с переносом ацильной части ацилирующего агента на первичную аминогруппу ключевой аминокислоты. Ацилирующим агентом в данном случае служит не свободная
46
карбоновая кислота, а активированное производное карбоновой кислоты или аминокислоты.
Выделение продуктов биокаталитического синтеза. Биокатали-
тические технологии отличаются от традиционных химических технологий не только стадией собственно синтеза, но и схемой выделения целевых продуктов. Реакционные смеси при ферментативном синтезе, как правило, содержат соединения близкой физико-химической природы, поэтому раз-
работка процессов разделения компонентов реакционных масс и выделения целевых продуктов, представляет собой, пожалуй, наиболее сложную проблему при создании биокаталитической технологии получения
β-лактамов. Особенно сложной является проблема разделения компонентов реакционной смеси синтеза амино-β-лактамов, содержащей три аминокислоты (целевой продукт, ядро β-лактама и побочный продукт синтеза), изоэлектрические точки и растворимость которых достаточно близки. Кроме того, из-за низкой растворимости побочных продуктов синтеза существует опасность осаждения их еще в процессе ферментативного превращения даже при работе с низкоконцентрированными растворами реагентов, поскольку ацильный донор практически всегда берется в избытке.
Разработаны оригинальные методы отделения иммобилизованных ферментов от реакционной массы, содержащей кристаллические компо-
ненты. Один из методов основан на использовании иммобилизованного фермента с плотностью меньше единицы, частицы которого флотируют на поверхности жидкости после прекращения перемешивания реакционной массы, в то время как кристаллические продукты удаляются через днище реактора. Другой подход к этой проблеме базируется на инженерном решении. Сконструированы специальные сита с порами такого размера, который позволяет мелким кристаллическим компонентам реакционной смеси проходить вместе с фильтратом через отверстия в сите, задерживая при этом в реакторе крупные частицы иммобилизованного фермента с диаметром более 150 мкм. Реакторы с такими фильтрующими ситовыми днищами используют, например, для отделения биокатализатора от смеси амоксициллина с парагидрокси-D-фенилглицина при получении амоксициллина.
47