Материал: Фарм производство БАР
2.4. Условия культивирования продуцентов антибиотиков
Синтез антибиотиков определяется условиями культивирования микроорганизмов. Поэтому оптимизация питательной среды является одним из главных факторов, приводящих к увеличению выхода целевого продукта – антибиотика.
При проведении первой стадии технологического процесса получения антибиотиков применяют натуральные среды неопределенного состава, к числу которых относят продукты крахмалопаточного производства, агар, желатин, отруби, зерно. Композиция натуральных сред неопределенного состава не является постоянной. Например, агар, получаемый из разных видов морских водорослей, по химическому составу является сложным эфирным комплексом полисахарида с серной кислотой и разнообразными микроэлементами. Агар содержит также жирные кислоты, биотин, тиамин или его компоненты. В картофельной среде с глюкозой и пептоном, при одной и той же партии пептона и химически чистой глюкозы, состав картофельного экстракта зависит от сорта картофеля, места его выращивания, время уборки, срока и режима хранения и других причин. Поэтому для получения сопоставимых результатов, особенно при изучении физиологических и биохимических особенностей микроорганизма, применяют синтетические среды, в состав которых входят определенные химически чистые соединения, взятые в точно указанных концентрациях. Для выделения актиномицетов, являющихся основными продуцентами антибиотиков, используют синтетические питательные среды, в которые в качестве источника углерода добавляют крахмал или глицерин. В качестве источника азота в среды добавляют нитратные соли. На этих средах рост бактерий подавляется, а грибы развиваются в малом количестве. Чтобы они росли лучше, нужно подкислить среду до значений рН = 4,0–4,5. Например, мутантные штаммы культивируют на обогащенной питательными компонентами среде. Процесс контролируют либо по концентрации биомассы, либо по концентрации питательных веществ в среде. Исследования показали, что выход цефалоспорина С уменьшается при переходе от использования в качестве источника углерода сахарозы к быстро усваиваемому углеводу глюкозе. Наиболее оптимальной средой для образования антибиотика культурой
48
Streptomyces antibioticus оказалась смесь 0,1 % глюкозы и 1 % галактозы. При таком соотношении моносахаридов глюкоза быстро утилизируется и микроорганизм переключается на усвоение галактозы, что и инициирует идиофазу. Для производства ряда антибиотиков необходимы липидные компоненты, в частности, насыщенные и ненасыщенные жирные кислоты. Так, например, для образования цефалоспорина С (штамм Cephalosporium acremonium) необходимо потребление в составе питательной среды жирных кислот: миристиновой С14:0, пальмитиновой С16:0, олеиновой С18:1, линолевой С18:2. Обнаружено, что при культивировании штамма обнаруживается максимальное потребление олеиновой и линолевой кислот.
Для выращивания актиномицетов предложено множество сред различного состава, например: соево-глицериновая среда, содержащая соевую муку – 1,5 %, глицерина – 3 %, натрия хлористого – 0,3 %, кальция карбоната – 0,3 % или соево-глюкозная среда, содержащая соевую муку – 1,5 %, глюкозы – 4 %, натрия хлористого – 0,25 %, кальция карбоната – 0,2 %, кальция хлорида – 0,2 %, сульфата натрия – 0,05 %. На этих средах культуры выращивают при 28 ° С в течение 6–7 суток.
На примере Streptomyces hygroscopicus (продуцент комплекса антибиотика азоломицина, полиеновых и неполиеновых макролидов) было показано, что использование хлористого аммония как единственного источника азота в высоких концентрациях или его добавление в питательные среды, содержащие аминокислоты (валин, треонин, серин) снижает синтез антибиотика. Добавление хлористого аммония в питательную среду, содержащую аланин и лизин, приводит к повышению синтеза антибиотика. Наличие в среде индивидуальных аминокислот валина и треонина также усиливает синтез антибиотика. Данный эффект может быть связан с тем, что у многих видов микроорганизмов ионы аммония ассимилируются по одному или двум метаболитным путям. При высоких концентрациях аммония глутаматдегидрогеназа катализирует восстановительное аминирование -кетоглутарата до глутамата, а при недостаточном снабжении ионом аммония глутаматсинтетаза катализирует АТФ-зависимое образование глутамина. Глутамин может быть образован в результате трансаминирования -кетоглутарата катализируемого глутаматсинтетазой.
Для увеличения выхода антибиотика и возможности направлять биосинтез в необходимом направлении в питательные среды добавляют ряд веществ – предшественников антибиотиков. Так как многие антибиотики
49
берут свое начало от промежуточных соединений обмена первичных метаболитов, то их биосинтез возможно регулировать путем ретроингибирования. Например, биосинтез пенициллина культурой гриба Penicillium chrysogenum контролируется по принципу обратной связи L-лизином. Этот эффект объясняется тем, что биосинтез как пенициллина, так и лизина осуществляется через общего предшественника – -аминоадипиновую кислоту. Торможение лизином первого фермента биосинтеза (гомоцитратсинтазы) приводит к недостатку -аминоадипиновой кислоты, что снижает выход антибиотика. Добавление в питательную среду α-аминоадипиновой кислоты предотвращает ингибирующий эффект лизина и активирует биосинтез пенициллина в отсутствие лизина. Кроме ретроингибирования биосинтез многих антибиотиков тормозится высокими концентрациями своих же антибиотиков. С накоплением определенной концентрации антибиотика рост микроорганизмов прекращается (например, Streptomyces griseus прекращает свой рост при концентрации в среде стрептомицина сульфата 0,5 %). Следует отметить, что в процессе эволюции многие микроорганизмы выработали механизмы защиты от действия собственных антибиотиков. Эта проблема успешно решается в результате использования иммобилизованных ферментов.
Большинство антибиотиков получают при глубинной аэробной ферментации периодического действия в асептических условиях. Период ферментации длится 7–10 суток.
Стадия выращивания вегетативного инокулюма в значительной ме-
ре определяет конечный результат ферментации. Установлено, что способность продуцента к интенсивному биосинтезу зависит от многих факторов, в том числе, от гидродинамических условий выращивания посевного материала, возраста и количества посевного мицелия. Культуры инокулюма используют от 10 % до 40 % при различных значениях интенсивности дыхания. Кроме того, направленность вторичного синтеза на образование того или иного метаболита определяется интенсивностью углеводного обмена, а именно, соотношением активности ферментов гликолиза и пентозофосфатного пути, которое в свою очередь зависит от характеристики посевного материала. На этом этапе при производстве антибиотиков необходимо проводить определение интенсивности дыхания посевной культуры, например, с помощью газоанализатора. Желательно использовать культуру с максимальной интенсивностью роста.
50
В процессе культивирования возникает необходимость изучения ферментов, катализирующих ключевые для вторичного метаболизма реакции, обусловленная практической задачей повышения продуктивности промышленных штаммов. Важное значение одного из этих ферментов – пропионил-КоА-карбоксилазы – определяется участием её в синтезе первичного безазотистого предшественника – метил-малонил-КоА, включающегося в макроциклические лактонные кольца макролидных антибиотиков (эритромицин, олеандомицин и др.), полиэфирных антибиотиков (салиномицин, монензин и др.) анзамицинов и др.
2.5. Выделение и очистка антибиотиков
Экстракцию антибиотиков из культуральной жидкости проводят ацетоном, бутанолом и другими органическими растворителями. Необходимо отметить, что при экстракции антибиотиков используют различные значения рН: для A. Rubra – нейтральное значение рН, для A. Madurae A и Carminata (карминомицин) – щелочное значение рН.
Технология выделения антибиотиков включает: экстракцию анти-
биотиков подходящими растворителями, осаждение и перекристаллизация их из разных сред, фракционирование на ионообменных смолах, лиофильную и распылительную сушку готовых препаратов. На экстракцию антибиотика в значительной степени влияет значение рН. Так, например, при выделении антрациклиновых антибиотиков установлено, что антрациклиновые антибиотики (рубомицин, канамицин, доксорубицин) взаимодействуют с полимерными сорбентами по ион-ионному и гидрофобному механизмам. Наиболее селективная сорбция происходит на сегрегированном карбоксильном катионите БДМ-12 (метакрилсодержащий катионит). Показано, что максимальное поглощение антрациклинового антибиотика находится в области нейтральных значений рН, когда в системе сорбент – сорбат реализуются как ион-ионные, так и гидрофобные взаимодействия.
Из культуральной среды антибиотики выделяют экстракцией органическими растворителями, осаждением, адсорбцией. Очистку антибиотиков проводят повторной заменой растворителя, адсорбционнохроматографическими методами, высокоэффективной жидкостной хрома-
тографией (ВЭЖХ). От степени чистоты препарата, влажности, температуры, рН растворителя зависит стабильность антибиотика.
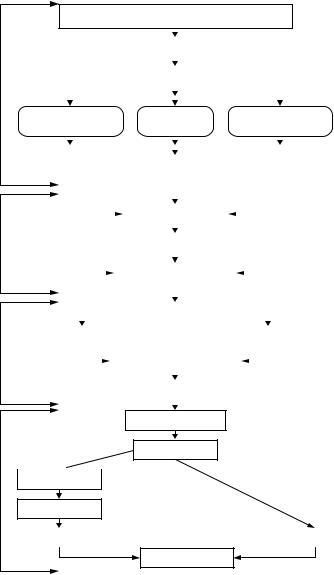
Общая схема получения антибиотиков представлена на рис. 8.
51
|
|
|
|
|
|
|
Выделение штамма-продуцента |
||||||||||||||||||||||
|
|
|
|
|
|
антибиотика из природных условий |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
Селекция наиболее активного штамма |
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
І |
|
|
|
Получение наиболее активного штамма методами: |
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
СТАДИЯ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Индуцированного |
|
|
|
Слияния |
Генно-инженерной |
|||||||||||||||||||||
|
|
|
мутагенеза |
|
|
протопластов |
|
|
манипуляцией |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
Высокопродуктивный и технологичный штамм продуцента |
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ІІ |
|
Продуцент |
|
|
|
|
|
|
Посевной материал |
|
|
|
|
|
|
|
Питательная среда |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
СТАДИЯ |
|
|
|
|
|
|
|
|
|
|
Подготовка инокулята |
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
Смешанная |
|
|
|
|
|
Культивирование |
|
|
|
|
|
|
|
|
|
Монокультура |
|||||||||||
|
|
|
культура |
|
|
|
|
|
(процесс биосинтеза) |
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
Разделение |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
ІІІ |
|
Культуральная жидкость |
|
|
|
|
|
|
Биомасса |
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
СТАДИЯ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Выделение антибиотика |
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Очистка |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Концентрирование
Стабилизация
ІV  СТАДИЯ Обезвоживание
СТАДИЯ Обезвоживание
Измельчение
Сухой препарат |
|
Жидкий экстракт |
|
|
|
Фасовка
Рисунок 8 – Схема получения антибиотиков в процессе микробного биосинтеза (по Н.Е. Егорову, 1994)
52
2.6. Условия производства антибиотиков
Поскольку основным этапом микробиологического производства антибиотиков является процесс ферментации продуцента, осуществляющего синтез целевого продукта, особое внимание необходимо уделять конструкции ферментеров их автоматизации и обеспечению надежности производственного процесса. Ферментеры должны быть оснащены электронными стойками автоматического управлениями процессом ферментации в автоматическом режиме и контролировать такие технологические параметры, как значения рН, уровень растворенного кислорода (рО2), температуру, давление, число оборотов мешалки, уровень пены в аппарате, расход подаваемого на аэрацию воздуха. Также необходимо учитывать возможность последовательной передачи биологического материала из аппаратов меньшего объема в аппараты большего объема. Для обеспечения стерильных условий ферментации и защиты окружающей среды в составе обвязки ферментера должны присутствовать стерилизующие фильтры тонкой очистки, например, фирмы PALL или MILLIPORE (DURAPORE, MILIDISK), обеспечивающие подачу в ферментер стерильного воздуха и очистку отработанного воздуха, выбрасываемого в атмосферу.
Аэрация культуральной жидкости в стерильных условиях. Сте-
пень бактериальной очистки воздуха, подаваемого на аэрацию культуральной жидкости, во многих случаях должна быть выше, чем для воздуха, подаваемого в «чистые» помещения наиболее ответственных стадий фармацевтического производства инъекционных препаратов.
В полном объеме схема получения стерильного сжатого воздуха многостадийна и включает в себя фильтр на входе в компрессор, компрессор, теплообменники для охлаждения и нагрева воздуха, предфильтр, фильтр тонкой очистки. Наиболее ответственным узлом в этом перечне является фильтр тонкой очистки, который должен удовлетворять следующим требованиям:
обеспечить гарантию 100 % удаления бактерий из сухого и влажного воздуха;
иметь достаточно длительный срок службы (не менее 1 года);
53
работать при низком исходном перепаде давления в продолжении длительного периода времени;
обладать свойствами, позволяющими периодически осуществлять стерилизацию паром;
быть простым в обслуживании;
иметь надежное уплотнение фильтрующего элемента.
По механизму фильтрации фильтры тонкой очистки подразделяются на поверхностные и глубинные.
Глубинные фильтры удерживают отделяемые частицы во всем объеме фильтрующего материала. Для их изготовления в настоящее время используют волокнистые, порошковые и прессованные материалы, а также пластик на бумажной или асбестовой основе. Вероятность задержки микроорганизмов в таких фильтрах связана с толщиной фильтрующего слоя, вследствие чего степень эффективности находится в диапазоне 90–99,999 %. Теоретически нельзя удалить из воздушного потока 100 % находящихся в нем микроорганизмов. Поэтому применение глубинных фильтров возможно только на стадии предварительной фильтрации.
Поверхностным фильтрам свойственна абсолютная эффективность (100 %). Механизм их действия подобен работе сита. Частицы и микроорганизмы не могут преодолеть мембрану, так как она имеет поры, размер которых меньше, чем размер этих частиц и микроорганизмов. Как правило, мембраны изготавливают в виде простых листов из эфира целлюлозы, чистой целлюлозы, неорганических микроволокон, покрытых смолами, полипропилена, нейлона, капрона, фторопласта и других материалов, изготовленных как одно целое. Размеры пор мембран в этих материалах лежат в широком диапазоне от 0,1 мкм до 5 мкм. Для стерилизующих фильтров воздуха, подаваемого в ферментеры, как правило, используют мембраны с размерами пор 0,22 мкм. Большинство фильтров выдерживают в течение 1 года многократную стерилизацию при режиме 121 °С в течение 30 мин, либо 141 °С в течение 10 мин.
Регулирование параметров процесса биосинтеза. Управление тех-
нологическим процессом микробиологического синтеза заключается в поддержании на заданных уровнях значений основных технологических параметров.
54
Наиболее широко применяют следующие контуры управления:
регулирование температуры культуральной жидкости путем изменения параметров теплоносителя;
контроль и регулирование концентрации растворенного кислорода (рО2) путем изменения расхода воздуха, подаваемого на аэрацию или числа оборотов мешалки;
поддержание давления в ферментере путем открытия или закрытия клапана на линии выходящего воздуха;
стабилизация рН путем добавления кислоты или щелочи;
поддержание уровня пены в заданных пределах путем внесения пеногасителя, снижения расхода воздуха или уменьшения числа оборотов мешалки;
поддержание на заданном уровне концентрации ингредиентов субстрата в культуральной жидкости путем их добавления в ферментер.
Регулирование температуры суспензии в ферментере. Процесс обеспечивается за счет подачи в «рубашку» аппарата теплоносителя – смеси воды и пара, транспортируемой циркуляционным насосом. Регулировка
температуры теплоносителя в диапазоне от 0 до 150 °С с точностью
± 0,5 °С обеспечивается за счет установления требуемой температуры на стойке управления. Паровоздушная смесь, пройдя через обратный клапан и инжектор, в котором происходит смешение воды и пара, поступает в рубашку ферментера. После выхода из рубашки, теплоноситель поступает на вход циркуляционного насоса. Избыток теплоносителя, образующийся за счет конденсации пара, отводится в канализацию через отрегулированный на определенное давление клапан.
Контроль уровня растворенного кислорода. Растворенный кисло-
род имеет исключительно большое значение в процессах биосинтеза, характеризующихся интенсивными скоростями роста биомассы и повышенными вязкостями культуральной жидкости, что характерно для процессов получения антибиотиков. При анаэробном метаболизме кислород играет роль акцептора электронов или водорода при участии фермента оксидазы. Кроме того, с помощью оксигеназ кислород может встраиваться в молекулу углеродных субстратов при их катаболизме. Причем, требующееся на единицу биомассы количество кислорода зависит от свойств субстрата
55
(углеводы требуют меньшего количества кислорода, а углеводороды – зна- |
стабилизирующих пузырьки пены. В стойких пенах длительность суще- |
чительно большего). Экспериментально установлено, что в случае фермен- |
ствования пузырька 1–15 мин. |
тации бактерий и грибов, использующих в качестве источника энергии уг- |
Интенсивное пенообразование затрудняет максимальное использо- |
леводы, на 1 г сухой биомассы требуется 1 г кислорода (теоретически для |
вание емкости биореактора, так как способствует выбросу пены и потери |
биосинтеза 3,39 г сухой биомассы – 1 г кислорода). |
целевого продукта. Кроме того выброс пены зачастую приводит к несте- |
Кислород является трудно растворимым газом (8 мг/л при 25 °С; |
рильности продукта. Для пеногашения в настоящее время использую раз- |
7 мг/л при 35 °С), причем наличие солей в жидкости существенно снижает |
личные методы: механические (разрушение пены за счет ударного воздей- |
растворимость в ней кислорода. При высоком содержании биомассы в |
ствия твердых поверхностей, воздействия струями жидкости или газа, рез- |
культуральной жидкости (потребление кислорода может достигать 50 г/л) |
кое изменение давления и др.); химические (добавление поверхностно- |
необходимо интенсивно пополнять среду растворенным кислородом. Дат- |
активных веществ, уменьшающих прочность пленок, добавление веществ, |
чики, регистрирующие концентрацию растворенного кислорода, выдержи- |
связывающих пенообразователи в поверхностно-неактивные комплексы); |
вающие многократную стерилизацию, основаны на методе полярографи- |
физические методы (электрическое пеногашение, воздействие колебаний |
ческого определения диффузионного потока кислорода через полупрони- |
звуковой или ультразвуковой частоты и др.); стабилизация уровня пены |
цаемую мембрану, под которой располагается анод (материал – свинец или |
путем временного уменьшения подачи воздуха или временного прекраще- |
серебро) и катод (материал – платина) в растворе электролита. Датчики |
ния механического перемешивания, вывода избыточной пены из биореак- |
имеют температурную компенсацию в диапазоне 0–50 °С. |
тора. Наиболее эффективными по нашему мнению являются химические и |
Рабочее давление в ферментере может изменяться от 0 до 2,5 атм. |
механические способы пеногашения или их комбинации. Проблему вспе- |
Результирующий сигнал от датчика давления преобразуется в электриче- |
нивания можно решить, если оставить в верхней части реактора достаточ- |
ский сигнал и по команде от блока управлению с помощью клапана обрат- |
ный объем пустого пространства, в котором бы лопались пузырьки возду- |
ного давления поддерживает его в заданных пределах. Контур давления |
ха, но это уменьшает рабочий объем реактора на 25–30 %. |
дополнительно оснащен контрольным манометром. |
Таким образом, регулирование уровня пены осуществляется не- |
Концентрация водородных ионов (рН) – важный параметр, влияю- |
сколькими способами: |
щий на рост микроорганизмов и образование конечного продукта. Бакте- |
воздействие на пену химическими и физико-химическими сред- |
рии обычно растут в диапазоне значений рН 4–8, дрожжи при рН 3–6, мик- |
ствами; |
роскопические грибы при рН 3–7. По разным причинам рН в ходе фермен- |
разрушение пены механическими, гидро- и аэродинамическими |
тации имеют тенденцию к изменению, поэтому необходима схема управ- |
способами; |
ления и поддержания рН на оптимальном уровне. Регулирование рН осу- |
разрушение пены колебаниями звуковой и ультразвуковой часто- |
ществляется автоматически добавлением кислоты или щелочи при помощи |
ты; |
перистальтических насосов (температурная компенсация 0–100 °С). |
стабилизация уровня пены уменьшением расхода аэрирующего |
Регулирование уровня пены. Процесс культивирования аэробных |
воздуха и снижением числа оборотов мешалки. |
микроорганизмов сопровождается образованием пены. Это связано, во- |
Для химического пеногашения наибольшее распространение полу- |
первых, с введением в жидкость воздуха, во-вторых, с наличием в составе |
чили полиэфирные препараты пропинол Б-400 и адеканоль, полиметилси- |
культуральной жидкости белков и других поверхностно активных веществ, |
локсаны АС-60 и др. В ходе культивирования химические поногасители |
56 |
57 |